- •Государственная фармакопея республики беларусь первое издание
- •Республики Беларусь
- •1. Общие сведения
- •1.1. Общие положения
- •1.2. Другие положения, распространяющиеся на общие и частные фармакопейные статьи
- •Условия хранения лекарственного средства
- •Пределы, указываемые на упаковке
- •1.5. Сокращения и обозначения
- •1.6. Единицы международной системы (си), используемые в фармакопейных статьях, и их соответствие другим единицам
- •2. Методы анализа
- •2.1. Оборудование
- •2.1.1. Каплемер
- •2.1.2. Сравнительная таблица пористости стеклянных фильтров
- •Пористость фильтра (ф.Евр.) (1)
- •Максимальный диаметр пор в микрометрах
- •2.1.3. Лампы с ультрафиолетовым излучением для аналитических целей
- •2.1.4. Сита
- •2.2. Физические и физико-химические методы
- •2.2.1. Определение прозрачности и степени мутности жидкостей
- •2.2.2. Определение степени окрашивания жидкостей
- •2.2.3. Потенциометрическое определение рН
- •2.2.4. Зависимость между реакцией раствора, приблизительным значением рН и цветом индикаторов
- •Изменение цвета
- •2.2.5. Относительная плотность
- •2.2.6. Показатель преломления (индекс рефракции)
- •2.2.7. Оптическое вращение
- •2.2.8. Вязкость
- •1/Прив 1
- •2.2.9. Метод капиллярной вискозиметрии
- •2.2.10. Метод ротационной вискозиметрии
- •2.2.11. Температурные пределы перегонки
- •2.2.14. Температура плавления - капиллярный метод
- •2.2.17. Температура каплепадения
- •2.2.18. Температура затвердевания
- •2.2.21. Флуориметрия
- •2.2.22. Атомно-эмиссионная спектрометрия
- •2.2.23. Атомно-абсорбционная спектрометрия
- •2.2.24. Абсорбционная спектрофотометрия в инфракрасной
- •2.2.25. Абсорбционная спектрофотометрия в ультрафиолетовой видимой областях
- •2. Многокомпонентный спектрофотометрический анализ.
- •2.2.26. Бумажная хроматография
- •2.2.27. Тонкослойная хроматография
- •2.2.28. Газовая хроматография
- •2.2.29. Жидкостная хроматография
- •2.2.30. Эксклюзионная хроматография
- •2.2.31. Электрофорез
- •2.2.32. Потеря в массе при высушивании
- •2.2.33. Спектрометрия ядерного магнитного резонанса
- •2.2.34. Термогравиметрия
- •2.2.35. Осмоляльность
- •2.2.36. Потенциометрическое определение концентрации ионов с использованием ионселективных электродов
- •2.2.37. Рентгенофлуоресцентная спектрометрия
- •2.2.38. Удельная электропроводность
- •2.2.39. Молекулярно-массовое распределение декстранов
- •2.2.40. Спектрофотометрия ближнего ик-диапазона
- •2.2.41. Круговой дихроизм
- •2.2.42. Плотность твердых тел
- •2.2.43. Масс-спектрометрия
- •2.2.44. Определение содержания общего органического углерода в воде для фармацевтического применения
- •2.2.45. Сверхкритическая флюидная хроматография
- •2.2.46. Хроматографические методы разделения
- •2.2.47. Капиллярный электрофорез
- •2.2.48. Рамановская спектрометрия (# спектрометрия комбинационного рассеяния)
- •2.2.54. Изоэлектрическое фокусирование
- •2.3.1. Реакции подлинности (идентификации) на ионы и функциональные группы
- •2.3.2. Идентификация жирных масел методом тонкослойной хроматографии
- •2.3.3. Идентификация фенотиазинов методом тонкослойной хроматографии
- •2.3.4. Определение запаха
- •2.4. Испытания на предельное содержание примесей
- •2.4.1. Аммония соли
- •2.4.2. Мышьяк
- •2.4.3. Кальций
- •2.4.6. Магний
- •2.4.7. Магний и щелочноземельные металлы
- •2.4.8. Тяжелые металлы
- •2.4.15. Никель в полиолах
- •2.4.1.6. Общая зола
- •2.4.21. Посторонние масла в жирных маслах методом тонкослойной хроматографии
- •2.4.22. Посторонние жирные кислоты в маслах методом газовой хроматографии
- •2.4.23. Стерины в жирных маслах
- •2.4.24. Идентификация остаточных растворителей и их количественное определение
- •2.4.25. Остаточные количества этиленоксида и диоксана
- •2.4.27. Никель в гидрогенизированных растительных маслах
- •2.5. Методы количественного определения 2.5.1. Кислотное число
- •2.5.3. Гидроксильное число
- •2.5.4. Йодное число
- •2.5.5. Перекисное (пероксидное) число
- •2.5.6. Число омыления
- •2.5.7. Неомыляемые вещества
- •2.5.8. Определение аминного азота в соединениях, которые содержат первичную ароматическую аминогруппу
- •2.5.9. Определение азота после минерализации серной кислотой
- •2.5.10. Метод сжигания в колбе с кислородом
- •2.5.11. Комплексометрическое титрование
- •2.5.12. Вода: полумикрометод (#Метод к.Фишера)
- •2.5.13. Алюминий в адсорбированных вакцинах
- •2.5.14. Кальций в адсорбированных вакцинах
- •2.5.20. Гексозамины в полисахаридных вакцинах
- •2.5.21. Метилпентозы в полисахаридных вакцинах
- •2.5.24. Диоксид углерода в газах
- •2.5.25. Оксид углерода в газах
- •2.5.26. Оксид азота и диоксид азота в газах
- •2.5.27. Кислород в газах
- •2.5.30. Окисляющие вещества
- •2.5.33. Общий белок
- •2.5.34. Уксусная кислота в синтетических пептидах
- •2.6. Биологические испытания
- •2.6.1. Стерильность
- •2.6.2. Микобактерии
- •2.6.3. Испытания на посторонние вирусы с использованием куриных эмбрионов
- •2.6.4. Испытание на вирусы лейкоза
- •2.6.5. Испытание на посторонние вирусы с использованием клеточных культур
- •2.6.6. Испытание на посторонние агенты с использованием цыплят.
- •2.6.7. Микоплазмы
- •2.6.8 Пирогенность
- •2.6.9. Аномальная токсичность
- •2.6.10. Гистамин
- •2.6.11. Депрессорные вещества
- •2.6.12. Микробиологические испытания нестерильной продукции (суммарное количество жизнеспособных аэробов)
- •2.6.13. Микробилогические испытания нестерильной продукции (испытания на наличие специфических микроорганизмов)
- •0,9 % Раствор натрия хлорида
- •1 % Раствор фенолового красного
- •0,5 % Раствор малахитового зеленого
- •2.6.14. Бактериальные эндотоксины
- •1. Предварительные испытания
- •2. Предельное испытание (метод а) (I) Методика
- •2. Полуколичественное испытание (метод в)
- •1. Турбидиметрический принцип (методы с и f)
- •2.6.15. Активатор прекалликреина
- •2.6.16. Испытания на посторонние агенты в вирусных вакцинах для медицинского применения
- •2.6.17. Испытание на антикомплементарную активность иммуноглобулина
- •2.6.18. Испытание живых вирусных вакцин на нейровирулентность
- •2.6.19. Испытание пероральной вакцины полиомиелита на нейровирулентность
- •5.1. Предотвращение загрязнения
- •5.4 Детектирование
- •7.1 Валидация системы для количественного определения методом
- •7.2. Контроль качества реагентов.
- •7.3. Контроль хода испытания.
- •7.4. Внешняя оценка качества
- •2.6.22. Активированные факторы свертывания крови
- •2.7 Биологические методы количественного определения
- •2.7.1. Иммунохимические методы
- •2.7.2. Количественное определение антибиотиков микробиологическим методом
- •2.7.3. Количественное определение кортикотропина
- •2.7.4. Количественное определение фактора свертывания крови VIII
- •2.7.5. Количественное определение гепарина
- •2.7.6. Количественное определение вакцины дифтерии (адсорбированной)
- •2.7.7. Количественное определение вакцины коклюша
- •2.7.8. Количественное определение вакцины столбняка (адсорбированной)
- •2.7.9. Определение функционального состояния Fc-фрагмента иммуноглобулина
- •2.7.10. Количественное определение фактора свертывания крови человека VII
- •2.7.11. Количественное определение фактора свертывания крови человека IX
- •2.7.12. Количественное определение гепарина в концентратах
- •2.7.13. Количественное определение человеческого анти-d-иммуноглобулина
- •2.7.14. Количественное определение антигенной (иммуногенной) активности вакцины гепатита а
- •2.7.15. Количественное определение вакцины гепатита в (rdna)
- •2.7.16. Количественное определение вакцины коклюша (бесклеточной)
- •2.7.17. Количественное определение антитромбина III человека
- •2.7.18. Количественное определение фактора свертывания крови II
- •2.7.19. Количественное определение фактора свертывания крови х
- •2.7.20. Количественное определение инактивированной вакцины полиомиелита in vivo
- •2.7.22. Количественное определение фактора свертывания крови человека XI
- •2.8. Методы анализа лекарственного растительного сырья и лекарственных средств из него
- •2.8.1. Зола, нерастворимая в хлористоводородной кислоте
- •2.8.4. Коэффициент набухания
- •2.8.5. Определение воды в эфирных маслах
- •2.8.10. Растворимость эфирных масел в спирте
- •2.8.11. Определение 1,8-цинеола в эфирных маслах
- •2.8.12. Определение эфирного масла
- •2.8.13. Остаточное количество пестицидов
- •1. Экстракция
- •2. Очистка
- •3. Количественный анализ
- •Относительные времена удерживания инсектицидов
- •2.8.15. Определение показателя горечи
- •2.8.16. Сухой остаток экстрактов
- •2.8.17. Потеря в массе при высушивании экстракта
- •2.9. Фармацевтико-технологические испытания
- •2.9.1. Распадаемость таблеток и капсул
- •2.9.2. Распадаемость суппозиториев и пессариев
- •2.9.3. Тест «растворение» для твердых дозированных форм
- •2.9.4. Тест «растворение» для трансдермальных пластырей
- •2.9.5. Однородность массы для единицы дозированного лекарственного средства
- •2.9.6. Однородность содержания действующего вещества в
- •2.9.7. Прочность таблеток без оболочки на истирание
- •2.9.8. Прочность таблеток на сжатие
- •2.9.9. Измерение консистенции методом пенетрометрии
- •2.9.10 Содержание этанола
- •2.9.11. Испытание на содержание метанола и 2-пропанола
- •2.9.12. Ситовой анализ
- •2.9.15. Насыпной объем
- •2.9.16. Сыпучесть
- •2.9.17. Определение извлекаемого объема парентеральных лекарственных средств
- •Масса действующего вещества высвобожденного при опорожнении
- •Фракция действующего вещества (%)
- •2.9.19. Загрязнение механическими включениями: невидимые частицы.
- •2.9.20. Загрязнение механическими включениями: видимые частицы
- •2.9.21. Загрязнение механическими включениями: метод микроскопии
- •2.9.22. Опредление времени деформации липофильных суппозиториев
- •2.9.23. Определение плотности твердых частиц при помощи пикнометра
- •2.9.24. Устойчивость суппозиториев и пессариев к разрушению
- •2.9.26. Опредедение удельной площади поверхности методом газовой адсорбции
- •III.1.3. Количество образца
- •III.2.1. Метод 1: метод динамического потока
- •III.2.2. Метод 2: метод объёмного анализа
- •2.9.27. Однородность массы одной дозы высвобожденной из многодозового контейнера
- •2.9.28. Определение массы или объема содержимого контейнера для жидких и мягких лекарственных средств
- •3.1. Материалы, используемые для производства контейнеров
- •3.1.1. Материалы, используемые для производства контейнеров для человеческой крови и компонентов
- •3.1.1.1. Материалы на основе пластифицированного поливинилхлорида, используемые для производства
- •3.1.1.2. Материалы на основе пластифицированного поливинилхлорида для трубок, используемых в комплектах для переливания крови и компонентов крови
- •3.1.3. Полиолефины
- •3.1.4. Полиэтилен без добавок для контейнеров для парентеральных и офтальмологических лекарственных средств
- •3.1.5. Полиэтилен с добавками для контейнеров для
- •3.1.6. Полипропилен для контейнеров и укупорочных материалов для парентеральных и офтальмологических лекарственных средств
- •3.1.7. Полиэтиленвинилацетат для контейнеров и трубок для лекарственных средств для парентерального питания
- •3.1.8. Силиконовое масло, используемое в качестве смазывающей добавки
- •3.1.9. Силиконовые эластомеры для укупорочных
- •3.1.10. Материалы на основе непластифицированного поливинилхлорида для контейнеров для неинъекционных водных растворов
- •3.1.11. Материалы на основе непластифицированного поливинилхлорида для контейнеров для твердых лекарственных форм для перорального применения
- •3.1.13. Добавки к пластмассе
- •3.1.14. Материалы на основе пластифицированного поливинилхлорида для контейнеров для водных растворов для внутривенного применения
- •3.1.15. Полиэтилентерефталат для контейнеров для лекарственных средств для непарентерального применения
- •3.2. Контейнеры
- •3.2.1. Стеклянные контейнеры для фармацевтического использования
- •3.2.2. Пластмассовые контейнеры и укупорочные средства для фармацевтического использования
- •3.2.2.1. Пластмассовые контейнеры для водных растворов для парентерального применения
- •3.2.3. Стерильные пластмассовые контейнеры для человеческой крови и ее компонентов
- •3.2.4. Пустые стерильные контейнеры из пластифицированного поливинилхлорида для человеческой крови и ее компонентов
- •3.2.5. Стерильные контейнеры из пластифицированного поливинилхлорида для человеческой крови, содержащие раствор антикоагулянта
- •3.2.6. Комплекты для переливания крови и компонентов крови
- •3.2.8. Стерильные одноразовые пластмассовые шприцы
- •3.2.9. Резиновые укупорочные средства для контейнеров, предназначенных для водных лекарственных средств для парентерального применения, порошков и лиофилизированных порошков
- •4. Реактивы
- •4.1. Реактивы, эталонные растворы, буферные растворы
- •4.1.1. Реактивы
- •4.1.2. Эталонные растворы для испытаний на предельное содержание примесей
- •0,1 М фосфатный буферный раствор рН 8,0. 4008400.
- •4.2. Реактивы, титрованные растворы для объемного нализа
- •1 М щелочной раствор меди-этилендиамина. 3008700
- •5.1 Общие тексты по стерилизации
- •5.1.1. Методы приготовления стерильных продуктов
- •5.1.2. Биологические индикаторы стерилизации
- •5.1.3. Эффективность антимикробных консервантов
- •24 Часа
- •5.1.4. Микробиологическая чистота лекарственных средств
- •5.1.5 .Применение f0 концепции при стерилизации паром водных растворов.
- •5.2. Общая информация о вакцинах
- •5.2.1. Общепринятая терминология
- •5.2.2. Стаи кур, не имеющих конкретных патогенов и используемые для производства вакцин и контроля их качества
- •5.2.3. Субстраты клеток для производства вакцин, используемых людьми
- •5.2.6. Оценка безопасности вакцин
- •5.2.7. Оценка эффективности вакцин
- •5.2.8. Снижение риска передачи возбудителей губчатой энцефалопатии через лекарственные средства
- •1. Общие замечания
- •2. Область применения общей главы
- •3.1. Животные как источник материала
- •3.2. Части тел животных, жидкости и выделения в качестве исходных материалов
- •3.3. Проверка процесса
- •5.3. Статистические методы обработки результатов анализа
- •5.3.1. Статистический анализ результатов биологических исследований и количественных определений
- •1.1. Общие положения и точность
- •2. Рандомизация и независимость конкретных исследований
- •3. Количественные определения, основанные на количественных эффектах
- •3.1. Статистические модели
- •3.2. Модель параллельных линий
- •3.2.2.1 Схема полной рандомизации
- •3.2.2.2 Схема рандомизированных блоков
- •3.3. Модель угловых коэффициентов
- •3.3.5.2 (/7С/)-схема
- •4. Тесты с альтернативным типом эффекта 4.1. Введение
- •4.2. Метод пробит-анализа
- •5.1. Модель параллельных линий.
- •5.2. Модель угловых коэффициентов
- •5.3. Альтернативные эффекты
- •6 Объединение результатов количественного определения 6.1. Введение
- •6.2. Взвешенное объединение результатов количественного определения
- •6.3. Невзвешенное объединение результатов количественного опре- деления
- •6.4. Пример определения взешенной средней активности с доверительн1м интервалом
- •7. Дополнение
- •7.1. Общие линейные модели
- •7.4. Ошибки корреляции
- •8. Таблицы и процедуры генерирования
- •8.5. Случайные размещения
- •8.6. Латинские квадраты
- •9. Принятые обозначения
- •1. Выборка
- •1.1. Среднее зна чение и дисперсия
- •1.3. Доверительные интервалы и оценка их величины.
- •1.4. Односторонние и двусторонние доверительные интервалы.
- •2. Метрологические характеристики методики анализа
- •2.1.1. Объединенная дисперсия и объединенное среднее
- •2.1.2. Критерий Бартлетта.
- •2.1.3. Критерий Кохрейна.
- •2.2. Проверка наличия значимой систематической погрешности.
- •3. Сравнение двух методик анализа по воспроизводимости
- •4. Метрологическая характеристика среднего результата.
- •5. Сравнение средних результатов двух выборок
- •5.3. Известно точное значение величины а.
- •6. Интерпретация результатов анализа, полученных с помощью метрологически аттестованной методики.
- •6.1. Оценка сходимости результатов параллельных определений.
- •6.2. Определение необходимого числа параллельных определений.
- •6.3. Гарантия качества продукции.
- •7. Расчет и статистическая оценка параметров линейной зависимости
- •8. Последовательная схема статистического анализа результатов химических измерений
- •9. Примеры
- •9.1 Вычисление среднего значения и дисперсии.
- •9.2 Проверка однородности выборки малого объема
- •9.3. Вычисление доверительных интервалов и неопределенностей измерений.
- •9.4. Проверка гипотезы равенства дисперсий.
- •9.4.1. Объединение результатов выборок разного объема.
- •9.4.2. Объединение результатов выборок одинакового объема.
- •9.5. Сравнение двух методик анализа по воспроизводимости.
- •9.6. Сравнение средних результатов двух выборок.
- •9.7. Оценка качества продукции.
- •9.8. Контроль содержания салициловой кислоты в салициловом спирте посредством секвенционального анализа.
- •10. Расчет неопределенности функции нескольких случайных переменных
- •10.1. Линейная модель
- •10.1.1. Взвешенное среднее
- •10.2. Подход Уэлча-Сатертуэйта
- •10.3. Примеры расчетов неопределенности функции нескольких переменных
- •10.3.1. Расчет неопределенности вэжх-анализа готового лекарственного средства
- •10.3.1.1. Конечная аналитическая операция
- •10.3.1.2. Суммарная неопределенность пробоподготовки asp,r.
- •10.3.1.3. Расчет суммарной неопределенности анализа aAs,r
- •10.3.2. Прогноз неопределенности спектрофотометрического анализа готового лекарственного средства
- •10.3.3. Расчет среднего значения нескольких неравноточных выборок
- •1. Введение
- •2. Аналитические испытания и методики, подлежащие валидации
- •3. Валидационные характеристики и требования
- •4. Словарь
- •2. Специфичность
- •5. Правильность
- •5.1. Количественное определение
- •5.2. Примеси (количественное содержание).
- •7. Предел обнаружения
- •8. Предел количественного определения
- •8.3. Использование калибровочной прямой и стандартного отклонения сигнала
- •9. Робастность
- •10. Проверка пригодности хроматографической системы
- •3. Неинструментальные испытания на чистоту и предельное содержание примесей
- •5. Разделительные методы
- •6.1. Метод добавок
- •6.2. Сравнение с арбитражным методом
- •5.4. Остаточные количества органических растворителей
- •5.4.1. Введение
- •5.4.2. Область применения
- •5.4.3. Общие положения
- •5.4.4. Предельные содержания остаточных растворителей
- •5.5. Алкоголеметрические таблицы
- •5.6. Отчет об исследовании интерферонов
- •3.3. Процедура исследования
- •3.3.1. Определение уровня доза-ответ
- •5.7. Таблица физических упоминаемых в фармакопеи
- •Вероятность эмиссии
- •Энергия (мЭв)
- •Энергия (мЭв)
- •Вероят ность эмиссии (на
- •Энергия (мЭв)
- •Вероятность эмиссии
- •5.8. Биодоступность и биоэквивалентность генерических лекарственных средств
- •3. Регистрационная оценка взаимозаменяемых лекарственных
- •4. Исследования эквивалентности, необходимые для
- •4.2.1. Исследования биоэквивалентности/биодоступности (исследования на человеке)
- •4.2.2. Общие методические подходы к выполнению исследований биоэк- вивалентности/биодоступности
- •4.2.3. Исследования сравнительной кинетики растворения (исследования вне живого организма)
- •4.3. Отсутствие необходимости в исследованиях биоэквивалентности или биодоступности
- •5. Дизайн и проведение исследований биологической эквивалентности и биодоступности на людях 5.1. Общие требования.
- •5.2. Испытуемые
- •6. Регламент фармакокинетического исследования
- •7. Аналитический метод
- •8. Анализ фармакокинетических данных
- •8.1. Параметры, подлежащие оценке
- •8.1.1. Однократное введение лекарственного средства
- •8.1.2. Многократное введение лекарственного средства
- •9. Исключение резко выделяющихся наблюдений
- •12. Фармакодинамические исследования
- •13. Клинические испытания
- •14. Тест сравнительной кинетики растворения in vitro
- •15. Клинически значимые колебания биодоступности, обуславливающие отказ в регистрации лекарственного средства
- •Лабораторных животных
- •Участие в испытаниях биоэквивалентности/биодоступности
- •Номограмма для определения достаточного числа добровольцев по результатам проведенного исследования.
- •Хорошо растворимые лекарственные средства
- •Средства с высокой степенью абсорбции
- •Перечень терапевтических (лечебных) доз средств на основе лекарственного растительного сырья
- •Основная литература
- •6. Общие статьи на лекарственные формы и субстанции
5.4.4. Предельные содержания остаточных растворителей
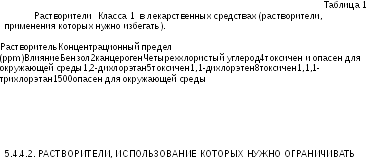
5.4.4.1. РАСТВОРИТЕЛИ, ИСПОЛЬЗОВАНИЕ КОТОРЫХ НУЖНО ИЗБЕГАТЬ
Растворители Класса 1 не должны использоваться в производстве фармацевтических субстанций, вспомогательных веществ и лекарственных средств из-за их высокой токсичности и вредного воздействия на окружающую среду. Однако, если их использование неизбежно для производства лекарственного средства, которое имеет сильно выраженный терапевтический эффект, их количества должны быть ограничены в соответствии с Табл.1, если иное не обосновано. 1,1,1-тирхлорэтан включен в Табл. 1, потому что он опасен для окружающей среды. Установленный предел в 1500 ppm основан на обзоре данных о безопасности.
 Содержание
растворителей, приведенных в Табл. 2,
должно быть ограничено в лекарственных
средствах в связи с их токсичностью.
Данные ДСД даны с точностью до 0,1 мг/сутки,
а концентрации - с точностью до 10
ppm.
Установленные значения не отражают
необходимую аналитическую точность
определения. Точность должна быть
определена как часть валидации (проверки
правильности) методики.
Содержание
растворителей, приведенных в Табл. 2,
должно быть ограничено в лекарственных
средствах в связи с их токсичностью.
Данные ДСД даны с точностью до 0,1 мг/сутки,
а концентрации - с точностью до 10
ppm.
Установленные значения не отражают
необходимую аналитическую точность
определения. Точность должна быть
определена как часть валидации (проверки
правильности) методики.
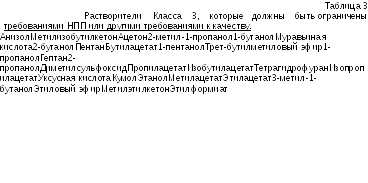 Растворители
Класса 3 (представлены в Табл.3) могут
можно отнести к менее токсичным и
обладающим меньшим риском для здоровья
человека. Класс 3 не включает растворители,
известные как опасные для здоровья
человека в концентрациях, которые обычно
допускаются в лекарственных средствах.
Однако, для многих растворителей Класса
3 не проводилось долгосрочное изучение
токсичности или канцерогенности.
Доступные данные указывают на то, что
они менее токсичны в острых или
краткосрочных испытаниях и дают
отрицательный результат в испытаниях
на генотоксичность (не проявляют
генотоксичность). Считается, что
содержание этих остаточных растворителей
равное 50 мг/сутки или меньше (соответствует
5000
ppm
или 0,5% по Методу 1) приемлемы без
обоснования. Более высокие значения
также могут быть приемлемы, при условии,
что они определяются возможностями
производства, которое отвечает требованиям
надлежащей производственной практики
(НПП).
Растворители
Класса 3 (представлены в Табл.3) могут
можно отнести к менее токсичным и
обладающим меньшим риском для здоровья
человека. Класс 3 не включает растворители,
известные как опасные для здоровья
человека в концентрациях, которые обычно
допускаются в лекарственных средствах.
Однако, для многих растворителей Класса
3 не проводилось долгосрочное изучение
токсичности или канцерогенности.
Доступные данные указывают на то, что
они менее токсичны в острых или
краткосрочных испытаниях и дают
отрицательный результат в испытаниях
на генотоксичность (не проявляют
генотоксичность). Считается, что
содержание этих остаточных растворителей
равное 50 мг/сутки или меньше (соответствует
5000
ppm
или 0,5% по Методу 1) приемлемы без
обоснования. Более высокие значения
также могут быть приемлемы, при условии,
что они определяются возможностями
производства, которое отвечает требованиям
надлежащей производственной практики
(НПП).
5.4.4.4. РАСТВОРИТЕЛИ, ДЛЯ КОТОРЫХ ОТСУТСТВУЮТ НЕОБХОДИМЫЕ
ДАННЫЕ О ТОКСИЧНОСТИ
Растворители, представленные в Табл. 4 могут также представлять интерес для производителей вспомогательных веществ, лекарственных субстанций или лекарственных средств. Однако, для них отсутствуют обоснованные данные о токсичности. Производители должны сами обосновывать остаточные содержания этих растворителей в лекарственных средствах.
 Генотоксичные
канцерогены -
канцерогены, которые вызывают появление
злокачественныз опухолей, воздействуя
на гены или хромосомы.
Генотоксичные
канцерогены -
канцерогены, которые вызывают появление
злокачественныз опухолей, воздействуя
на гены или хромосомы.
Минимальный уровень, с которого наблюдается эффект (МУНЭ) -минимальная доза (вещества) в испытании или серии испытаний, которая вызывает биологически существенное увеличение в частоте или серьезности любых эффектов у людей или животных.
Коэффициент корреляции- коэффициент, определенный в соответствии с обоснованным заключением токсиколога и основанный на экстраполяции на чекловека данных по безопасности, полученных при испытаниях на животных.
Нейротоксичность - способность вещества оказывать неблагоприятное воздействие на нервную систему.
Уровень, при котором не наблюдается эффект (УННЭ) - максимальная доза вещества, при которой нет биологически существенных увеличений в частоте или серьезности любых эффектов у людей или животных.
ДСД - разрешенная (допустимая) суточная доза - максимально приемлемое суточное потребление остаточного растворителя в лекарственном средстве.
Обратимая токсичность - возникновение вредных эффектов, которые вызваны данным веществом и исчезают после прекращения действия вещества.
Предполагаемый канцероген человека - вещество, для которого нет эпидемиологической очевидности канцерогенеза, но есть положительные данные по генотоксичности и очевидность канцерогенеза у грызунов.
Тератогенность - возникновение структурных уродств в развивающемся зародыше, когда вещество принимается в период беременности.
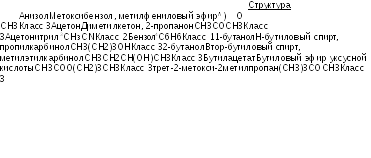
Приложение 1. Список растворителей, включенных в руководящие указания
|
бутилметиловый эфир |
|
|
|
|
Гептан |
Н-гептан |
СН3(СН2)5СН3 |
Класс 3 |
|
Гексан29 |
Н-гексан |
СН3(СН2)4СН3 |
Класс 2 |
|
N,N- диметилацетамид |
Диметиламид уксусной кислоты, ДМА |
СНзСОN(CHз)2 |
Класс 2 |
|
Диметилсульфоксид |
Метилсульфинилметан, Метилсульфоксид, ДМСО |
(СН3)2ЭО |
Класс 3 |
|
N,N- диметилформамид |
Диметиламид уксусной кислоты, ДМФ |
НСО^СНзЬ |
Класс 2 |
|
1,2- диметоксиэтан64 |
Диметиловый эфир этиленгликоля, диметилцеллозольв |
H3COCH2CH2OCH3 |
Класс 2 |
|
1,4-диоксан23 |
Диэтилендиоксид, p-диоксан |
|
Класс 2 |
|
Дихлорметан17 |
Метиленхлорид |
СН2С12 |
Класс 2 |
|
1,2- дихлорэтан14 |
Этилендихлорид |
СH2ClСH2Сl |
Класс 1 |
|
1,1-дихлорэтен15 |
1,1-дихлорэтилен |
H2C = CCl2 |
Класс 1 |
|
1,2-дихлорэтен16а |
1,2-дихлорэтилен |
dHC=CHCl |
Класс 2 |
|
Изобутилацетат |
Изобутиловый эфир уксусной кислоты |
СН3СООСН2СН(СН3)2 |
Класс 3 |
|
Изопропилацетат |
Изопропиловый эфир уксусной кислоты |
СН3СООСН(СН3)2 |
Класс 3 |
|
Ксилол*54 |
Диметилбензол |
(СН3)2С6Н4 |
Класс 2 |
|
Кумол |
Изопропилбензол, 1-метилэтилбензол |
^ СН(СН 3)2 |
Класс 3 |
|
Метанол34 |
Метиловый спирт |
СН3ОН |
Класс 2 |
|
Метилацетат |
Метиловый эфир уксусной кислоты |
СН3СООСН3 |
Класс 3 |
|
3-метил-1 - бутанол |
Изоамиловый спирт, изопентанол |
(СН3)2СНСН2СН2ОН |
Класс 3 |
|
Метилбутилкетон30 |
2-гексанон |
СН3(СН2)3СОСН3 |
Класс 2 |
|
Метилизобутилкетон |
4-метил-2-пентанон МИБК |
СН3СОСН2СН(СН3)2 |
Класс 3 |
|
N- метилпирролидон |
1-метил-2-пирролидон |
|
Класс 2 |
|
2-метил-1-пропанол |
Изобутиловый спирт |
(СН3)2СНСН2ОН |
Класс 3 |
|
Метилциклогексан62 |
Циклогексилметан |
|
Класс 2 |
|
Метилэтилкетон |
2-бутанол, МЭК |
СН3СН2СОСН3 |
Класс 3 |
|
2-метоксиэтанол |
Метилцеллозольв |
СНзОСH2CH2OH |
Класс 2 |
|
Муравьиная кислота |
|
НСООН |
Класс 3 |
|
Нитрометан63 |
|
СНзNO2 |
Класс 2 |
|
Пентан |
Н-пентан |
СН3(СН2)3СН3 |
Класс 3 |
|
1-пентанол |
Амиловый спирт |
СНз(СН2)зСН2ОН |
Класс 3 |
|
Пиридин49 |
|
|
Класс 2 |
|
1-пропанол |
Пропиловый спирт |
СН3СН2СН2ОН |
Класс 3 |
|
2-пропанол |
Изопропиловый спирт |
(СНзЬСНОН |
Класс 3 |
|
Пропилацетат |
Пропиловый эфир уксусной кислоты |
СН3СООСН2СН2СН3 |
Класс 3 |
|
Сульфолан |
Тетрагидротиофен-1, 1-диоксид |
O O |
Класс 2 |
|
Тетрагидрофуран |
Тетраметиленоксид |
О |
Класс 3 |
|
Тетралин61 |
1,2,3,4- тетрагидронафталин |
СО |
Класс 2 |
|
Толуол51 |
Метилбензол |
^CH3 |
Класс 2 |
|
1,1,1-трихлорэтан52 |
Метилхлороформ |
CH3CCl3 |
Класс 1 |
|
1,1,2- трихлорэтен53 |
Трихлорэтен |
HdC=CCl2 |
Класс 2 |
|
Уксусная кислота |
Этановая кислота |
СН3СООН |
Класс 3 |
|
Формамид |
Метанамид |
НСОNH2 |
Класс 2 |
|
Хлорбензол58 |
|
|
Класс 2 |
|
Хлороформ11 |
Трихлорметан |
СНС1з |
Класс 2 |
|
Циклогексан13 |
Гексаметилен |
о |
Класс 2 |
|
Четыреххлористый углерод10 |
Тетрахлорметан |
CCl4 |
Класс 1 |
|
Этанол |
Этиловый спирт |
СН3СН2ОН |
Класс 3 |
|
Этилацетат |
Этиловый эфир уксусной кислоты |
СН3СООСН2СН3 |
Класс 3 |
|
Этиленгликоль |
1,2-дигидроксиэтан, 1,2-этандиол |
НОСН2СН2ОН |
Класс 2 |
|
Этиловый эфир |
Диэтиловый эфир, этоксиэтан, 1,1-оксибисэтан, серный эфир |
СН3СН2ОСН2СН3 |
Класс 3 |
|
Этилформиат |
Этиловый эфир муравьиной кислоты |
НСООСН2СН3 |
Класс 3 |
|
2-этоксиэтанол |
Целлозоль |
СН3СН2ОСН2СН2ОН |
Класс 2 |
*- обычно 60% м-ксилола, 14% п-ксилола, 9% o-ксилола с 17% этилбензола. Примечание: числовые индексы растворителей (цифры вверху) соответствуют номерам пиков на типичных хроматограммах остаточных растворителей (рис.2.4.24.-1, рис.2.4.24.-2, рис.2.4.24.-3, рис.2.4.24.-4) в разделе 2.4.24.
ПРИЛОЖЕНИЕ 2. ДОПОЛНИТЕЛЬНЫЕ ДАННЫЕ
А 2.1. ВЛИЯНИЕ ОРГАНИЧЕСКИХ ЛЕТУЧИХ РАСТВОРИТЕЛЕЙ НА ОКРУЖАЮЩУЮ
СРЕДУ
Некоторые из остаточных растворителей, часто используемых в фармацевтическом производстве, внесены в перечень токсичных химических соединений в монографиях «Критерии здоровья окружающей среды» (ЕНС) и «Объединенная система информации риска» (IRIS). Цели таких организаций, как Международная программа по химической безопасности (IPSC), Управление по охране окружающей среды США (USEPA), Управление лекарственных средств и пищевых продуктов (USFDA) включают определение предельного содержания химических веществ. Основная их цель - защита человеческого здоровья и окружающей среды от возможного негативного влияния химических соединений в результате длительного воздействия. Методы, используемые для оценки максимальных, безопасных пределов воздействия, обычно основываются на долгосрочных исследованиях. Когда данные долгосрочных испытаний недоступны, могут быть использованы данные краткосрочных испытаний с модификацией подхода, например, использование более высоких коэффициентов корреляции.
Подход, описанный в настоящей статье, относится прежде всего к долгосрочным воздействиям или воздействиям на продолжительность жизни популяции окружающей среды, в частности, воздуха,продовольствия, питьевой воды
и др.
А 2.2. ОСТАТОЧНЫЕ РАСТВОРИТЕЛИ В ЛЕКАРСТВЕННЫХ СРЕДСТВАХ
Пределы воздействия в этой статье установлены в соответствии с методологией и данными токсичности, приведенными в монографиях ECH и IRIS. Однако, при установлении пределов воздействия должны быть приняты некоторые допущения относительно остаточных растворителей, которые используются в процессе синтеза и изготовления лекарственных средств, а именно:
Пациенты используют лекарственные средства для лечения болезней или для профилактики с целью избежать инфекции или болезни.
Предположение о воздействии на продолжительность жизни пациента не обязательно для большинства лекарственных средств, но может рассматриваться как рабочая гипотеза, чтобы уменьшить риск для здоровья человека.
Остаточные растворители - неизбежные компоненты фармацевтического производства и зачастую являются составной частью лекарственных средств.
Остаточные растворители не должны превышать рекомендуемые концентрации, кроме исключительных обстоятельств.
Данные о токсикологических испытаниях, которые используются для определения приемлемых концентраций остаточных растворителей, должны быть зафиксированы с использованием соответствующих протоколов, описанных, например, в документах OECD, EPA и FDA Red Book.
ПРИЛОЖЕНИЕ 3. МЕТОДЫ УСТАНОВЛЕНИЯ ДОПУСТИМОЙ СУТОЧНОЙ ДОЗЫ
Для оценки риска канцерогенных растворителей Класса 1 используют метод Гейлора-Коделя (Gaylor, D.W. and Kodell, R.l.: Linear Interpolation algorithm for low dose assessment of toxic substance. J. Environ. Pathology, 4, 305, 1980). Для установления ДСД экстраполяцию с использованием математических моделей следует применять только в тех случаях, когда есть достоверные данные о канцерогенности. ДСД для растворителей Класса 1 также может определяться с использованием высокого значения коэффициета корреляции (например, от 10000 до 100000) для уровня, при котором эффект не наблюдается. Обнаружение и количественное определение этих растворителей следует проводить валидированными аналитическими методиками.
Предельные содержания для растворителей Класса 2 в этом руководстве были установлены путем вычисления значений ДСД согласно методикам определения предельного содержания растворителей в лекарственных средствах (Pharmacopeial Forum, ноябрь-декабрь 1989г.) и методам, принятым IPCS для оценки риска химических веществ в отношении здоровья человека (Environmental Health Criteria 170, ВОЗ, 1994). Эти методы подобны тем, которые используют USEPA (IRIS), USFDA (Красная книга) и др. Метод описан ниже, чтобы пояснить происхождение значений ДСД. Чтобы использовать значения ДСД, приведенные в таблице Раздела 4 этого документа, нет необходимости производить эти вычисления.
При экспериметах на животных значения ДСД рассчитывают исходя из уровня, при котором эффект не наблюдается (УННЭ) или уровня, при котором наблюдается самый низкий эффект (МУНЭ) по формуле:
УННЭ ■ Масса тела
ДСД = ,
F ■ F2 ■ F3 ■ F4 ■ F5
Значение ДСД преимущественно получают на основании УННЭ. Если значения УННЭ неизвестны, могут быть использованы значения МУНЭ. Коэффициенты корреляции, предложенные здесь для экстраполяции на человека данных, полученных на животных, это те же «коэффициенты неопределенности», которые использовались в монографии «Критерии здоровья окружающей среды» (Environmental Health Criteria 170, ВОЗ, Женева, 1994) и «коэффициенты корреляции» или «коэффициенты безопасности» - в «Pharmacopeial Forum". Во всех расчетах принимается предположение о 100% системном воздействии независимо от способа применения лекарств.
Коэффициенты корреляции:
F1 - коэффициент корреляции для расчета экстраполяции между видами F1 = 5 при экстраполяции на человека данных, полученных при исследованиях на крысах
F1 = 12 при экстраполяции на человека данных, полученных при исследованиях на мышах
F1 = 2 при экстраполяции на человека данных, полученных при исследованиях на собаках
F1 = 2,5 при экстраполяции на человека данных, полученных при исследованиях на кроликах
F1 = 3 при экстраполяции на человека данных, полученных при исследованиях на обезъянах
F1 = 10 при экстраполяции на человека данных, полученных при исследованиях на других животных
F1 принимает во внимание отношение площади поверхности тела: к весу тела соответствующих видов животных и человека. Площадь поверхности рассчитывается следующим образом:
S = kM 0,67,
где:
М - масса тела,
k - константа, принята равной 10.
Массы тела, используемые в уравнении, представлены в таблице А 3.1.
F2 = коэффициент 10 , учитывающий индивидуальную изменчивость . Для всех органических растворителей, приведенных в данном руководстве, коэффициент обычно принимают равным 10.
F3 = переменный коэффициент для расчета испытаний токсичности кратковременных воздействий.
F3 = 1, для испытаний, которые длятся по меньшей мере в течение периода равного половине продолжительности жизни животных (1 год для грызунов и кроликов; 7 лет для собак, котов и обезьян).
F3 = 1, для репродуктивных (воспроизводительных) испытаний, которые охватывают весь период органогенеза.
F3 = 2, для испытаний в течение 6 месяцев на грызунах, или 3,5 лет - не на грызунах.
F3 = 5, для 3-х месячных испытаний на грызунах, или 2-х летних - на не грызунах.
F3 = 10, для испытаний более короткой продолжительности.
Для всех промежуточных испытаний необходимо использовать более высокий коэффициент (например, для 9-месячных испытаний на грызунах используется коэффициент =2).
F4 = коэффициент, который может применяться при высокой токсичности растворителя, например, негенотоксичной канцерогенности, нейротоксичности или тератогенности. В испытаниях репродуктивной токсичности используются следующие коэффициенты:
F4 = 1, для эмбриональной токсичности, связанной с материнской токсичностью (интоксикацией)
F4 = 5, для эмбриональной токсичности (интоксикацией), не связанной с материнской
F4 = 5, для тератогенного эффекта, связанного с материнской интоксикацией F4 = 10, для тератогенного эффекта, не связанного с материнской интоксикацией.
F5 = переменный коэффициент, который может применяться, если УННЭ (уровень, не вызывающий эффекта) не был установлен. Когда доступны только данные уровня МУНЭ (уровень, вызывающий минимальный эффект) то, в зависимости от уровня токсичности, может использоваться коэффициент вплоть до
10.
Допускается, что масса тела взрослого человека любого пола равна 50 кг. Этот относительно низкий вес обеспечивает дополнительный коэффициент безопасности стандартному весу человека 60 или 70 кг, который часто используется в таких вычислениях. Известно, что многие взрослые пациенты весят менее 50 кг, поэтому в этом случае при определении ДСД используются другие коэффициенты. Если лекарственное средство, содержащее растворитель, предназначено длч педиатрии, то необходимо сделать корректировку на более низкую массу тела.
Как пример применения этого уравнения, рассмотрим испытание токсичности ацетонитрила на мышах, которое было описано в Pharmeuropa, т.9, №1. Дополнение. Апрель 1997, с. S24. Установлено, что значение УННЭ - 50,7 мг/кг • сутки. ДСД для ацетонитрила при этом рассчитывали следующим образом: „„„ 50,7 мг ■ кг 1 ■ сутки 1 ■ 50кг
ДСД = — = 4,22 мг / сутки
12■10■5■1■l
В этом примере
F1 = 12, учитывает экстраполяцию на человека данных, полученных при исследованиях на мышах
F2 = 10, учитывает индивидуальную изменчивость
F3 = 5, так как продолжительность испытаний составила только 13 недель
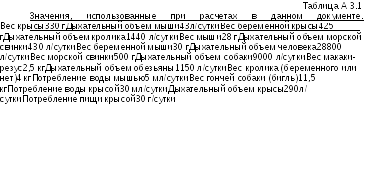
F4 = 1, так как с серьезной токсичностью не сталкивались
 F5
= 1,
так как не был определен уровень, не
вызывающий эффекта
F5
= 1,
так как не был определен уровень, не
вызывающий эффекта
Для перерасчета концентраций газов, используемых в дыхательных (ингаляторных) испытаниях из ppm в мг/л или мг/м3 , использовали уравнение для идеального газа: PV = nRT. Рассмотрим в качестве примера испытание репродуктивной токсичности крысы в результате вдыхания четыреххлористого углерода (М.м. 153,84), описанное в Pharmeurope, т.9, №1, Дополнение, апрель
1997, стр. S9.
n P 300 -10-6атм. ■ 153840мг ■ моль-1 4615мг
— = = = = 1,89 мг / л
V RT 0,082л ■ атм. ■ К -1 ■ моль-1 ■ 298 ■ К 24,45л
Для приведения к мг/м3 использовали соотношение 1000 л = 1 м3