
- •Государственная фармакопея республики беларусь первое издание
- •Республики Беларусь
- •1. Общие сведения
- •1.1. Общие положения
- •1.2. Другие положения, распространяющиеся на общие и частные фармакопейные статьи
- •Условия хранения лекарственного средства
- •Пределы, указываемые на упаковке
- •1.5. Сокращения и обозначения
- •1.6. Единицы международной системы (си), используемые в фармакопейных статьях, и их соответствие другим единицам
- •2. Методы анализа
- •2.1. Оборудование
- •2.1.1. Каплемер
- •2.1.2. Сравнительная таблица пористости стеклянных фильтров
- •Пористость фильтра (ф.Евр.) (1)
- •Максимальный диаметр пор в микрометрах
- •2.1.3. Лампы с ультрафиолетовым излучением для аналитических целей
- •2.1.4. Сита
- •2.2. Физические и физико-химические методы
- •2.2.1. Определение прозрачности и степени мутности жидкостей
- •2.2.2. Определение степени окрашивания жидкостей
- •2.2.3. Потенциометрическое определение рН
- •2.2.4. Зависимость между реакцией раствора, приблизительным значением рН и цветом индикаторов
- •Изменение цвета
- •2.2.5. Относительная плотность
- •2.2.6. Показатель преломления (индекс рефракции)
- •2.2.7. Оптическое вращение
- •2.2.8. Вязкость
- •1/Прив 1
- •2.2.9. Метод капиллярной вискозиметрии
- •2.2.10. Метод ротационной вискозиметрии
- •2.2.11. Температурные пределы перегонки
- •2.2.14. Температура плавления - капиллярный метод
- •2.2.17. Температура каплепадения
- •2.2.18. Температура затвердевания
- •2.2.21. Флуориметрия
- •2.2.22. Атомно-эмиссионная спектрометрия
- •2.2.23. Атомно-абсорбционная спектрометрия
- •2.2.24. Абсорбционная спектрофотометрия в инфракрасной
- •2.2.25. Абсорбционная спектрофотометрия в ультрафиолетовой видимой областях
- •2. Многокомпонентный спектрофотометрический анализ.
- •2.2.26. Бумажная хроматография
- •2.2.27. Тонкослойная хроматография
- •2.2.28. Газовая хроматография
- •2.2.29. Жидкостная хроматография
- •2.2.30. Эксклюзионная хроматография
- •2.2.31. Электрофорез
- •2.2.32. Потеря в массе при высушивании
- •2.2.33. Спектрометрия ядерного магнитного резонанса
- •2.2.34. Термогравиметрия
- •2.2.35. Осмоляльность
- •2.2.36. Потенциометрическое определение концентрации ионов с использованием ионселективных электродов
- •2.2.37. Рентгенофлуоресцентная спектрометрия
- •2.2.38. Удельная электропроводность
- •2.2.39. Молекулярно-массовое распределение декстранов
- •2.2.40. Спектрофотометрия ближнего ик-диапазона
- •2.2.41. Круговой дихроизм
- •2.2.42. Плотность твердых тел
- •2.2.43. Масс-спектрометрия
- •2.2.44. Определение содержания общего органического углерода в воде для фармацевтического применения
- •2.2.45. Сверхкритическая флюидная хроматография
- •2.2.46. Хроматографические методы разделения
- •2.2.47. Капиллярный электрофорез
- •2.2.48. Рамановская спектрометрия (# спектрометрия комбинационного рассеяния)
- •2.2.54. Изоэлектрическое фокусирование
- •2.3.1. Реакции подлинности (идентификации) на ионы и функциональные группы
- •2.3.2. Идентификация жирных масел методом тонкослойной хроматографии
- •2.3.3. Идентификация фенотиазинов методом тонкослойной хроматографии
- •2.3.4. Определение запаха
- •2.4. Испытания на предельное содержание примесей
- •2.4.1. Аммония соли
- •2.4.2. Мышьяк
- •2.4.3. Кальций
- •2.4.6. Магний
- •2.4.7. Магний и щелочноземельные металлы
- •2.4.8. Тяжелые металлы
- •2.4.15. Никель в полиолах
- •2.4.1.6. Общая зола
- •2.4.21. Посторонние масла в жирных маслах методом тонкослойной хроматографии
- •2.4.22. Посторонние жирные кислоты в маслах методом газовой хроматографии
- •2.4.23. Стерины в жирных маслах
- •2.4.24. Идентификация остаточных растворителей и их количественное определение
- •2.4.25. Остаточные количества этиленоксида и диоксана
- •2.4.27. Никель в гидрогенизированных растительных маслах
- •2.5. Методы количественного определения 2.5.1. Кислотное число
- •2.5.3. Гидроксильное число
- •2.5.4. Йодное число
- •2.5.5. Перекисное (пероксидное) число
- •2.5.6. Число омыления
- •2.5.7. Неомыляемые вещества
- •2.5.8. Определение аминного азота в соединениях, которые содержат первичную ароматическую аминогруппу
- •2.5.9. Определение азота после минерализации серной кислотой
- •2.5.10. Метод сжигания в колбе с кислородом
- •2.5.11. Комплексометрическое титрование
- •2.5.12. Вода: полумикрометод (#Метод к.Фишера)
- •2.5.13. Алюминий в адсорбированных вакцинах
- •2.5.14. Кальций в адсорбированных вакцинах
- •2.5.20. Гексозамины в полисахаридных вакцинах
- •2.5.21. Метилпентозы в полисахаридных вакцинах
- •2.5.24. Диоксид углерода в газах
- •2.5.25. Оксид углерода в газах
- •2.5.26. Оксид азота и диоксид азота в газах
- •2.5.27. Кислород в газах
- •2.5.30. Окисляющие вещества
- •2.5.33. Общий белок
- •2.5.34. Уксусная кислота в синтетических пептидах
- •2.6. Биологические испытания
- •2.6.1. Стерильность
- •2.6.2. Микобактерии
- •2.6.3. Испытания на посторонние вирусы с использованием куриных эмбрионов
- •2.6.4. Испытание на вирусы лейкоза
- •2.6.5. Испытание на посторонние вирусы с использованием клеточных культур
- •2.6.6. Испытание на посторонние агенты с использованием цыплят.
- •2.6.7. Микоплазмы
- •2.6.8 Пирогенность
- •2.6.9. Аномальная токсичность
- •2.6.10. Гистамин
- •2.6.11. Депрессорные вещества
- •2.6.12. Микробиологические испытания нестерильной продукции (суммарное количество жизнеспособных аэробов)
- •2.6.13. Микробилогические испытания нестерильной продукции (испытания на наличие специфических микроорганизмов)
- •0,9 % Раствор натрия хлорида
- •1 % Раствор фенолового красного
- •0,5 % Раствор малахитового зеленого
- •2.6.14. Бактериальные эндотоксины
- •1. Предварительные испытания
- •2. Предельное испытание (метод а) (I) Методика
- •2. Полуколичественное испытание (метод в)
- •1. Турбидиметрический принцип (методы с и f)
- •2.6.15. Активатор прекалликреина
- •2.6.16. Испытания на посторонние агенты в вирусных вакцинах для медицинского применения
- •2.6.17. Испытание на антикомплементарную активность иммуноглобулина
- •2.6.18. Испытание живых вирусных вакцин на нейровирулентность
- •2.6.19. Испытание пероральной вакцины полиомиелита на нейровирулентность
- •5.1. Предотвращение загрязнения
- •5.4 Детектирование
- •7.1 Валидация системы для количественного определения методом
- •7.2. Контроль качества реагентов.
- •7.3. Контроль хода испытания.
- •7.4. Внешняя оценка качества
- •2.6.22. Активированные факторы свертывания крови
- •2.7 Биологические методы количественного определения
- •2.7.1. Иммунохимические методы
- •2.7.2. Количественное определение антибиотиков микробиологическим методом
- •2.7.3. Количественное определение кортикотропина
- •2.7.4. Количественное определение фактора свертывания крови VIII
- •2.7.5. Количественное определение гепарина
- •2.7.6. Количественное определение вакцины дифтерии (адсорбированной)
- •2.7.7. Количественное определение вакцины коклюша
- •2.7.8. Количественное определение вакцины столбняка (адсорбированной)
- •2.7.9. Определение функционального состояния Fc-фрагмента иммуноглобулина
- •2.7.10. Количественное определение фактора свертывания крови человека VII
- •2.7.11. Количественное определение фактора свертывания крови человека IX
- •2.7.12. Количественное определение гепарина в концентратах
- •2.7.13. Количественное определение человеческого анти-d-иммуноглобулина
- •2.7.14. Количественное определение антигенной (иммуногенной) активности вакцины гепатита а
- •2.7.15. Количественное определение вакцины гепатита в (rdna)
- •2.7.16. Количественное определение вакцины коклюша (бесклеточной)
- •2.7.17. Количественное определение антитромбина III человека
- •2.7.18. Количественное определение фактора свертывания крови II
- •2.7.19. Количественное определение фактора свертывания крови х
- •2.7.20. Количественное определение инактивированной вакцины полиомиелита in vivo
- •2.7.22. Количественное определение фактора свертывания крови человека XI
- •2.8. Методы анализа лекарственного растительного сырья и лекарственных средств из него
- •2.8.1. Зола, нерастворимая в хлористоводородной кислоте
- •2.8.4. Коэффициент набухания
- •2.8.5. Определение воды в эфирных маслах
- •2.8.10. Растворимость эфирных масел в спирте
- •2.8.11. Определение 1,8-цинеола в эфирных маслах
- •2.8.12. Определение эфирного масла
- •2.8.13. Остаточное количество пестицидов
- •1. Экстракция
- •2. Очистка
- •3. Количественный анализ
- •Относительные времена удерживания инсектицидов
- •2.8.15. Определение показателя горечи
- •2.8.16. Сухой остаток экстрактов
- •2.8.17. Потеря в массе при высушивании экстракта
- •2.9. Фармацевтико-технологические испытания
- •2.9.1. Распадаемость таблеток и капсул
- •2.9.2. Распадаемость суппозиториев и пессариев
- •2.9.3. Тест «растворение» для твердых дозированных форм
- •2.9.4. Тест «растворение» для трансдермальных пластырей
- •2.9.5. Однородность массы для единицы дозированного лекарственного средства
- •2.9.6. Однородность содержания действующего вещества в
- •2.9.7. Прочность таблеток без оболочки на истирание
- •2.9.8. Прочность таблеток на сжатие
- •2.9.9. Измерение консистенции методом пенетрометрии
- •2.9.10 Содержание этанола
- •2.9.11. Испытание на содержание метанола и 2-пропанола
- •2.9.12. Ситовой анализ
- •2.9.15. Насыпной объем
- •2.9.16. Сыпучесть
- •2.9.17. Определение извлекаемого объема парентеральных лекарственных средств
- •Масса действующего вещества высвобожденного при опорожнении
- •Фракция действующего вещества (%)
- •2.9.19. Загрязнение механическими включениями: невидимые частицы.
- •2.9.20. Загрязнение механическими включениями: видимые частицы
- •2.9.21. Загрязнение механическими включениями: метод микроскопии
- •2.9.22. Опредление времени деформации липофильных суппозиториев
- •2.9.23. Определение плотности твердых частиц при помощи пикнометра
- •2.9.24. Устойчивость суппозиториев и пессариев к разрушению
- •2.9.26. Опредедение удельной площади поверхности методом газовой адсорбции
- •III.1.3. Количество образца
- •III.2.1. Метод 1: метод динамического потока
- •III.2.2. Метод 2: метод объёмного анализа
- •2.9.27. Однородность массы одной дозы высвобожденной из многодозового контейнера
- •2.9.28. Определение массы или объема содержимого контейнера для жидких и мягких лекарственных средств
- •3.1. Материалы, используемые для производства контейнеров
- •3.1.1. Материалы, используемые для производства контейнеров для человеческой крови и компонентов
- •3.1.1.1. Материалы на основе пластифицированного поливинилхлорида, используемые для производства
- •3.1.1.2. Материалы на основе пластифицированного поливинилхлорида для трубок, используемых в комплектах для переливания крови и компонентов крови
- •3.1.3. Полиолефины
- •3.1.4. Полиэтилен без добавок для контейнеров для парентеральных и офтальмологических лекарственных средств
- •3.1.5. Полиэтилен с добавками для контейнеров для
- •3.1.6. Полипропилен для контейнеров и укупорочных материалов для парентеральных и офтальмологических лекарственных средств
- •3.1.7. Полиэтиленвинилацетат для контейнеров и трубок для лекарственных средств для парентерального питания
- •3.1.8. Силиконовое масло, используемое в качестве смазывающей добавки
- •3.1.9. Силиконовые эластомеры для укупорочных
- •3.1.10. Материалы на основе непластифицированного поливинилхлорида для контейнеров для неинъекционных водных растворов
- •3.1.11. Материалы на основе непластифицированного поливинилхлорида для контейнеров для твердых лекарственных форм для перорального применения
- •3.1.13. Добавки к пластмассе
- •3.1.14. Материалы на основе пластифицированного поливинилхлорида для контейнеров для водных растворов для внутривенного применения
- •3.1.15. Полиэтилентерефталат для контейнеров для лекарственных средств для непарентерального применения
- •3.2. Контейнеры
- •3.2.1. Стеклянные контейнеры для фармацевтического использования
- •3.2.2. Пластмассовые контейнеры и укупорочные средства для фармацевтического использования
- •3.2.2.1. Пластмассовые контейнеры для водных растворов для парентерального применения
- •3.2.3. Стерильные пластмассовые контейнеры для человеческой крови и ее компонентов
- •3.2.4. Пустые стерильные контейнеры из пластифицированного поливинилхлорида для человеческой крови и ее компонентов
- •3.2.5. Стерильные контейнеры из пластифицированного поливинилхлорида для человеческой крови, содержащие раствор антикоагулянта
- •3.2.6. Комплекты для переливания крови и компонентов крови
- •3.2.8. Стерильные одноразовые пластмассовые шприцы
- •3.2.9. Резиновые укупорочные средства для контейнеров, предназначенных для водных лекарственных средств для парентерального применения, порошков и лиофилизированных порошков
- •4. Реактивы
- •4.1. Реактивы, эталонные растворы, буферные растворы
- •4.1.1. Реактивы
- •4.1.2. Эталонные растворы для испытаний на предельное содержание примесей
- •0,1 М фосфатный буферный раствор рН 8,0. 4008400.
- •4.2. Реактивы, титрованные растворы для объемного нализа
- •1 М щелочной раствор меди-этилендиамина. 3008700
- •5.1 Общие тексты по стерилизации
- •5.1.1. Методы приготовления стерильных продуктов
- •5.1.2. Биологические индикаторы стерилизации
- •5.1.3. Эффективность антимикробных консервантов
- •24 Часа
- •5.1.4. Микробиологическая чистота лекарственных средств
- •5.1.5 .Применение f0 концепции при стерилизации паром водных растворов.
- •5.2. Общая информация о вакцинах
- •5.2.1. Общепринятая терминология
- •5.2.2. Стаи кур, не имеющих конкретных патогенов и используемые для производства вакцин и контроля их качества
- •5.2.3. Субстраты клеток для производства вакцин, используемых людьми
- •5.2.6. Оценка безопасности вакцин
- •5.2.7. Оценка эффективности вакцин
- •5.2.8. Снижение риска передачи возбудителей губчатой энцефалопатии через лекарственные средства
- •1. Общие замечания
- •2. Область применения общей главы
- •3.1. Животные как источник материала
- •3.2. Части тел животных, жидкости и выделения в качестве исходных материалов
- •3.3. Проверка процесса
- •5.3. Статистические методы обработки результатов анализа
- •5.3.1. Статистический анализ результатов биологических исследований и количественных определений
- •1.1. Общие положения и точность
- •2. Рандомизация и независимость конкретных исследований
- •3. Количественные определения, основанные на количественных эффектах
- •3.1. Статистические модели
- •3.2. Модель параллельных линий
- •3.2.2.1 Схема полной рандомизации
- •3.2.2.2 Схема рандомизированных блоков
- •3.3. Модель угловых коэффициентов
- •3.3.5.2 (/7С/)-схема
- •4. Тесты с альтернативным типом эффекта 4.1. Введение
- •4.2. Метод пробит-анализа
- •5.1. Модель параллельных линий.
- •5.2. Модель угловых коэффициентов
- •5.3. Альтернативные эффекты
- •6 Объединение результатов количественного определения 6.1. Введение
- •6.2. Взвешенное объединение результатов количественного определения
- •6.3. Невзвешенное объединение результатов количественного опре- деления
- •6.4. Пример определения взешенной средней активности с доверительн1м интервалом
- •7. Дополнение
- •7.1. Общие линейные модели
- •7.4. Ошибки корреляции
- •8. Таблицы и процедуры генерирования
- •8.5. Случайные размещения
- •8.6. Латинские квадраты
- •9. Принятые обозначения
- •1. Выборка
- •1.1. Среднее зна чение и дисперсия
- •1.3. Доверительные интервалы и оценка их величины.
- •1.4. Односторонние и двусторонние доверительные интервалы.
- •2. Метрологические характеристики методики анализа
- •2.1.1. Объединенная дисперсия и объединенное среднее
- •2.1.2. Критерий Бартлетта.
- •2.1.3. Критерий Кохрейна.
- •2.2. Проверка наличия значимой систематической погрешности.
- •3. Сравнение двух методик анализа по воспроизводимости
- •4. Метрологическая характеристика среднего результата.
- •5. Сравнение средних результатов двух выборок
- •5.3. Известно точное значение величины а.
- •6. Интерпретация результатов анализа, полученных с помощью метрологически аттестованной методики.
- •6.1. Оценка сходимости результатов параллельных определений.
- •6.2. Определение необходимого числа параллельных определений.
- •6.3. Гарантия качества продукции.
- •7. Расчет и статистическая оценка параметров линейной зависимости
- •8. Последовательная схема статистического анализа результатов химических измерений
- •9. Примеры
- •9.1 Вычисление среднего значения и дисперсии.
- •9.2 Проверка однородности выборки малого объема
- •9.3. Вычисление доверительных интервалов и неопределенностей измерений.
- •9.4. Проверка гипотезы равенства дисперсий.
- •9.4.1. Объединение результатов выборок разного объема.
- •9.4.2. Объединение результатов выборок одинакового объема.
- •9.5. Сравнение двух методик анализа по воспроизводимости.
- •9.6. Сравнение средних результатов двух выборок.
- •9.7. Оценка качества продукции.
- •9.8. Контроль содержания салициловой кислоты в салициловом спирте посредством секвенционального анализа.
- •10. Расчет неопределенности функции нескольких случайных переменных
- •10.1. Линейная модель
- •10.1.1. Взвешенное среднее
- •10.2. Подход Уэлча-Сатертуэйта
- •10.3. Примеры расчетов неопределенности функции нескольких переменных
- •10.3.1. Расчет неопределенности вэжх-анализа готового лекарственного средства
- •10.3.1.1. Конечная аналитическая операция
- •10.3.1.2. Суммарная неопределенность пробоподготовки asp,r.
- •10.3.1.3. Расчет суммарной неопределенности анализа aAs,r
- •10.3.2. Прогноз неопределенности спектрофотометрического анализа готового лекарственного средства
- •10.3.3. Расчет среднего значения нескольких неравноточных выборок
- •1. Введение
- •2. Аналитические испытания и методики, подлежащие валидации
- •3. Валидационные характеристики и требования
- •4. Словарь
- •2. Специфичность
- •5. Правильность
- •5.1. Количественное определение
- •5.2. Примеси (количественное содержание).
- •7. Предел обнаружения
- •8. Предел количественного определения
- •8.3. Использование калибровочной прямой и стандартного отклонения сигнала
- •9. Робастность
- •10. Проверка пригодности хроматографической системы
- •3. Неинструментальные испытания на чистоту и предельное содержание примесей
- •5. Разделительные методы
- •6.1. Метод добавок
- •6.2. Сравнение с арбитражным методом
- •5.4. Остаточные количества органических растворителей
- •5.4.1. Введение
- •5.4.2. Область применения
- •5.4.3. Общие положения
- •5.4.4. Предельные содержания остаточных растворителей
- •5.5. Алкоголеметрические таблицы
- •5.6. Отчет об исследовании интерферонов
- •3.3. Процедура исследования
- •3.3.1. Определение уровня доза-ответ
- •5.7. Таблица физических упоминаемых в фармакопеи
- •Вероятность эмиссии
- •Энергия (мЭв)
- •Энергия (мЭв)
- •Вероят ность эмиссии (на
- •Энергия (мЭв)
- •Вероятность эмиссии
- •5.8. Биодоступность и биоэквивалентность генерических лекарственных средств
- •3. Регистрационная оценка взаимозаменяемых лекарственных
- •4. Исследования эквивалентности, необходимые для
- •4.2.1. Исследования биоэквивалентности/биодоступности (исследования на человеке)
- •4.2.2. Общие методические подходы к выполнению исследований биоэк- вивалентности/биодоступности
- •4.2.3. Исследования сравнительной кинетики растворения (исследования вне живого организма)
- •4.3. Отсутствие необходимости в исследованиях биоэквивалентности или биодоступности
- •5. Дизайн и проведение исследований биологической эквивалентности и биодоступности на людях 5.1. Общие требования.
- •5.2. Испытуемые
- •6. Регламент фармакокинетического исследования
- •7. Аналитический метод
- •8. Анализ фармакокинетических данных
- •8.1. Параметры, подлежащие оценке
- •8.1.1. Однократное введение лекарственного средства
- •8.1.2. Многократное введение лекарственного средства
- •9. Исключение резко выделяющихся наблюдений
- •12. Фармакодинамические исследования
- •13. Клинические испытания
- •14. Тест сравнительной кинетики растворения in vitro
- •15. Клинически значимые колебания биодоступности, обуславливающие отказ в регистрации лекарственного средства
- •Лабораторных животных
- •Участие в испытаниях биоэквивалентности/биодоступности
- •Номограмма для определения достаточного числа добровольцев по результатам проведенного исследования.
- •Хорошо растворимые лекарственные средства
- •Средства с высокой степенью абсорбции
- •Перечень терапевтических (лечебных) доз средств на основе лекарственного растительного сырья
- •Основная литература
- •6. Общие статьи на лекарственные формы и субстанции
5.1. Модель параллельных линий.
5.1.1 ДВУХДОЗОВОЕ МНОГОКРАТНОЕ КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ С ИСПОЛЬЗОВАНИЕМ СХЕМЫ ПОЛНОЙ РАНДОМИЗАЦИИ.
Количественное определение активности кортикотропина путем подкожной инъекции у крыс.
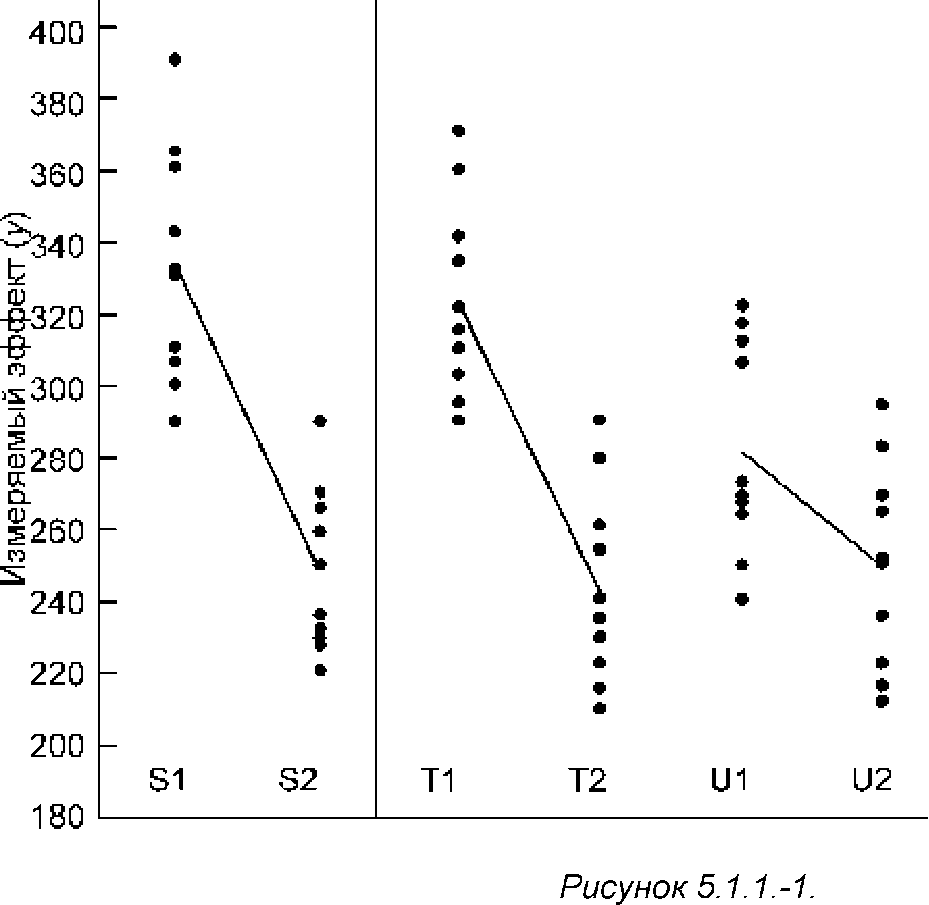
Стандартный препарат вводили в дозах от 0,25 до 1,0 ЕД на 100 г массы тела. Предполагалось, что оба испытуемых препарата имели активность 1 ЕД/мг и вводились в тех же количествах, что и стандартный. Значения эффектов и средние значения приведены в Таблице 5.1.1.-1.
Таблица 5.1.1.-1.
Измеряемый эффект y - масса аскорбиновой кислоты (мг) на 100 г надпочечника.
|
|
Стандартный препарат S |
Испытуемый препарат t |
Испытуемый препарат u | |||
|
|
|
|
t |
|
u1 |
|
|
|
300 |
289 |
310 |
230 |
250 |
236 |
|
|
310 |
221 |
290 |
210 |
268 |
213 |
|
|
330 |
267 |
360 |
280 |
273 |
283 |
|
|
290 |
236 |
341 |
261 |
240 |
269 |
|
|
364 |
250 |
321 |
241 |
307 |
251 |
|
|
328 |
231 |
370 |
290 |
270 |
294 |
|
|
390 |
229 |
303 |
223 |
317 |
223 |
|
|
360 |
269 |
334 |
254 |
312 |
250 |
|
|
342 |
233 |
295 |
216 |
320 |
216 |
|
|
306 |
259 |
315 |
235 |
265 |
265 |
|
Среднее |
332,0 |
248,4 |
323,9 |
244,0 |
282,2 |
250,0 |
Графическое представление результатов не дает поводов сомневаться в однородности дисперсий и нормальности распределения данных, но возникают некоторые сомнения, относительно параллельности результатов для препарата u.
Расчет по формулам, приведенным в Таблицах 3.2.3.-1 и 3.2.3.-2, дал следующие результаты:
Ps = 580,4 Рт = 567,9 Pu = 532,2 10
Hp = —=5
2
Ls = -41,8 Lt = -39,95 Lu = -16,1
Hl = 120 =20
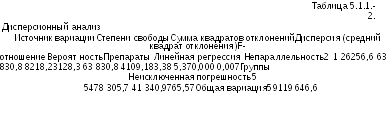 Далее
проводят дисперсионный анализ по
формулам, приведенным в Таблицах
3.2.3.3
и
3.2.3.-4.
Результаты
приведены в Таблице 5.1.1.-2.
Далее
проводят дисперсионный анализ по
формулам, приведенным в Таблицах
3.2.3.3
и
3.2.3.-4.
Результаты
приведены в Таблице 5.1.1.-2.
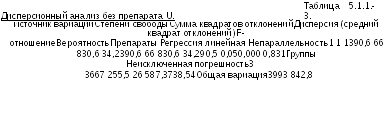 Анализ
подтвердил высокую значимость линейной
регрессии. Отклонение от параллельности
для препарата
u
по
сравнению со стандартным препаратом,
которое ожидалось на основании анализа
графического представления результатов,
тем не менее также оказалось значимым
(р =
0,0075). По
этой причине препарат
U
исключают
и анализ повторяют только для препарата
Т и стандартного препарата.
Анализ
подтвердил высокую значимость линейной
регрессии. Отклонение от параллельности
для препарата
u
по
сравнению со стандартным препаратом,
которое ожидалось на основании анализа
графического представления результатов,
тем не менее также оказалось значимым
(р =
0,0075). По
этой причине препарат
U
исключают
и анализ повторяют только для препарата
Т и стандартного препарата.
Анализ, проведенный без препарата u, свидетельствует о соответствии условиям как линейности регрессии, так и параллельности, что позволяет перейти к расчету активности. Используя формулы, приведенные в Разделе 3.2.5, получаем следующие результаты:
Общий угловой коэффициент:
b = 20-418 - 3995) = -58970
In4 х 10 х 2
Натуральный логарифм отношения активностей:
MT
567,9 - 580,4
2 х (-58,970)
0,1060
C
66830,6
66830,6 - 738,54 х 2,0282
= 1,0476
V
66830 6
(-58,970)2 х 2 х10
0 9609
Натуральный логарифм доверительных интервалов: 1,0476 х 0 11060 ±yj0,0476 х (1,0476 х 0,10602 + 2 х 0,9609) = 0,1110 ± 0,3034
Вычислив антилогарифм, мы найдем отношение активностей, равное 1,11, при 95% доверительном интервале от 0,82 до 1,51.
Умножение на предполагаемую активность препарата Т, дает рассчитанную активность 1,11 ЕД/мг при 95% доверительном интервале от 0,82 до 1,51 ЕД/мг.
5.1.2 ТРЕХДОЗОВОЕ КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ С ИСПОЛЬЗОВАНИЕМ СХЕМЫ ЛА ТИНСКИХ КВАДРА ТОВ.
Количественное определение антибиотика методом диффузии в агар, используя прямоугольный планшет.
Стандартный препарат имел установленную активность, равную 4855 МЕ/мг. Предполагаемая активность испытуемого препарата принималась равной 5600 МЕ/мг. Исходные растворы готовились следующим образом: 25,2 мг стандартного препарата растворяли в 24,5 мл растворителя и 21,4 мг испытуемого препарата растворяли в 23,95 мл растворителя. Для анализа исходные растворы сначала разводили в соотношении 1/20, а затем, используя степень разведения 1,5.
Латинские квадраты строились при помощи метода, описанного в Разделе 8.6 (см. Таблицу 5.1.2.-I). Результаты, полученные в ходе данного количественного определения, приведены в Таблице 5.1.2.-II (зоны ингибирования роста в мм х10). Средние значения для групп приведены в Таблице 5.1.2.-III. Графическое представление данных (см. Рисунок 5.1.2.-I) не дает поводов сомневаться в нормальности распределения и однородности дисперсий.
Используя формулы, приведенные в Таблицах 3.2.3.-I и 3.2.3.-II, получаем следующие результаты:
 Ps
=
529,667 Pt
=
526,333
Ps
=
529,667 Pt
=
526,333
Hp = 6 = 2
Далее проводят дисперсионный анализ по формулам, приведенным в Таблицах 3.2.3.-3 и 3.2.3.-4. Результаты приведены в Таблице 5.1.2.-4.
Анализ показывает значительные различия между строками. Это означает, что использование схемы Латинских квадратов обеспечивает в данном случае более высокую точность по сравнению со схемой полной рандомизации. Высокая значимость регрессии, а также отсутствие значимого отклонения индивидуальных линий регрессии от параллельности и линейности, подтверждают, что результаты количественного определения пригодны для расчета активности.
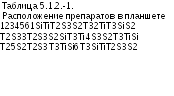
Таблица 5.i.2.-2.
i
2
3 4 5 6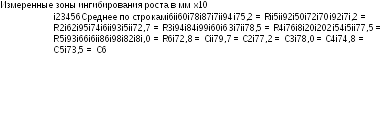
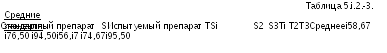

Общий угловой коэффициент:
b = 3 х (35,833 + 39,333) = 46346
In(1,5) х 6 х 2 Натуральный логарифм отношения активностей:
- 526,333 - 529,667
' 3 х 46,346
-0,023974
C = 84750417 - = 10108
8475,0417 - 20,7667 х 2,0862
![]()
Натуральный логарифм доверительных интервалов:
1 , 0108 х (-0,0240) ±yJ0,0108 х (-0,0240)2 + 2 х 0,2192 = -0,02423 ± 0,06878
Вычислив антилогарифм, мы найдем отношение активностей, равное 0,9763 при 95% доверительном интервале от 0,9112 до 1,0456.
Поскольку разведения, приготовленные исходя из предполагаемой активности, не были точно равноактивными, следует ввести поправочный коэффициент
4855 х 25 ,2/24,5 = 0 99799 5600 х 21,4/23,95
Перемножая данный коэффициент и предполагаемую активность препарата 5600 МЕ/мг, получаем рассчитанную активность 5456 МЕ/мг при 95% доверительном интервале от 5092 до 5843 МЕ/мг.
5.1.3 ЧЕТЫРЕХДОЗОВАЯ СХЕМА РАНДОМИЗИРОВАННЫХ БЛОКОВ Количественное определение антибиотика турбидиметрическим методом
Данное количественное определение проводят с целью установления активности антибиотика в международных единицах на флакон. Стандартный препарат имел установленную активность 670 МЕ/мг. Предполагаемая активность испытуемого препарата принималась равной 20 000 ЕД/флакон. Исходя из этих данных исходные растворы готовились следующим образом: 16,7 мг стандартного препарата растворяли в 25 мл растворителя, а содержимое одного флакона испытуемого препарата растворяли в 40 мл растворителя. Для анализа исходные растворы сначала разводили в соотношении i/40, а затем, используя степень разведения i,5. Пробирки размещали в водяной бане в соответствии со схемой рандомизированного блока (см. Раздел 8.5). Полученные результаты приведены в Таблице 5.1.3.-1.
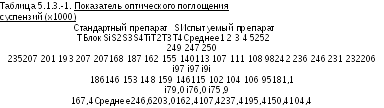
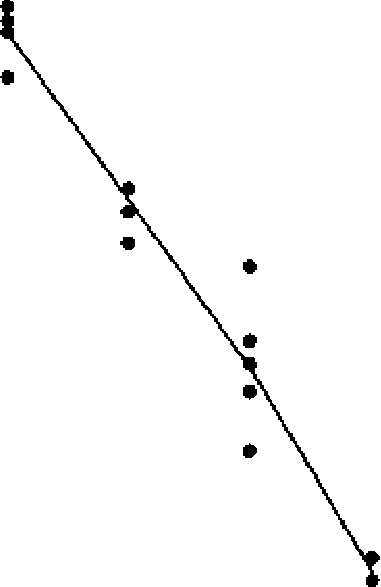
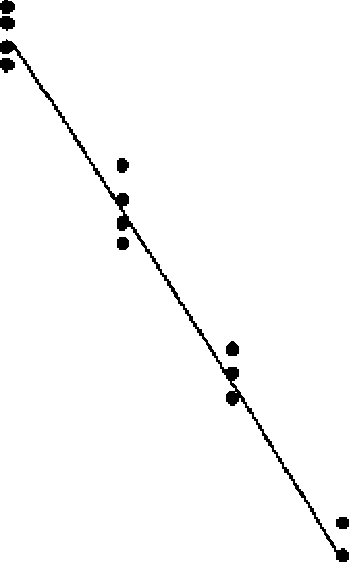
Анализ Рисунка 5.1.3.-1 не дает оснований сомневаться в справедливости предположения о нормальности распределения данных и однородности дисперсий. Стандартное отклонение S3 несколько велико, но не является причиной для беспокойства. Используя формулы, приведенные в Таблицах 3.2.3.-1 и 3.2.3.-2, получаем следующие результаты:
Ps = 719,4 Pt = 687,6
Hp = 5 = 1,25 4
Ls = -229,1 Lt = -222
HL = 60 = 1
Далее проводим дисперсионный анализ по формулам, приведенным в Таблицах 3.2.3.-3 и 3.2.3.-4. Полученные результаты приведены в Таблице 5.1.3.-2.
 275-
275-
250-
х225-
<и
&200-о>
|l75-о
о 150-
(D Q
П 125-<и
100-
О
75 -
S1
S2
S3
U1
U2
из
 50
50
Рисунок 5.1.3.-1.
Следует отметить значительное различие между блоками. Это означает, что применение схемы рандомизированных блоков позволяет добиться более высокой точности оценки. Высокая значимость регрессии, а также отсутствие значимого отклонения от параллельности и линейности подтверждают, что результаты количественного определения пригодны для расчета активности.
Используя формулы, приведенные в Разделе 3.2.5, получаем следующие результаты:
Общий угловой коэффициент:
и 1 х (-2291 - 222) „„„0<г<г
b = —- = -111,255
In(1,5) х 5 х 2
Натуральный логарифм отношения активностей:
„. 687,6 - 719,4
Mt = — = 0,071457
4 х ( -111,255 ) 101745 ,6
C = w = 1,00223
101745,6 - 53,916 х 2,0482
101745 6
V = ^ = 0,4110
(-111,255)2 х 4 х 5
Натуральный логарифм доверительных интервалов: 1,00223 х 0,0715 ± V0,00223 х 0,07152 + 2 х 0,4110 = 0,07162 ± 0,04293
Вычислив антилогарифм, мы найдем отношение активностей, равное 1,0741 при 95% доверительном интервале от 1,0291 до 1,1214.
Поскольку разведения, приготовленные исходя из предполагаемой активности, не были точно равноактивными, следует ввести поправочный коэффициент
670 х167 / 25 = 089512 20000 х1/40
Перемножая данный коэффициент и предполагаемую активность препарата 20000 МЕ/флакон, получаем рассчитанную активность 19228 МЕ/флакон при 95% доверительном интервале от 18423 до 20075 МЕ/флакон.
5.1.4 ПЯТИДОЗОВОЕ МНОГОКРА ТНОЕ КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ С ИСПОЛЬЗОВАНИЕМ СХЕМЫ ПОЛНОЙ РАНДОМИЗАЦИИ
Количественное определение in vitro активности трех вакцин против Гепатита В по сравнению со стандартным препаратом
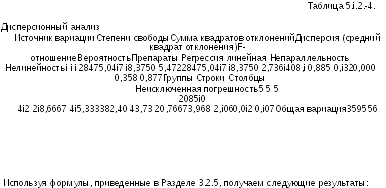
Для каждой из вакцин подготавливали по три независимые серии разведений, каждая из которых состоит из пяти двукратных разведений. После определенных подготовительных операций, предусмотренных процедурой количественного определения, измеряли оптические плотности растворов. Результаты приведены в Таблице 5.1.4.-1.
Испытуемый
препарат
T
0,097
0,157
0,355
0,665
1,386
0,345 0,576
1,051
|
Разведение |
Испытуемый препарат U |
Испытуемый препарат V | ||||
|
1:16 000 1:8000 1:4000 1:2000 1:1000 |
0,086 0,127 0,277 0,586 0,957 |
0,071 0,146 0,268 0,489 0,866 |
0,073 0,133 0,269 0,546 1,045 |
0,082 0,145 0,318 0,552 1,037 |
0,082 0,144 0,306 0,551 1,039 |
0,086 0,173 0,316 0,624 1,068 |
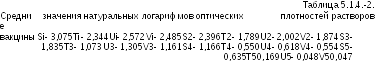
Как известно, натуральные логарифмы оптических плотностей раствора имеют линейную зависимость от логарифмов доз растворенного вещества. Средние результаты логарифмического преобразования оптических плотностей приведены в Таблице 5.1.4.-2. Графическое представление результатов не выявило каких-либо необычных закономерностей расположения данных.
0.5
0.0-


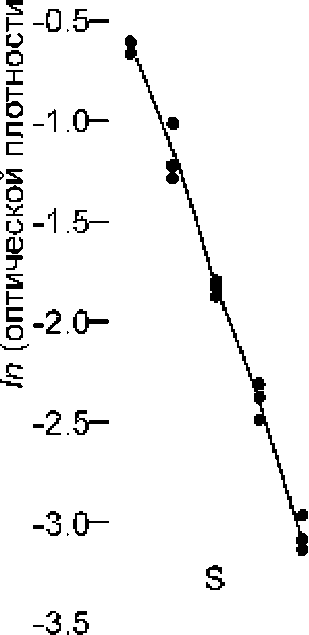
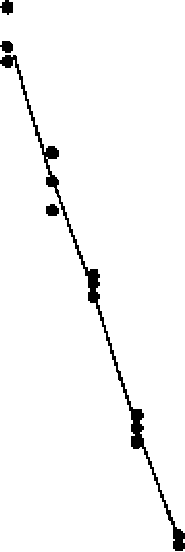
U V Рисунок 5.1.4.-1.
Используя формулы, приведенные в Таблицах 3.2.3.-1 и 3.2.3.-2, получаем следующие результаты:
Ps = -9,108 Ls = 6,109
Pt = -5,586 Lt = 6,264
Pu = -6,544 Lu = 6,431
Pv = -6,027 Lv = 6,384
Hp
= 3 =
5
0,6
36 120 0,3
 Далее
проводим дисперсионный анализ по
формулам, приведенным в Таблицах
3.2.3.-3 и 3.2.3.-4. Полученные результаты
приведены в Таблице 5.1.4.-3.
Далее
проводим дисперсионный анализ по
формулам, приведенным в Таблицах
3.2.3.-3 и 3.2.3.-4. Полученные результаты
приведены в Таблице 5.1.4.-3.
Высокая значимость регрессии, а также отсутствие значимого отклонения от параллельности и линейности подтверждают, что результаты данного количественного определения пригодны для расчета активности.
Используя формулы, приведенные в Разделе 3.2.5, получаем следующие результаты:
Общий угловой коэффициент:
b = 0,3 х (6109 + 6,264 + 6,431 + 6,384) = 0 90848 In2 х 3 х 4 ' Натуральный логарифм отношения активностей:
M = - 5,586 - (-9108) = 07752
' 5 х 0,90848
C = 4758 = 1,00057
47,58 - 0,0067 х 2,0212
V = 4758 = 3,8436
0,90852 х 5 х 3 Натуральный логарифм доверительных интервалов:
1,00057 х 0,7752 ±yj0,00057 х (1,00057 х 0,77522 + 2 х 3,8436) = 0,756 ± 0,0689
Вычислив антилогарифм, мы найдем отношение активностей вакцин, равное 2,171 при 95% доверительном интервале от 2,027 до 2,327.
Все образцы имеют установленную активность 20 мкг протеина/мл и, следовательно, найденная активность испытуемого препарата Т равна 43,4 мкг протеина/мл при 95% доверительном интервале от 40,5 до 46,5 мкг протеина/мл.
 Аналогичным
образом вычисляют активность и
доверительные интервалы для других
испытуемых препаратов. Полученные
результаты приведены в Таблице 5.1.4.-4.
Аналогичным
образом вычисляют активность и
доверительные интервалы для других
испытуемых препаратов. Полученные
результаты приведены в Таблице 5.1.4.-4.
Количественное определение активности инсулина путем подкожной инъекции у кроликов
Стандартный препарат вводился в дозах 1 и 2 ЕД/мл. Эквивалентные дозы испытуемого препарата назначались исходя из предполагаемой активности 40 ЕД/мл. Кроликам подкожно вводили 0,5 мл соответствующих растворов в соответствии со схемой, приведенной в Таблице 5.1.5.-1. полученные результаты приведены в таблице 5.1.5.-2. Высокое значение дисперсии свидетельствует о наличии статистически значимых различий между кроликами и необходимости использовать перекрестную схему исследования.
|
| ||
|
| ||
|
Группа кроликов |
|
|
|
1 |
2 3 |
4 |
|
День 1 S1 |
|
|
День
2
T2Ti
S2Si
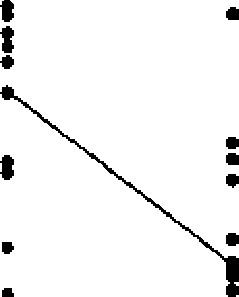
^80 -
и:
1б0 -40 -20 -
0
S1
S2
Т1 Т2 Рисунок 5.1.5.-1.
Для рассматриваемой схемы количественного определения применение дисперсионного анализа является более сложным, чем рассмотренных ранее схем, потому что компонента вариации, обусловленная параллельностью, не является независимой от компонента, обусловленного различием между кроликами. Поэтому проверка па-
раллельности линий регрессий дополнительно требует второй поправочный коэффициент для ошибки среднего квадрата отклонений (дисперсии), который вычисляется путем вычитания компонента параллельности и пар «взаимодействующих» компонентов из компонента, связанного с различием между кроликами.
За счет повторений в каждой из групп, в дисперсионном анализе присутствуют три пары «взаимодействующих» компонентов:
Дни х препарат; дни х регрессия; дни х параллельность.
Эти коэффициенты характеризуют тенденцию компонентов (препараты, регрессия и параллельность) изменяться в серии «изо дня в день». Таким образом, соответствующие F-отношения обеспечивают проверку этих компонентов оценки достоверности количественного определения. Если статистическая значимость полученных оценок F-отношений является высокой, следует с большой осторожностью интерпретировать результаты количественного определения и, если это возможно, следует повторить количественное определение активности инсулина.
Дисперсионный анализ проводится с использованием формул, приведенных в Таблицах 3.2.3.-1. - 3.2.3.-3., отдельно как для каждого дня, так и для объединенного набора данных. Используя формулы, приведенные в Таблицах 3.2.3.-1. и 3.2.3.-2, получаем следующие результаты:
День 1:
День 2:
Объединенные данные:
Ps Pt
165,25 162,25
Ps Pt
HP = 8 = 4 P 2
173,38
4
176,00
Hp 8
Ps = Pt =
Hp
2
196,31 169,13 16
8
2
Ls
:
Lt
=
Hl
96
Ls Lt
6
-20,06 -5,25
hl = 96
Ls Lt
L 6
-16,53 -7,00
L 6
16
16
32
Используя формулы, приведенные в Таблице 3.2.3.-3, получаем следующие результаты:
День 1 День 2 Объединенные данные
SSprep = 18,000 SSprep = 13,781 SSprep = 0,141
SSreg = 3784,5 SSreg = 5125,8 SSreg = 8859,5
SSpar = 144,5 SSpar = 1755,3 SSpar = 1453,5
Коэффициенты Объединенные данные».
SSdaysxprep — 31,64 SSdaysxreg — 50,77 SSdaysxpar — 446,27
взаимодействия
рассчитывают
как: «День1+День2-
Дополнительно, рассчитывают сумму квадратов отклонений вследствие вариации в серии «изо-дня-в-день»:
1
SSdays = 2N(°1 + D2) - K = 478,52
и сумму квадратов отклонений вследствие вариаций в блоках (различие между кроликами):
SSbi0Ck = 2У B2 - K = 397947
где Bj - среднее значение в пересчете на одного кролика.
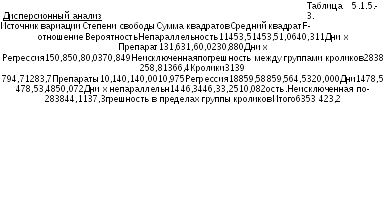 Далее
проводят дисперсионный анализ, результаты
которого приведены в Таблице 5.1.5.-3.
Далее
проводят дисперсионный анализ, результаты
которого приведены в Таблице 5.1.5.-3.
Дисперсионный анализ подтверждает, что полученные данные удовлетворяют необходимым условиям обоснованности оценки активности инсулина: высокая статистическая значимость линейной регрессии, отсутствие статистически значимых отклонений от параллельности и незначимые все три коэффициента взаимодействия.
Используя формулы, приведенные в Разделе 3.2.5, получаем следующие результаты:
Общий угловой коэффициент: b = 32 х (-16,53 - 7) = -зз95
In2 х 16 х 2
Натуральный логарифм отношения активностей:
Ыт = 16913 -169,31 = 000276
' 2 х (-33,95)
C = 88595 - = 10695
8859,5 -137,3х 2,0482
V = 88595 = 0,2402
(-33,95)2 х 2 х16
Натуральный логарифм доверительного интервала:
1,0695 х 0,00276 + 70,0695 х (1,0695 х 0,002762 + 2 х 0,2402) = 0,00295 ± 0,18279
Вычислив антилогарифм, мы найдем отношение активностей, равное 1,003 при 95% доверительном интервале от 0,835 до 1,204.
Умножив на AT = 40, получим активность 40,1 единиц на миллилитр при 95% доверительном интервале от 33,4 до 48,2 единиц на миллилитр.

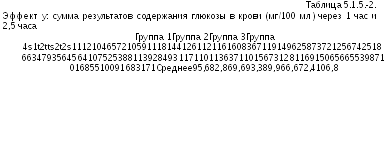 Планирование
исследования
Планирование
исследования