
- •Государственная фармакопея республики беларусь первое издание
- •Республики Беларусь
- •1. Общие сведения
- •1.1. Общие положения
- •1.2. Другие положения, распространяющиеся на общие и частные фармакопейные статьи
- •Условия хранения лекарственного средства
- •Пределы, указываемые на упаковке
- •1.5. Сокращения и обозначения
- •1.6. Единицы международной системы (си), используемые в фармакопейных статьях, и их соответствие другим единицам
- •2. Методы анализа
- •2.1. Оборудование
- •2.1.1. Каплемер
- •2.1.2. Сравнительная таблица пористости стеклянных фильтров
- •Пористость фильтра (ф.Евр.) (1)
- •Максимальный диаметр пор в микрометрах
- •2.1.3. Лампы с ультрафиолетовым излучением для аналитических целей
- •2.1.4. Сита
- •2.2. Физические и физико-химические методы
- •2.2.1. Определение прозрачности и степени мутности жидкостей
- •2.2.2. Определение степени окрашивания жидкостей
- •2.2.3. Потенциометрическое определение рН
- •2.2.4. Зависимость между реакцией раствора, приблизительным значением рН и цветом индикаторов
- •Изменение цвета
- •2.2.5. Относительная плотность
- •2.2.6. Показатель преломления (индекс рефракции)
- •2.2.7. Оптическое вращение
- •2.2.8. Вязкость
- •1/Прив 1
- •2.2.9. Метод капиллярной вискозиметрии
- •2.2.10. Метод ротационной вискозиметрии
- •2.2.11. Температурные пределы перегонки
- •2.2.14. Температура плавления - капиллярный метод
- •2.2.17. Температура каплепадения
- •2.2.18. Температура затвердевания
- •2.2.21. Флуориметрия
- •2.2.22. Атомно-эмиссионная спектрометрия
- •2.2.23. Атомно-абсорбционная спектрометрия
- •2.2.24. Абсорбционная спектрофотометрия в инфракрасной
- •2.2.25. Абсорбционная спектрофотометрия в ультрафиолетовой видимой областях
- •2. Многокомпонентный спектрофотометрический анализ.
- •2.2.26. Бумажная хроматография
- •2.2.27. Тонкослойная хроматография
- •2.2.28. Газовая хроматография
- •2.2.29. Жидкостная хроматография
- •2.2.30. Эксклюзионная хроматография
- •2.2.31. Электрофорез
- •2.2.32. Потеря в массе при высушивании
- •2.2.33. Спектрометрия ядерного магнитного резонанса
- •2.2.34. Термогравиметрия
- •2.2.35. Осмоляльность
- •2.2.36. Потенциометрическое определение концентрации ионов с использованием ионселективных электродов
- •2.2.37. Рентгенофлуоресцентная спектрометрия
- •2.2.38. Удельная электропроводность
- •2.2.39. Молекулярно-массовое распределение декстранов
- •2.2.40. Спектрофотометрия ближнего ик-диапазона
- •2.2.41. Круговой дихроизм
- •2.2.42. Плотность твердых тел
- •2.2.43. Масс-спектрометрия
- •2.2.44. Определение содержания общего органического углерода в воде для фармацевтического применения
- •2.2.45. Сверхкритическая флюидная хроматография
- •2.2.46. Хроматографические методы разделения
- •2.2.47. Капиллярный электрофорез
- •2.2.48. Рамановская спектрометрия (# спектрометрия комбинационного рассеяния)
- •2.2.54. Изоэлектрическое фокусирование
- •2.3.1. Реакции подлинности (идентификации) на ионы и функциональные группы
- •2.3.2. Идентификация жирных масел методом тонкослойной хроматографии
- •2.3.3. Идентификация фенотиазинов методом тонкослойной хроматографии
- •2.3.4. Определение запаха
- •2.4. Испытания на предельное содержание примесей
- •2.4.1. Аммония соли
- •2.4.2. Мышьяк
- •2.4.3. Кальций
- •2.4.6. Магний
- •2.4.7. Магний и щелочноземельные металлы
- •2.4.8. Тяжелые металлы
- •2.4.15. Никель в полиолах
- •2.4.1.6. Общая зола
- •2.4.21. Посторонние масла в жирных маслах методом тонкослойной хроматографии
- •2.4.22. Посторонние жирные кислоты в маслах методом газовой хроматографии
- •2.4.23. Стерины в жирных маслах
- •2.4.24. Идентификация остаточных растворителей и их количественное определение
- •2.4.25. Остаточные количества этиленоксида и диоксана
- •2.4.27. Никель в гидрогенизированных растительных маслах
- •2.5. Методы количественного определения 2.5.1. Кислотное число
- •2.5.3. Гидроксильное число
- •2.5.4. Йодное число
- •2.5.5. Перекисное (пероксидное) число
- •2.5.6. Число омыления
- •2.5.7. Неомыляемые вещества
- •2.5.8. Определение аминного азота в соединениях, которые содержат первичную ароматическую аминогруппу
- •2.5.9. Определение азота после минерализации серной кислотой
- •2.5.10. Метод сжигания в колбе с кислородом
- •2.5.11. Комплексометрическое титрование
- •2.5.12. Вода: полумикрометод (#Метод к.Фишера)
- •2.5.13. Алюминий в адсорбированных вакцинах
- •2.5.14. Кальций в адсорбированных вакцинах
- •2.5.20. Гексозамины в полисахаридных вакцинах
- •2.5.21. Метилпентозы в полисахаридных вакцинах
- •2.5.24. Диоксид углерода в газах
- •2.5.25. Оксид углерода в газах
- •2.5.26. Оксид азота и диоксид азота в газах
- •2.5.27. Кислород в газах
- •2.5.30. Окисляющие вещества
- •2.5.33. Общий белок
- •2.5.34. Уксусная кислота в синтетических пептидах
- •2.6. Биологические испытания
- •2.6.1. Стерильность
- •2.6.2. Микобактерии
- •2.6.3. Испытания на посторонние вирусы с использованием куриных эмбрионов
- •2.6.4. Испытание на вирусы лейкоза
- •2.6.5. Испытание на посторонние вирусы с использованием клеточных культур
- •2.6.6. Испытание на посторонние агенты с использованием цыплят.
- •2.6.7. Микоплазмы
- •2.6.8 Пирогенность
- •2.6.9. Аномальная токсичность
- •2.6.10. Гистамин
- •2.6.11. Депрессорные вещества
- •2.6.12. Микробиологические испытания нестерильной продукции (суммарное количество жизнеспособных аэробов)
- •2.6.13. Микробилогические испытания нестерильной продукции (испытания на наличие специфических микроорганизмов)
- •0,9 % Раствор натрия хлорида
- •1 % Раствор фенолового красного
- •0,5 % Раствор малахитового зеленого
- •2.6.14. Бактериальные эндотоксины
- •1. Предварительные испытания
- •2. Предельное испытание (метод а) (I) Методика
- •2. Полуколичественное испытание (метод в)
- •1. Турбидиметрический принцип (методы с и f)
- •2.6.15. Активатор прекалликреина
- •2.6.16. Испытания на посторонние агенты в вирусных вакцинах для медицинского применения
- •2.6.17. Испытание на антикомплементарную активность иммуноглобулина
- •2.6.18. Испытание живых вирусных вакцин на нейровирулентность
- •2.6.19. Испытание пероральной вакцины полиомиелита на нейровирулентность
- •5.1. Предотвращение загрязнения
- •5.4 Детектирование
- •7.1 Валидация системы для количественного определения методом
- •7.2. Контроль качества реагентов.
- •7.3. Контроль хода испытания.
- •7.4. Внешняя оценка качества
- •2.6.22. Активированные факторы свертывания крови
- •2.7 Биологические методы количественного определения
- •2.7.1. Иммунохимические методы
- •2.7.2. Количественное определение антибиотиков микробиологическим методом
- •2.7.3. Количественное определение кортикотропина
- •2.7.4. Количественное определение фактора свертывания крови VIII
- •2.7.5. Количественное определение гепарина
- •2.7.6. Количественное определение вакцины дифтерии (адсорбированной)
- •2.7.7. Количественное определение вакцины коклюша
- •2.7.8. Количественное определение вакцины столбняка (адсорбированной)
- •2.7.9. Определение функционального состояния Fc-фрагмента иммуноглобулина
- •2.7.10. Количественное определение фактора свертывания крови человека VII
- •2.7.11. Количественное определение фактора свертывания крови человека IX
- •2.7.12. Количественное определение гепарина в концентратах
- •2.7.13. Количественное определение человеческого анти-d-иммуноглобулина
- •2.7.14. Количественное определение антигенной (иммуногенной) активности вакцины гепатита а
- •2.7.15. Количественное определение вакцины гепатита в (rdna)
- •2.7.16. Количественное определение вакцины коклюша (бесклеточной)
- •2.7.17. Количественное определение антитромбина III человека
- •2.7.18. Количественное определение фактора свертывания крови II
- •2.7.19. Количественное определение фактора свертывания крови х
- •2.7.20. Количественное определение инактивированной вакцины полиомиелита in vivo
- •2.7.22. Количественное определение фактора свертывания крови человека XI
- •2.8. Методы анализа лекарственного растительного сырья и лекарственных средств из него
- •2.8.1. Зола, нерастворимая в хлористоводородной кислоте
- •2.8.4. Коэффициент набухания
- •2.8.5. Определение воды в эфирных маслах
- •2.8.10. Растворимость эфирных масел в спирте
- •2.8.11. Определение 1,8-цинеола в эфирных маслах
- •2.8.12. Определение эфирного масла
- •2.8.13. Остаточное количество пестицидов
- •1. Экстракция
- •2. Очистка
- •3. Количественный анализ
- •Относительные времена удерживания инсектицидов
- •2.8.15. Определение показателя горечи
- •2.8.16. Сухой остаток экстрактов
- •2.8.17. Потеря в массе при высушивании экстракта
- •2.9. Фармацевтико-технологические испытания
- •2.9.1. Распадаемость таблеток и капсул
- •2.9.2. Распадаемость суппозиториев и пессариев
- •2.9.3. Тест «растворение» для твердых дозированных форм
- •2.9.4. Тест «растворение» для трансдермальных пластырей
- •2.9.5. Однородность массы для единицы дозированного лекарственного средства
- •2.9.6. Однородность содержания действующего вещества в
- •2.9.7. Прочность таблеток без оболочки на истирание
- •2.9.8. Прочность таблеток на сжатие
- •2.9.9. Измерение консистенции методом пенетрометрии
- •2.9.10 Содержание этанола
- •2.9.11. Испытание на содержание метанола и 2-пропанола
- •2.9.12. Ситовой анализ
- •2.9.15. Насыпной объем
- •2.9.16. Сыпучесть
- •2.9.17. Определение извлекаемого объема парентеральных лекарственных средств
- •Масса действующего вещества высвобожденного при опорожнении
- •Фракция действующего вещества (%)
- •2.9.19. Загрязнение механическими включениями: невидимые частицы.
- •2.9.20. Загрязнение механическими включениями: видимые частицы
- •2.9.21. Загрязнение механическими включениями: метод микроскопии
- •2.9.22. Опредление времени деформации липофильных суппозиториев
- •2.9.23. Определение плотности твердых частиц при помощи пикнометра
- •2.9.24. Устойчивость суппозиториев и пессариев к разрушению
- •2.9.26. Опредедение удельной площади поверхности методом газовой адсорбции
- •III.1.3. Количество образца
- •III.2.1. Метод 1: метод динамического потока
- •III.2.2. Метод 2: метод объёмного анализа
- •2.9.27. Однородность массы одной дозы высвобожденной из многодозового контейнера
- •2.9.28. Определение массы или объема содержимого контейнера для жидких и мягких лекарственных средств
- •3.1. Материалы, используемые для производства контейнеров
- •3.1.1. Материалы, используемые для производства контейнеров для человеческой крови и компонентов
- •3.1.1.1. Материалы на основе пластифицированного поливинилхлорида, используемые для производства
- •3.1.1.2. Материалы на основе пластифицированного поливинилхлорида для трубок, используемых в комплектах для переливания крови и компонентов крови
- •3.1.3. Полиолефины
- •3.1.4. Полиэтилен без добавок для контейнеров для парентеральных и офтальмологических лекарственных средств
- •3.1.5. Полиэтилен с добавками для контейнеров для
- •3.1.6. Полипропилен для контейнеров и укупорочных материалов для парентеральных и офтальмологических лекарственных средств
- •3.1.7. Полиэтиленвинилацетат для контейнеров и трубок для лекарственных средств для парентерального питания
- •3.1.8. Силиконовое масло, используемое в качестве смазывающей добавки
- •3.1.9. Силиконовые эластомеры для укупорочных
- •3.1.10. Материалы на основе непластифицированного поливинилхлорида для контейнеров для неинъекционных водных растворов
- •3.1.11. Материалы на основе непластифицированного поливинилхлорида для контейнеров для твердых лекарственных форм для перорального применения
- •3.1.13. Добавки к пластмассе
- •3.1.14. Материалы на основе пластифицированного поливинилхлорида для контейнеров для водных растворов для внутривенного применения
- •3.1.15. Полиэтилентерефталат для контейнеров для лекарственных средств для непарентерального применения
- •3.2. Контейнеры
- •3.2.1. Стеклянные контейнеры для фармацевтического использования
- •3.2.2. Пластмассовые контейнеры и укупорочные средства для фармацевтического использования
- •3.2.2.1. Пластмассовые контейнеры для водных растворов для парентерального применения
- •3.2.3. Стерильные пластмассовые контейнеры для человеческой крови и ее компонентов
- •3.2.4. Пустые стерильные контейнеры из пластифицированного поливинилхлорида для человеческой крови и ее компонентов
- •3.2.5. Стерильные контейнеры из пластифицированного поливинилхлорида для человеческой крови, содержащие раствор антикоагулянта
- •3.2.6. Комплекты для переливания крови и компонентов крови
- •3.2.8. Стерильные одноразовые пластмассовые шприцы
- •3.2.9. Резиновые укупорочные средства для контейнеров, предназначенных для водных лекарственных средств для парентерального применения, порошков и лиофилизированных порошков
- •4. Реактивы
- •4.1. Реактивы, эталонные растворы, буферные растворы
- •4.1.1. Реактивы
- •4.1.2. Эталонные растворы для испытаний на предельное содержание примесей
- •0,1 М фосфатный буферный раствор рН 8,0. 4008400.
- •4.2. Реактивы, титрованные растворы для объемного нализа
- •1 М щелочной раствор меди-этилендиамина. 3008700
- •5.1 Общие тексты по стерилизации
- •5.1.1. Методы приготовления стерильных продуктов
- •5.1.2. Биологические индикаторы стерилизации
- •5.1.3. Эффективность антимикробных консервантов
- •24 Часа
- •5.1.4. Микробиологическая чистота лекарственных средств
- •5.1.5 .Применение f0 концепции при стерилизации паром водных растворов.
- •5.2. Общая информация о вакцинах
- •5.2.1. Общепринятая терминология
- •5.2.2. Стаи кур, не имеющих конкретных патогенов и используемые для производства вакцин и контроля их качества
- •5.2.3. Субстраты клеток для производства вакцин, используемых людьми
- •5.2.6. Оценка безопасности вакцин
- •5.2.7. Оценка эффективности вакцин
- •5.2.8. Снижение риска передачи возбудителей губчатой энцефалопатии через лекарственные средства
- •1. Общие замечания
- •2. Область применения общей главы
- •3.1. Животные как источник материала
- •3.2. Части тел животных, жидкости и выделения в качестве исходных материалов
- •3.3. Проверка процесса
- •5.3. Статистические методы обработки результатов анализа
- •5.3.1. Статистический анализ результатов биологических исследований и количественных определений
- •1.1. Общие положения и точность
- •2. Рандомизация и независимость конкретных исследований
- •3. Количественные определения, основанные на количественных эффектах
- •3.1. Статистические модели
- •3.2. Модель параллельных линий
- •3.2.2.1 Схема полной рандомизации
- •3.2.2.2 Схема рандомизированных блоков
- •3.3. Модель угловых коэффициентов
- •3.3.5.2 (/7С/)-схема
- •4. Тесты с альтернативным типом эффекта 4.1. Введение
- •4.2. Метод пробит-анализа
- •5.1. Модель параллельных линий.
- •5.2. Модель угловых коэффициентов
- •5.3. Альтернативные эффекты
- •6 Объединение результатов количественного определения 6.1. Введение
- •6.2. Взвешенное объединение результатов количественного определения
- •6.3. Невзвешенное объединение результатов количественного опре- деления
- •6.4. Пример определения взешенной средней активности с доверительн1м интервалом
- •7. Дополнение
- •7.1. Общие линейные модели
- •7.4. Ошибки корреляции
- •8. Таблицы и процедуры генерирования
- •8.5. Случайные размещения
- •8.6. Латинские квадраты
- •9. Принятые обозначения
- •1. Выборка
- •1.1. Среднее зна чение и дисперсия
- •1.3. Доверительные интервалы и оценка их величины.
- •1.4. Односторонние и двусторонние доверительные интервалы.
- •2. Метрологические характеристики методики анализа
- •2.1.1. Объединенная дисперсия и объединенное среднее
- •2.1.2. Критерий Бартлетта.
- •2.1.3. Критерий Кохрейна.
- •2.2. Проверка наличия значимой систематической погрешности.
- •3. Сравнение двух методик анализа по воспроизводимости
- •4. Метрологическая характеристика среднего результата.
- •5. Сравнение средних результатов двух выборок
- •5.3. Известно точное значение величины а.
- •6. Интерпретация результатов анализа, полученных с помощью метрологически аттестованной методики.
- •6.1. Оценка сходимости результатов параллельных определений.
- •6.2. Определение необходимого числа параллельных определений.
- •6.3. Гарантия качества продукции.
- •7. Расчет и статистическая оценка параметров линейной зависимости
- •8. Последовательная схема статистического анализа результатов химических измерений
- •9. Примеры
- •9.1 Вычисление среднего значения и дисперсии.
- •9.2 Проверка однородности выборки малого объема
- •9.3. Вычисление доверительных интервалов и неопределенностей измерений.
- •9.4. Проверка гипотезы равенства дисперсий.
- •9.4.1. Объединение результатов выборок разного объема.
- •9.4.2. Объединение результатов выборок одинакового объема.
- •9.5. Сравнение двух методик анализа по воспроизводимости.
- •9.6. Сравнение средних результатов двух выборок.
- •9.7. Оценка качества продукции.
- •9.8. Контроль содержания салициловой кислоты в салициловом спирте посредством секвенционального анализа.
- •10. Расчет неопределенности функции нескольких случайных переменных
- •10.1. Линейная модель
- •10.1.1. Взвешенное среднее
- •10.2. Подход Уэлча-Сатертуэйта
- •10.3. Примеры расчетов неопределенности функции нескольких переменных
- •10.3.1. Расчет неопределенности вэжх-анализа готового лекарственного средства
- •10.3.1.1. Конечная аналитическая операция
- •10.3.1.2. Суммарная неопределенность пробоподготовки asp,r.
- •10.3.1.3. Расчет суммарной неопределенности анализа aAs,r
- •10.3.2. Прогноз неопределенности спектрофотометрического анализа готового лекарственного средства
- •10.3.3. Расчет среднего значения нескольких неравноточных выборок
- •1. Введение
- •2. Аналитические испытания и методики, подлежащие валидации
- •3. Валидационные характеристики и требования
- •4. Словарь
- •2. Специфичность
- •5. Правильность
- •5.1. Количественное определение
- •5.2. Примеси (количественное содержание).
- •7. Предел обнаружения
- •8. Предел количественного определения
- •8.3. Использование калибровочной прямой и стандартного отклонения сигнала
- •9. Робастность
- •10. Проверка пригодности хроматографической системы
- •3. Неинструментальные испытания на чистоту и предельное содержание примесей
- •5. Разделительные методы
- •6.1. Метод добавок
- •6.2. Сравнение с арбитражным методом
- •5.4. Остаточные количества органических растворителей
- •5.4.1. Введение
- •5.4.2. Область применения
- •5.4.3. Общие положения
- •5.4.4. Предельные содержания остаточных растворителей
- •5.5. Алкоголеметрические таблицы
- •5.6. Отчет об исследовании интерферонов
- •3.3. Процедура исследования
- •3.3.1. Определение уровня доза-ответ
- •5.7. Таблица физических упоминаемых в фармакопеи
- •Вероятность эмиссии
- •Энергия (мЭв)
- •Энергия (мЭв)
- •Вероят ность эмиссии (на
- •Энергия (мЭв)
- •Вероятность эмиссии
- •5.8. Биодоступность и биоэквивалентность генерических лекарственных средств
- •3. Регистрационная оценка взаимозаменяемых лекарственных
- •4. Исследования эквивалентности, необходимые для
- •4.2.1. Исследования биоэквивалентности/биодоступности (исследования на человеке)
- •4.2.2. Общие методические подходы к выполнению исследований биоэк- вивалентности/биодоступности
- •4.2.3. Исследования сравнительной кинетики растворения (исследования вне живого организма)
- •4.3. Отсутствие необходимости в исследованиях биоэквивалентности или биодоступности
- •5. Дизайн и проведение исследований биологической эквивалентности и биодоступности на людях 5.1. Общие требования.
- •5.2. Испытуемые
- •6. Регламент фармакокинетического исследования
- •7. Аналитический метод
- •8. Анализ фармакокинетических данных
- •8.1. Параметры, подлежащие оценке
- •8.1.1. Однократное введение лекарственного средства
- •8.1.2. Многократное введение лекарственного средства
- •9. Исключение резко выделяющихся наблюдений
- •12. Фармакодинамические исследования
- •13. Клинические испытания
- •14. Тест сравнительной кинетики растворения in vitro
- •15. Клинически значимые колебания биодоступности, обуславливающие отказ в регистрации лекарственного средства
- •Лабораторных животных
- •Участие в испытаниях биоэквивалентности/биодоступности
- •Номограмма для определения достаточного числа добровольцев по результатам проведенного исследования.
- •Хорошо растворимые лекарственные средства
- •Средства с высокой степенью абсорбции
- •Перечень терапевтических (лечебных) доз средств на основе лекарственного растительного сырья
- •Основная литература
- •6. Общие статьи на лекарственные формы и субстанции
3. Неинструментальные испытания на чистоту и предельное содержание примесей
3.1. Внешний вид раствора (2.2.1 и 2.2.2). Это визуальные испытания, предназначенные для оценки общей чистоты субстанции и основанные на сравнении окраски (или опалесценции) испытуемого раствора и серии эталонов. Часто неизвестно, какие примеси и в какой концентрации обуславливают окраску или опалесценцию. В этом случае валидация основывается на сопоставлении данных, полученных для разных серий, представленных производителем (или производителями). Если примеси известны и доступны, валидацию этого метода проводят путем сравнения с более совершенным методом.
3.2. Кислотность и щелочность. Это неспецифичное испытание является одной из характеристик чистоты образца и используется для контроля протеолити-ческих примесей.
3.2.1. Выбор показателя «рН» или «Кислотность/щелочность» для контроля качества субстанций. Для контроля протолитических примесей в субстанциях используют два испытания:
полуколичественное титрование с использованием индикатора или потенцио-метрического определения точки титрования - испытание «Кислотность/щелочность»;
измерение рН.
Если вещество имеет буферную емкость, преимущественным является измерение рН. В обратном случае рекомендуется титриметрическая методика. Испытание «Кислотность/щелочность» применяют тогда, если испытуемая субстанция не гидролизуется или нерастворима в воде.
Вопрос выбора испытания «Кислотность/щелочность» или «рН» при разработке аналитической нормативной документации или монографии на субстанцию может быть определен на подступе оценки буферных емкостей самой субстанции.
Для оценки буферных емкостей субстанции строят кривую потенциометри-ческого титрования водного раствора (или, в случае нерастворимых в воде веществ, - экстракта (водной вытяжки)) необходимой концентрации (от 10 г/л до 50 г/л), используя в качестве титранта 0,01 М раствор кислоты хлористоводородной или 0,01М раствор натрия гидроксида, соответственно. Точка изгиба на кривой титрования является настоящим рН раствора и для чистой субстанции находится на изгибе с пределом рН. Ступеней буферной емкости испытуемого раствора является величина суммарного сдвига рН (АрН), рассчитанная из кривой титрования в результате прибавления к 10 мл испытуемого раствора 0,25 мл 0,01 М раствора натрия гидроксида, а затем к другим 10 мл этого же раствора - 0,25 мл 0,01 М раствора кислоты хлористоводородной. Чем больше величина АрН, тем меньше буферная емкость раствора.
Величина АрН испытуемого раствора определяет выбор метода для регламентации протолитических примесей в соответствии с приведенной схемой (Табл.2). Классификация субстанций базируется на том, что для большинства индикаторов переход окраски происходит в пределах 2 единиц рН.
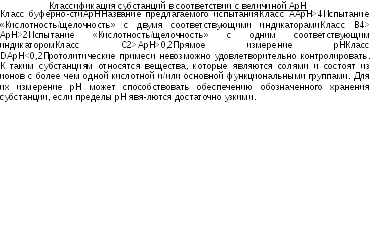 Путем
изменения концентрации испытуемого
раствора можно изменить класс буферности,
к которому попадает испытуемая субстанция
и в соответствии со схемой, приведенной
в Таблице 2. При этом будет изменяться
и форма кривой титрования. При этом,
если возможно, не следует выходить за
пределы обозначенных выше концентраций.
Однако, если вещество очень мало
растворимо в воде, можно использовать
раствор с концентрацией меньше 10-50 г/л.
Путем
изменения концентрации испытуемого
раствора можно изменить класс буферности,
к которому попадает испытуемая субстанция
и в соответствии со схемой, приведенной
в Таблице 2. При этом будет изменяться
и форма кривой титрования. При этом,
если возможно, не следует выходить за
пределы обозначенных выше концентраций.
Однако, если вещество очень мало
растворимо в воде, можно использовать
раствор с концентрацией меньше 10-50 г/л.
В некоторых случаях испытание «Кислотность/щелочность» нельзя провести при помощи индикатора или через окрашивание самого индикатора, или через разложение самого вещества. В таком случае испытание проводят при помощи потенциометрического титрования. Если прибавление кислоты или щелочи вызывает равновесие молекулы субстанции, или выпадения осадка, следует, не обращая внимания на буферную емкость, отказаться от проведения испытания «Кислотность/щелочность» на предмет измерения рН.
Растворы готовят с использованием воды, свободной от углерода диоксида, Р.
3.3. Испытания на предельное содержание анионов и катионов (2.4.) Пригодность этих испытаний следует доказать путем использования метода добавок и/или сравнения с другими, более совершенными методами.
Сульфатная зола (2.4.14). Это испытание предназначено для определения суммы катионов металлов, присутствующих в органических субстанциях, но не подходит для неорганических солей органических соединений. Обычно предел не должен превышать 0.1%. Этот метод не требует валидации.
Тяжелые металлы (2.4.8). Применяют различные способы проведения этого испытания. Обычно предел содержания тяжелых металлов составляет 0,001%
(10 ррт) или 0,002% (20 ррт), но иногда и 0,0005% (5 ррт), что находится вблизи предела обнаружения.
Для валидации испытания на тяжелые металлы анализируют испытуемый образец и образец, специально загрязненный свинцом в соответствующей концентрации. Окраска испытуемого образца должна быть меньше, а загрязненного образца - равной или большей, чем окраска эталона.
Для ряда методик, требующих сжигания образца, существует опасность потерь некоторых тяжелых металлов (таких как, например, ртуть и свинец в присутствии хлоридов). В таких случаях, когда это в возможно, контролируют содержание тяжелых металлов методом атомно-абсорбционной спектрометрии или другим инструментальным методом.
Если известно, что при синтезе субстанции используется катализатор, например, палладий, никель или родий, то их содержание целесообразно контролировать колориметрическими или инструментальными методами (например, атомно-абсорбционная спектрометрия и др.).
Цветные реакции или реакции осаждения. Для отдельных катионов и анионов описаны предельные испытания, основанные на визуальном сравнении окраски или опалесценции. При этом необходимо доказать, что:
—окраска или опалесценция для нормируемых концентраций отчетливо видны;
—найденная концентрация добавленного иона одинакова как для испытуемого раствора, так и для раствора сравнения (как визуально, так и с помощью методов, основанных на измерении поглощения);
—значения оптической плотности растворов, содержащих 50%, 100% и 150% анализируемой примеси от нормируемой концентрации, должны значимо различаться;
—определение примеси на уровне нормируемой концентрации проводят не менее шести раз и вычисляют стандартное отклонение. Найденная концентрация должна составлять не менее 80% от введенной, а относительное стандартное отклонение - не более 20%.
Целесообразно провести сравнение результатов предельного испытания с результатами количественного определения с использованием независимого метода, например, атомно-абсорбционной спектрофотометрии для катионов или ионной хроматографии для анионов. Результаты, полученные двумя методами, должны быть близки.
4. Атомно-абсорбционная спектрометрия (2.2.23)
Метод атомно-абсорбционной спектрометрии (ААС) применяют для испытаний по определению содержания отдельных элементов, присутствующих в образце.
4.1. Специфичность. Специфичность данного метода определяется тем, что атомы анализируемого элемента поглощают характеристическое излучение от источника со строго дискретными длинами волн, соответствующими данному элементу. Однако возможны помехи вследствие как оптических, так и химических эффектов. Перед началом валидации необходимо выявить помехи такого рода и, если возможно, снизить их влияние путем использования соответствующих приемов.
Эти помехи могут привести к систематической погрешности при использовании метода прямой калибровки или к изменению чувствительности метода. Основным источником погрешности в методе ААС являются погрешности, связанные с процессом калибровки и мешающим влиянием матрицы.
Градуировка. Использование линейной модели градуировки описано в общей статье 2.2.23 «Атомно-абсорбционная спектрометрия». Для доказательства применимости линейной регрессионной модели рекомендуется использовать не менее пяти градуировочных растворов. В некоторых случаях возможно использование параболической модели градуировки. При этом также используют не менее пяти градуировочных растворов. Рекомендуется использовать концентрации градуировочных растворов с равномерным распределением внутри диапазона применения.
Для каждой концентрации рекомендуется выполнять не менее пяти измерений.
Проблемы с калибровкой часто могут быть выявлены визуально. Однако градуировочные графики сами по себе нельзя использовать как доказательство пригодности метода калибровки. Калибровочный график представляют в следующем виде:
а) на графике откладывают измеренные оптические плотности как функции концентраций и строят кривую, описывающую эту градуировочную функцию, вме- сте с ее доверительными интервалами. Экспериментальные точки должны нахо- диться в пределах доверительного интервала построенного графика.
б) на графике откладывают остаточные отклонения (разности между измерен- ными и вычисленными по градуировочному графику оптическими плотностями) как функции концентрации. Эти разности должны распределяться вокруг оси абсцисс случайным образом.
В некоторых случаях разброс значений сигнала возрастает с ростом концентрации, что может быть выявлено из графика остаточных отклонений или статистическими методами. При этом наибольшая точность может быть достигнута при использовании градуировки с весовыми множителями. Может быть применена как линейная, так и квадратичная весовая функция.
В случае использования весовой модели строится график взвешенных разностей (т.е. разностей, умноженных на веса) как функции концентрации следующим образом:
а) на графике откладывают измеренные оптические плотности как взвешен- ные функции концентраций и строят кривую, описывающую эту градуировочную функцию вместе с ее доверительными интервалами.
б) на графике откладывают взвешенные остаточные отклонения (т.е. взве- шенные разности между измеренными и вычисленными по градуировочному графику оптическими плотностями) как функции концентрации.
Необходимо показать, что модель достаточно точно описывает экспериментальные данные.
Эффекты матрицы. Если для получения градуировочной функции используют метод градуировочного графика, то необходимо показать, что чувствительность для раствора анализируемого образца и градуировочных растворов одинакова.
Если применяется градуировка в виде прямой линии, различия в чувствительности могут быть обнаружены путем сравнения наклонов градуировочного графика, полученного с использованием эталонных растворов, и растворов, полученных внесением стандартной добавки к испытуемому раствору. Точность оценки наклонов обеих прямых зависит от числа и распределения точек измерения. Поэтому для построения обоих регрессионных линий рекомендуется использовать достаточное число точек (не менее пяти) и выбирать концентрации преимущественно на границах диапазона градуировки.
Обоснованием для возможности использования метода градуировочного графика является незначимость различий наклонов полученных прямых по критерию Стьюдента. Если различия значимы, то используют метод стандартных добавок.
4.4. Предел обнаружения и предел количественного определения (метод, основанный на стандартном отклонении контрольного опыта - см. 7.3.1 и 8.3.1, раздел В). Выполняют контрольные опыты, для которых предпочтительно использовать растворы «плацебо», содержащие все компоненты образца, за исключением определяемого. Если такие контрольные опыты выполнить невозможно, то допустимо использовать холостые растворы, содержащие все реагенты и приготовленные так же, как и испытуемый раствор.
