
- •Майкл Ферранте
- •Майкл
- •ЗНАЧИМОСТЬ ПРОБЛЕМЫ ПОСЛЕОПЕРАЦИОННОЙ БОЛИ
- •Распространенность проблемы по данным исследований
- •Распространенность проблемы по хирургическим данным
- •Аналгезия, контролируемая пациентом
- •Премедикация и техника анестезии
- •Недостаток рутинной количественной оценки
- •Побочное действие анальгетиков
- •Индивидуальные различия реакции на анальгетики
- •НАПРАВЛЕНИЯ И ПУТИ РЕШЕНИЯ
- •Микроскопическое строение
- •Таблица 2-2.
- •Категории ноцицепторов
- •Миелинизированные ноцицепторы
- •Немиелинизированные ноцицепторы
- •Роль ноцицепторов в перцепции боли
- •Сенсибилизация и гиперсенсибилизация
- •Фермент
- •Трансдукция в глубоких соматических тканях
- •Суставы
- •Кости
- •Трансдукция в висцеральных органах
- •Резюме по вопросам трансдукции
- •ЦЕНТРАЛЬНАЯ НЕРВНАЯ СИСТЕМА
- •Ультраструктура спинного мозга
- •Стволовая часть мозга
- •Таблица 2-4.
- •Главные структуры ствола мозга
- •Таламус
- •Первичные афферентные волокна в спинном мозге
- •Терминалы первичных афферентов
- •Нейротрансмиттеры первичных аффекторов
- •Центральная гиперсенсибилизация, или нервное перевозбуждение
- •Восходящие ноцицептивные проводящие пути
- •Вентральный спиноталамический путь
- •Дорсальный столб постсинаптической спинно-медуллярной системы
- •Проприоспинальная мультисинаптическая восходящая система
- •Таламус
- •Гипоталамус и лимбическая система
- •Кора мозга
- •Резюме по вопросам трансмиссии
- •МОДУЛЯЦИЯ
- •Аналгезия, возникающая при стимуляции
- •Аналгезия, обеспечиваемая опиоидами
- •Мост
- •Продолговатый мозг
- •Кора и промежуточный мозг
- •Серотонин
- •Эндогенные опиоиды
- •Резюме по вопросам модуляции
- •ПУТИ КОНТРОЛЯ ТЕОРИИ БОЛИ
- •ПЕРИФЕРИЧЕСКИЙ ОТДЕЛ АВТОНОМНОЙ НЕРВНОЙ СИСТЕМЫ
- •Гипоталамус
- •Субстанция Р
- •Эндокринные
- •Обменные
- •Обмен липидов
- •ЗАКЛЮЧЕНИЕ
- •СВЯЗКИ
- •1. Нет болей
- •Турникетный болевой тест
- •Карбохолиновые кислоты
- •Салициловые кислоты
- •Уксусная кислота
- •Пиролуксусная кислота
- •Фенилацетиловые кислоты
- •Пропионовые кислоты
- •Нафтипропионовые кислоты
- •ПОБОЧНЫЕ ДЕЙСТВИЯ
- •Кожные реакции
- •СООТНОШЕНИЕ СТРУКТУРЫ И АКТИВНОСТИ
- •Опиоидные рецепторы
- •Прототипы
- •Связывание рецепторов и их реакция: истинная активность
- •Типы рецепторов
- •Пути поступления препаратов
- •С помощью общей абсорбции
- •Проникновение к рецепторам
- •Таблица 8-8. Аналгезические эквиваленты опиоидов
- •ЗАКЛЮЧЕНИЕ
- •Список литературы
- •Химическая структура
- •Дозировка
- •Добавки
- •Смеси
- •Беременность
- •ФАРМАКОКИНЕТИКА
- •Абсорбция
- •Распределение
- •Метаболизм и выведение
- •ТОКСИЧНОСТЬ
- •Общая токсичность
- •Токсичность для центральной нервной системы
- •Токсичность для сердечно-сосудистой системы
- •Различные системные эффекты
- •Аллергические реакции
- •Местное токсическое воздействие
- •ОСЛОЖНЕНИЯ РЕГИОНАЛЬНОЙ АНЕСТЕЗИИ
- •Эпидуральная анестезия
- •Уровень блокады
- •Доза препарата
- •Особенности локального анестетика
- •Дополнительное введение вазоконстрикторов
- •Волемическое состояние, объем циркулирующей крови
- •Спинальная анестезия
- •Кокаин
- •Хлоропрокаин
- •Тетракаин
- •Прилокаин
- •Бупивакаин
- •Этидокаин
- •Бензокаин
- •ЗАКЛЮЧЕНИЕ
- •Определение методов АКП и параметры дозировок
- •Инфузионная технология АКП
- •Характеристика прибора
- •Шприц
- •Безопасность
- •Неблагоприятные реакции и побочное действие
- •Взаимодействие прибора и пользователя
- •Образец (парадигма) АКП
- •Непрерывная инфузионная аналгезия для преодоления острой боли
- •Индивидуализация требований аналгезии
- •Вопросы фармакокинетики
- •Факторы фармакодинамики
- •Психологические факторы
- •ПОДКОЖНАЯ АНАЛГЕЗИЯ, КОНТРОЛИРУЕМАЯ ПАЦИЕНТОМ
- •ЭПИДУРАЛЬНАЯ АНАЛГЕЗИЯ, КОНТРОЛИРУЕМАЯ ПАЦИЕНТОМ
- •ЗАКЛЮЧЕНИЕ
- •Список литературы
- •Механизм действия
- •Значение растворимости в липидах
- •Наступление аналгезии
- •Продолжительность аналгезии
- •Ростральная миграция в ЦСЖ
- •Место инъекции
- •Интермитткрующие инъекции или продолжительные инфузии?
- •Показания к применению
- •СУБАРАХНОИДАЛЬНОЕ ВВЕДЕНИЕ ОПИОИДОВ В КЛИНИКЕ
- •Замечания
- •ПОБОЧНОЕ ДЕЙСТВИЕ СПИНАЛЬНЫХ ОПИОИДОВ
- •Угнетение дыхания
- •Таблица 11-5. Побочное действие спинальных опиоидов
- •Тошнота
- •Задержка мочи
- •Активация латентной герпетической инфекции
- •Угнетение функции желудочно-кишечного тракта
- •Неврологические эффекты
- •МОНИТОРИНГ
- •ЗАКЛЮЧЕНИЕ
- •БАЛАНСИРОВАННАЯ АНАЛГЕЗИЯ
- •ЭПИДУРАЛЬНОЕ ВВЕДЕНИЕ ЛОКАЛЬНЫХ АНЕСТЕТИКОВ
- •Влияние эпидуральной блокады на сердечно-сосудистую систему
- •Интермиттирующие инъекции
- •Дозирующие
- •Продолжительные инфузии
- •Тахифилаксия
- •Общие сведения
- •Механизм тахифилаксии
- •Фармакокинетические
- •Фармакодинамические
- •Нейропластические
- •Синергизм аналгезии
- •Угнетение тахифилаксии
- •Угнетение ноцицептивной трансмиссии: афферентный «барраж»
- •Продолжительность действия
- •Клинические исследования
- •Выявление нарушений
- •Осложнения и побочное действие
- •ЗАКЛЮЧЕНИЕ
- •АНАТОМИЯ
- •МЕХАНИЗМ ДЕЙСТВИЯ
- •Противопоказания
- •ПРИМЕНЕНИЕ В КЛИНИКЕ
- •ЗАКЛЮЧЕНИЕ
- •Список литературы
- •АНАТОМИЯ
- •Симпатическая иннервация верхней конечности
- •МЕТОДИКА
- •Межскаленный подход
- •Подключичный периваскулярный доступ
- •Подключичный (инфраклавикулярный) доступ
- •ПРИМЕНЕНИЕ В КЛИНИКЕ
- •ОСЛОЖНЕНИЯ
- •Токсическое действие локальных анестетиков
- •Повреждение нерва
- •ЗАКЛЮЧЕНИЕ
- •АНАТОМИЯ
- •МЕХАНИЗМ ДЕЙСТВИЯ
- •Выполнение процедуры
- •Возможные технические трудности
- •Варианты методики
- •Выбор локального анестетика и его дозировка
- •Интервалы между повторными введениями
- •ПРИМЕНЕНИЕ В КЛИНИКЕ
- •Пневмоторакс
- •Повреждение сосудов
- •Токсическое действие локального анестетика
- •Повреждение нерва
- •ЗАКЛЮЧЕНИЕ
- •АНАТОМИЯ
- •МЕХАНИЗМ АНАЛГЕЗИИ
- •Положение пациента и ориентиры
- •Выполнение процедуры
- •Объем вводимого раствора
- •Другие локальные анестетики
- •Адреналин
- •Длительные внутриплевральные инфузий
- •ПРИМЕНЕНИЕ В КЛИНИКЕ
- •Продолжительная внутриплевральная инфузия
- •ОСЛОЖНЕНИЯ
- •Пневмоторакс
- •Токсическое действие локального анестетика
- •Противопоказания к внутриплевральной региональной аналгезии
- •ПЛЕВРАЛЬНЫЙ ВЫПОТ
- •СИНДРОМ ГОРНЕРА
- •БЛОКАДА ДИАФРАГМАЛЬНОГО НЕРВА
- •ПРОТИВОПОКАЗАНИЯ
- •ЗАКЛЮЧЕНИЕ
- •АНАТОМИЯ
- •МЕХАНИЗМ ДЕЙСТВИЯ
- •МЕТОДИКА
- •Положение пациента и ориентиры
- •Выполнение
- •Варианты методики
- •ПРИМЕНЕНИЕ В КЛИНИКЕ
- •Пневмоторакс
- •Прокол твердой мозговой оболочки
- •Гипотензия
- •Повреждение сосудов
- •Повреждение нервов
- •ЗАКЛЮЧЕНИЕ
- •Список литературы
- •АНАТОМИЯ
- •МЕТОДИКА
- •Мониторинг и подготовка
- •Положение пациента и ориентиры
- •Выполнение процедуры
- •Околосрединный подход
- •Подход по средней линии
- •Контроль проникновения в эпидуральное пространство
- •Потеря сопротивления
- •Ощущение прокола желтой связки
- •Легкость введения катетера
- •Физиологические реакции
- •Выбор анальгетиков и их дозировка
- •Снижение артериального давления
- •Потребность миокарда в кислороде
- •ПРИМЕНЕНИЕ В КЛИНИКЕ
- •ОСЛОЖНЕНИЯ
- •Прокол твердой мозговой оболочки
- •Прокол вены
- •Парестезия
- •Задержка мочи
- •Тошнота
- •Седация
- •Гипотензия
- •Снижение сердечного резерва
- •ЗАКЛЮЧЕНИЕ
- •ЭПИДУРАЛЬНАЯ ГЕМАТОМА
- •Клинические признаки и патофизиология
- •Эпидуральная гематома после субарахноидальной пункции
- •Имеются явные факторы риска
- •Эпидуральная гематома после эпидуральной анестезии
- •ОРИЕНТИРЫ ДЛЯ КРИТИЧЕСКОГО РЕШИТЕЛЬНОГО АНАЛИЗА
- •Предоперационная оценка
- •Нестероидные противовоспалительные препараты
- •Ведение больного в операционном и послеоперационном периодах
- •Время полувыведения
- •Послеоперационный мониторинг
- •ЗАКЛЮЧЕНИЕ
- •Список литературы
- •ИСТОРИЧЕСКАЯ СПРАВКА
- •МЕХАНИЗМ ДЕЙСТВИЯ
- •ТЕХНИЧЕСКИЕ АСПЕКТЫ
- •Продолжительность импульса
- •Постоянный поток или постоянный вольтаж
- •Форма волн
- •Частотность
- •Амплитуда
- •Установка электродов и множественные каналы стимуляции
- •Электроды
- •Сроки стимуляции
- •Побочное действие
- •Противопоказания
- •Методологические аспекты
- •Абдоминальная хирургия
- •ЧЭСН
- •Ортопедичесчик операции
- •Кардиоторакальная хирургия
- •Разные операции
- •Кардиоторакальные операции
- •Различные операции
- •Ортопедические операции
- •Акушерские операции
- •Операции на сердце и на органах грудной клетки
- •Состояние после ампутации
- •ЗАКЛЮЧЕНИЕ
- •Обучение
- •Гипноз
- •Введение в транс
- •Погружение в транс
- •Гипнотическая работа
- •Завершение
- •Релаксационная реакция
- •Достижение релаксационной реакции
- •ЗАКЛЮЧЕНИЕ
- •ПРЕДОПЕРАЦИОННЫЕ ФАКТОРЫ И ПОДГОТОВКА
- •ОЦЕНКА СТЕПЕНИ ВЫРАЖЕННОСТИ БОЛИ
- •Боль у ребенка, не умеющего говорить
- •Оценка степени боли
- •Неопиоиды
- •Опиоиды
- •Опиоиды
- •Внутримышечное введение
- •Интермиттирующее внутривенное введение опиоидов
- •Продолжительное внутривенное введение опиоидов
- •Региональная анестезия/аналгезия
- •Каудальный блок
- •Эпидуральная аналгезия в поясничном и грудном отделах
- •Блокада подвздошно-пахового и подвздошно-подчревного нервов
- •Блокада дорсального нерва полового члена
- •Блокада бедренного и бокового кожного нервов бедра
- •Блокада отсека подвздошной фасции
- •Внутриплевральная региональная аналгезия
- •Инфильтрационная аналгезия операционной раны
- •ЗАКЛЮЧЕНИЕ
- •Внутривенное введение опиоидов
- •Эпидуральное введение опиоидов
- •Морфин
- •Субарахноидально
- •Меперидин
- •Фентанил
- •Суфентанил
- •Буторфанол
- •Бупренорфин
- •Сочетанное применение препаратов
- •Субарахноидальное введение опиоидов
- •Морфин
- •Фентанил
- •Суфентанил
- •Эпидуральное введение клофелина
- •АНАЛГЕЗИЯ ОПИОИДАМИ И ГРУДНОЕ ВСКАРМЛИВАНИЕ
- •ВЫБОР АНАЛГЕЗИИ ПОСЛЕ КЕСАРЕВА СЕЧЕНИЯ
- •Список литературы
- •Артропластика и протезирование тазобедренного сустава
- •Осложнения, % в группе
- •Тазобедренный сустав
- •Субарахноидальное введение опиоидов
- •Эпидуральное введение опиоидов и локальных анестетиков
- •Тазобедренный сустав
- •Коленный сустав
- •Оба сустава
- •Операции со вскрытием коленного сустава
- •Общее назначение опиоидов
- •Субарахноидальное введение опиоидов
- •Эпидуральное введение опиоидов
- •Эпидуральное введение локального анестетика
- •Комбинированная аналгезия
- •Невральная блокада поясничного сплетения
- •Внутрисуставное введение морфина
- •Блокада плечевого сплетения
- •Эпидуральная анестезия/аналгезия в области шеи
- •Ампутация
- •Открытое вправление и внутренняя фиксация переломов лодыжки
- •Невральная блокада седалищного нерва в подколенной области
- •ЗАКЛЮЧЕНИЕ
- •Межреберная невральная блокада
- •Внутриплевральная региональная аналгезия
- •Паравертебральная невральная блокада
- •Криоаналгезия
- •Чрескожная электростимуляция нерва
- •Субарахноидальное введение опиоидов
- •Эпидуралыюе введение локальных анестетиков и опиоидов
- •Введение локальных анестетиков
- •Введение опиоидов
- •Установка эпидурального катетера в грудном или поясничном отделе
- •Комбинированное применение локальных анестетиков и опиоидов
- •Влияние на дыхание
- •ОСОБЫЕ ПРОБЛЕМЫ АНАЛГЕЗИИ ПОСЛЕ ТОРАКОТОМИИ
- •ЗАКЛЮЧЕНИЕ
- •Сенсибилизация ноцицепторов
- •Глубокая соматическая боль
- •Трансмиссия
- •Иррадиирующая боль
- •Предполагаемые механизмы иррадиирующей боли
- •Последовательные рефлекторные реакции
- •Кортикальные реакции
- •Нарушения функции легких
- •Осложнения со стороны желудочно-кишечного тракта
- •Тромбоэмболия
- •Аналгезия, контролируемая пациентом
- •Межреберная невральная блокада
- •Внутриплевральная региональная аналгезия
- •Аналгезия при ВПА
- •Субарахноидальное введение опиоидов
- •Эпидуральное введение локальных анестетиков и опиоидов
- •Операции на нижнем отделе брюшной полости
- •Аппендэктомия
- •Операции на толстом кишечнике
- •Опорожнение желудка и подвижность тонкого кишечника
- •Моторика толстого кишечника
- •ЗАКЛЮЧЕНИЕ
- •ДВА МНЕНИЯ: АНАЛГЕЗИЯ ПРОТИВ ДИАГНОСТИКИ
- •ФИЗИОЛОГИЧЕСКИЕ НАРУШЕНИЯ, СВЯЗАННЫЕ С ТРАВМОЙ
- •Региональная анестезия/аналгезия
- •Подкожная инфильтрационная анестезия
- •Бупивакаин
- •Фоновая блокада
- •Периферическая невральная блокада
- •Блокада сплетения
- •Внутриплевральная региональная аналгезия
- •Эпидуральная аналгезия
- •Субарахноидальная аналгезия
- •ТРАВМЫ ГОЛОВЫ
- •ТРАВМЫ ГРУДНОЙ КЛЕТКИ
- •ПОВРЕЖДЕНИЯ СКЕЛЕТА
- •ЗАКЛЮЧЕНИЕ
- •КОММУНИКАЦИЯ
- •ВРАЧЕБНЫЙ ВКЛАД
- •КОНЦЕПЦИЯ «ГЛОБАЛЬНОГО ГОНОРАРА»
- •Администрация госпиталей
- •Приобретение оборудования
- •Маркетинг
- •ЗАКЛЮЧЕНИЕ
- •Цели
- •Группа задач, связанных с АКП
- •Распределение препаратов
- •Участие медицинских сестер в переориентировке целей
- •Доза АКП, мг
- •Объекты проведения целевых усилии
- •АЛЬТЕРНАТИВНЫЕ МЕТОДЫ КОНТРОЛЯ БОЛИ
- •Поза, позиционная установка
- •Сон, релаксация
- •Тошнота, рвота
- •Стимуляция активности пациента
- •Психологический статус
- •Дополнительные медикаментозные назначения
- •ЗАКЛЮЧЕНИЕ
- •АНАЛГЕЗИЯ, КОНТРОЛИРУЕМАЯ ПАЦИЕНТОМ
- •Аналгезия, контролируемая пациентом
- •Общие указания
- •Обучение пациента/родственников
- •ПЕРСОНАЛЬНЫЙ ФАКТОР
- •Анестезиолог
- •Сестринская помощь
- •Фармакологическая служба
- •ОБОРУДОВАНИЕ
- •Простота и легкость в обращении
- •Ограничитель скорости потока
- •Приборы для эпидуральной инфузии
- •Вход для инъекций
- •Безопасность
- •Мониторы
- •ПРОЦЕДУРЫ, ПРОВОДИМЫЕ СЛУЖБОЙ ОСТРОЙ БОЛИ
- •Документация
- •ПРОБЛЕМЫ, СТОЯЩИЕ ПЕРЕД СЛУЖБОЙ ОСТРОЙ БОЛИ
- •Проблемы, стоящие перед СОБ
- •МОЛЕКУЛЯРНАЯ ФАРМАКОЛОГИЯ
- •Нейроэндокринная система
- •Сердечно-сосудистая система
- •Дыхательная система
- •Почки
- •Пищеварительная система
- •Центральная нервная система
- •МЕХАНИЗМ АНАЛГЕЗИИ
- •Нейроэндокринные
- •Сердечно-сосудистые
- •Респираторные
- •Желудочно-кишечные
- •Центральная нервная система
- •Эпидуральное назначение
- •Субарахноидальное введение
- •ЗАКЛЮЧЕНИЕ

Мембранный потенциал покоя тесно связан с соотношением ионов калия внутри (К;) и снаружи (Кд) мембраны. В состоянии покоя соотношение Кi/Кo равно примерно 30:1. Клеточные мембраны относительно непроницаемы для ионов натрия, поэтому они не создают мембранного потенциала покоя.
После возбуждения проницаемость клеточной мембраны возрастает. Ионы натрия начинают проходить внутрь клетки по натриевому каналу. Это движение ионов натрия внутрь клетки характеризует деполяризационную фазу потенциала действия (приток катионов объясняет положительный мембранный потенциал). По мере нарастания деполяризации проницаемость ее для ионов натрия падает(инактивация натриевого канала). Усиливающийся поток ионов калия из клетки приводит к реполяризации клеточной мембраны.
Рис. 9-1. Поверхностный потенциал действия, записанный на изолированном нерве (а). Активация натриевого канала в фазе деполяризации и открытие калиевого канала в фазе реполяризации (б).
Таблица 9-1. Химическая структура, физико-химические, фармакологические свойства и преимущественноеKJ] ческое использование локальных анестетиков
Пре- |
Химическая структура |
Физико-химические свойФармакологичес- |
|
па- |
|
ства |
кие свойства |

рат |
аро- |
про- |
ами- |
мол. |
рКа |
раз- |
свя- |
нача- |
отно- |
дли- |
ос- |
|
мати- |
межу |
ны |
масса |
(25 |
дели- |
зыва- |
ло |
сител |
тель- |
новк |
|
ческая |
точ- |
ги- |
осно- |
°С) |
тель- |
ние |
дейст- |
ьная |
ность |
при- |
|
липо- |
ная |
дро- |
вания |
|
ный |
бел- |
вия |
мощ- |
|
мени |
|
филь- |
цепь |
филь- |
|
|
коэф- |
ками, |
|
ность |
|
В |
|
ность |
|
ные |
|
|
фи- |
% |
|
|
|
КЛИ |
|
|
|
|
|
|
циент |
|
|
|
|
Н] |
|
|
|
|
|
|
|
|
|
|
|
|
Поток ионов натрия и калия во время возбужденияэто пассивный феномен, поскольку передвижение этих ионов происходит в соответствии с градиентом их концентрации. В конце потенциала действия образуется избыток ионов натрия внутри клетки при избытке ионов калия вне клетки. Восстановление ионного соотношения по обе стороны клеточной мембраны тре-
бует затрат энергии для выталкивания ионов натрия против градиента их

концентрации. Ионы калия также активно транспортируются снаружи внутрь нервной мембраны. Ионы калия могут перемещаться также и пассивно в силу электростатического градиента. Энергия, необходимая для активного транспорта ионов натрия и калия(так называемый натриевый насос), обеспечивается метаболизмом аденозинтрифосфата (АТФ).
Воздействие локального анестетика на изолированный нерв заметно не меняет потенциал покоя и пороговый потенциал. Под влиянием 0,005% раствора лидокаина (0,2 мМ) максимальная скорость подъема потенциала действия снижается по сравнению с контролем со 190 В/с до 120 В/с. Скорость реполяризации при этом не изменяется [I].
Локальные анестетики снижают проницаемость мембраны нервных клеток к натрию. Например, при обычной концентрации натрия, равной 116 мМ, высота потенциала действия снижается на50% при воздействии 3,3 ммоль кокаина на изолированный седалищный нерв лягушки[2]. Однако если концентрация натрия в окружающем нерв растворе снижена до12 ммоль, достаточно 0,15 ммоль кокаина, чтобы вызвать подобное снижение амплитуды потенциала действия. При непосредственных исследованиях проводимости натрия и калия было выявлено полное прекращение потока натрия в присутствии 1 ммоль лидокаина. В то же время3,5 ммоль лидокаина снижают проведение калия всего на 5% [3, 4].
Большинство используемых в клинике локальных анестетиков выпускают в виде растворов солей (например, 0,5-2% раствор лидокаина гидрохлорида). В таких растворах соли локальных анестетиков присутствуют как в виде незаряженных оснований (В), так и в виде положительно заряженных катионов (ВН+). Соотношение между этими компонентами определяется специфичностью состава самого вещества(рНа) и величиной рН раствора. Это соотношение можно выразить следующей формулой:
Поскольку рНа является величиной постоянной для любого химического соединения, то соотношение свободной основы (В) и заряженного катиона (BН+) будет зависеть от величины рН раствора местного анестетика. По мере снижения величины рН и роста концентрацииH+ равновесие будет смещаться в сторону заряженных катионных форм. И напротив, по мере роста рН и снижения концентрации ионовH+ равновесие будет смещаться в сторону свободных основных форм.
Вдействии локального анестетика принимают участие два фактора:
1)диффузия через оболочки нерва и его мембраны;
2)процессы связывания на некоторых участках клеточной мембраны.
В изолированном нерве с интактным эпиневрием при повышении рН омывающего раствора анестетика(что благоприятствует формированию В) значительно увеличивается скорость падения высоты поверхностного потенциала действия. Однако в нервах, лишенных оболочки, более слабые щелоч-
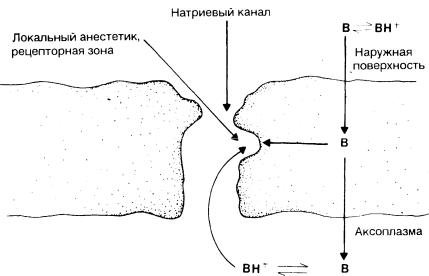
ные растворы (способствующие накоплению заряженных катионов) усиливают действие локальных анестетиков. Эти наблюдения показывают, что незаряженные основные формы (В) играют важную роль в оптимальной проницаемости оболочки нерва [5, 6]. Равновесие между В и ВН+ восстанавливается благодаря диффузии через периневрий. Что касается клеточной мембраны, то заряженные катионы в конечном счете определяют супрессию электрофизиологических процессов в периферическом нерве [7] (рис. 9-2).
Рис. 9-2. Схематическое отображение действия локального анестетика, блокирующего проводимость. Основная форма (В) определяет преимущественную диффузию через нервную мембрану в направлении аксоплазмы, где происходит конверсия в катионы(ВН+). Катионы главным образом вовлекаются в соединение с рецепторными зонами в натриевом канале, что и приводит к его блокаде.
Локальный анестетик проявляет свое фармакологическое действие в натриевом канале. Полагают, что именно там препараты этого ряда связываются с рецепторами и это связывание в конечном счете инактивируетна триевый канал, блокируя его [8]. Исследования, проведенные с третичными амидами локальных анестетиков и с четвертичными производными лидокаина, установили, что анестезирующее действие этих веществ усиливается при их нанесеннии на внутреннюю поверхность нервной мембраны[9]. Таким образом, полагают, что обычные локальные анестетики (например, лидокаин) входят в натриевый канал со стороны аксоплазмы (см. рис. 9-2).
Высказано предположение, что проводниковая блокада натриевого канала определяется главным образом катионами локальных анестетиков благодаря их взаимодействию с расположенными в нем рецепторными зонами. Однако незаряженные основания также могут влиять на действие этих анестетиков. Незаряженные основания проникают через липидные участки клеточной мембраны и вызывают структурные изменения в липопротеиновой матрице. При этом диаметр натриевого канала уменьшается, что и угнетает проведение натрия. Таким образом, последовательность процессов, приво-
дящих к проводниковой блокаде периферического нерва под влиянием - ло кального анестетика, можно представить следующим образом.
1.Диффузия основных форм локального анестетика через оболочку нерва и нервную мембрану.
2.Восстановление равновесия между основными и катионными формами локального анестетика на аксиальной поверхности нервной мембраны.
3.Проникновение внутрь и фиксация локального анестетика в зоне рецепторов в натриевом канале.
4.Блокада натриевого канала.
5.Угнетение проведения натрия.
6.Снижение скорости и степени фазы деполяризации потенциала дей-
ствия.
7.Невозможность достигнуть порогового уровня потенциала.
8.Недостаточное развитие потенциала действия.
9.Проводниковая блокада.
ВЗАИМООТНОШЕНИЕ СТРУКТУРЫ И ДЕЙСТВИЯ
Соединения, обладающие клинически выраженным обезболивающим действием, имеют следующую химическую структуру: ароматическая часть– промежуточная цепь–аминная часть. Изменения в каждом из звеньев этой структуры сказываются на обезболивающем действии препарата. Например, увеличение молекулярной массы, удлинение промежуточной цепи, включение дополнительного атома углерода в ароматическую или в аминную часть анестетика усиливает собственные анестезирующие свойства препарата, приближая их к максимально возможным[10]. Дальнейшее увеличение молекулярной массы, напротив, приводит к ослаблению анестезирующего действия препарата. Ароматическая часть молекулы локального анестетика обычно определяет степень его липофильности, а аминная часть ассоциируется с гидрофильностью. Изменения в ароматическом или в аминном компоненте нарушают водно-липидный коэффициент распределения соответствующего анестетика. Химическая модификация любого из краевых участков молекулы нарушает связывание препарата с протеинами, что в свою очередь сказывается на его анестезирующих характеристиках. Например, присоединение бутиловой группы к ароматическому звену молекулы прокаина повышает его липофильность и связывание с протеинами. Это сопровождается усилением обезболивающего действия препарата и удлинением продолжительности его действия (тетракаин) [11]. Присоединение бутиловой группы к аминному концу молекулы мепивакаина трансформирует этот препарат, делая его еще более липофильным и прочно связывающимся с протеинами. Этот новый препарат (бупивакаин) обладает более мощным и продолжительным действием [12] (см. табл. 9-1). Если в молекуле лидокаина подставить пропил вместо этиловой группы на аминном конце и этиловую группу к- а углероду промежуточной цепи, получаем препарат этидокаин. Последний

лучше растворим в липидах, прочнее связывается с белками, обладает более выраженным и стойким местным анестезирующим действием [13].
Локальные анестетики, используемые в клинической практике, можно распределить на две различные в химическом отношении категории.
1.Препараты с эфирным звеном, расположенным между ароматическим концом молекулы и промежуточной цепью. Примерами таких амино-эфирных препаратов являются прокаин, хлорпрокаин, тетракаин.
2.Соединения, содержащие аминное звено между ароматическим концом и промежуточной цепью.
Представителями подобных аминоамидных препаратов являются лидокаин, мепивакаин, прилокаин, бупивакаин и этидокаин.
Основные различия между соединениями, содержащими эфир или амид, заключаются, во-первых, в путях их метаболизма ,иво-вторых, в их аллергизирующем потенциале.
Эфиросодержащие препараты гидролизируются в плазме под действием псевдохолинэстеразы, а аминосодержащие соединения разрушаются ферментами печени. Парааминобензойная кислота является одним из метаболитов, образующихся при гидролизе эфиросодержащих препаратов. У некоторых больных эта кислота способна индуцировать реакции аллергического типа. Соединения аминоамидного типа не распадаются с образованием парааминобензойной кислоты и крайне редко вызывают аллергические реакции.
ФАРМАКОЛОГИЯ
В клинике имеют значение такие свойства локального анестетика как сила обезболивающего действия, скорость наступления обезболивания, его продолжительность, а также способность к дифференцированной сенсорной и моторной блокаде. Профиль клинического действия локального анестетика в каждом случае зависит от особенностей его физико-химических характеристик, определяемых химической структурой вещества. Подобными физикохимическими характеристиками, влияющими на анестезирующие возможности, служат растворимость в липидах, связывание с протеинами, а также рКа. Даже минимальные модификации молекулярной структуры могут коренным образом изменить указанные характеристики.
Возможности обезболивающего действия
Растворимость в липидах, по-видимому, является первостепенным показателем обезболивающей способности препарата. Мембрана нервной клетки в основном - представлена липопротеиновым матриксом. Аксолемма на 90% состоит из липидов и на 10% - из протеинов. В результате этого химиче-
ские вещества с высокой липофильностью легче и быстрее преодолевают клеточные мембраны. Проводниковая блокада обеспечивается небольшим числом молекул, что отражает высокую действенность препарата. Экспериментальные исследования на изолированном нерве подтвердили существова-
ние четкой корреляции между коэффициентом разделения локального анестетика и величиной минимальной концентрации (Сm), обеспечивающей проводниковую анестезию [14, 15]. Например, мепивакаин, прилокаин и препараты из группы аминоамидов в наименьшей степени растворимы в липидах и соответственно обладают самым слабым обезболивающим действием. В противоположность этому этидокаин, наиболее липофильный препарат этой группы, является и наиболее действенным анестетиком(см. табл. 9-1). Подобная же зависимость между растворимостью в липидах и клиническим действием наблюдается и у препаратов эфирного ряда. Прокаин наименее растворим в липидах и малоэффективен. В то же время тетракаин обладает высокой липофильностью и наиболее выраженным обезболивающим действием среди препаратов эфирного ряда.
Помимо растворимости препарата в липидах, его обезболивающее действие определяется также и другими факторами. Сопоставление величин коэффициентов распределения и анестезирующего действия локальных анестетиков эфирного и амидного рядов показало, что это действие у аминоэфиров значительно выше, чем у аминоамидов даже при одинаковых коэффициентах распределения (см. табл. 9-1). Аминоэфиры взаимодействуют с большим числом различных рецепторов, что обеспечивает им значительно большие возможности действия [16].
Экспериментальные исследования показали, что в организме человека корреляция между липофильностью анестетика и его действенностью не столь выражена, как в опытах на изолированном нерве. Лидокаин был почти вдвое активнее прилокаина и мепивакаина в опытах на препаратах изолированного нерва. Однако у человека все три анестетика оказывали примерно одинаковое действие. Точно так же этидокаин, более активный, чем бупивакаин в опытах на изолированном нерве, в условиях клиники оказался слабее.
Разное действие локальных анестетиков в лабораторных условиях и в клинике может быть обусловлено различным их распределением в тканях и сосудорасширяющим эффектом. Например, лидокаин расширяет сосуды сильнее, чем мепивакаин или прилокаин, и поэтому быстрее абсорбируется.
Меньшие по размерам молекулы лидокаина также предрасполагают к более быстрому наступлению блокады при клиническом использовании. Очень высокая липофильность этидокаина приводит к тому, что весьма значительные количества этого препарата захватываются жировой тканью эпидурального пространства. Поэтому для создания невральной блокады остается меньшее число молекул, чем это имеет место при назначении бупивакаина.
Продолжительность действия
Продолжительность обезболивания под влиянием локальных анестетиков зависит прежде всего от степени их связывания с белками. Эти препараты, по-видимому, образуют комплексы с белковыми рецепторами, расположенными в натриевом канале нервной мембраны. Чем выше аффинитет и прочнее связь этих химических соединений, тем дольше будет блокирован

рецептор в натриевом канале. Результатом этого и станет более продолжительная блокада проводимости нерва. Большая часть информации о связывании локальных анестетиков с белками получена на примере взаимодействия этих веществ с белками плазмы. При этом постулировано, что процессы связывания локальных анестетиков в нервной мембране и в плазме крови идентичны.
Лабораторные исследования установили, что локальные анестетики, слабо комплексирующиеся с белками(например, прокаин), быстро вымываются из изолированного нерва. В то же время такие препараты, как тетракаин, бупивакаин, этидокаин, длительно задерживаются в нем. Опыты in vivo, в том числе и в клинических условиях, подтвердили, что существует зависимость между белковым связыванием местных анестиков и продолжительностью их действия. Например, прокаин обеспечивает блокаду плечевого сплетения в течение 30-60 мин, в то время как бупивакаин или этидокаин поддерживают ее на протяжении до 10 ч [17].
Продолжительность местной анестезии у человека в значительной сте- пени зависит от сосудистых изменений на периферии, вызванных самими обезболивающими средствами. Все локальные анестетики, за исключением кокаина, оказывают двоякое влияние на гладкие мышцы сосудов. В малой концентрации эти вещества вызывают сужение сосудов, а в терапевтической - их расширение [18, 19]. Однако величина вазодилатации, вызываемой отдельными анестетиками, весьма различна. Например, лидокаин обладает более мощным сосудорасширяющим действием, чем мепивакаин или прилокаин. В экспериментах на изолированном нерве эти препараты блокируют проведение нервного импульса примерно на одинаковый срок, однако in vivo лидокаин обеспечивает анестезию на более короткое время, чем мепивакаин или прилокаин. Если же одновременно с анестетиками вводятся сосудосуживающие вещества, то продолжительность действия всех трех локальных анестетиков становится одинаковой.
Наступление действия
Развитие блока проводимости в изолированном нерве зависит прежде всего от величины рКa соответствующего анестетика [5]. Эта величина равна показателю рН при условии, что ионизированная и неионизированная формы этого химического соединения присутствуют в равных количествах. Диффузия локального анестетика через оболочку нерва и через нервную мембрану определяется прежде всего незаряженной формой препарата. Поэтому сроки наступления обезболивания находятся в прямой зависимости от количества препарата в его основной форме (табл. 9-2).
Процентное содержание локального анестетика в форме основания при его введении в ткани с рН7,4 обратно пропорционально рКд этого вещества. Например, мепивакаин, лидокаин, прилокаин и этидокаин имеют рН7,7. Когда эти препараты вводят в ткани с рН7,4, то около 65% их общего количества находятся в ионизированной форме и остальные35% остаются неиони-
зированными. Тетракаин имеет рКa 8,6. Поэтому в тканях с рН 7,4 только 5% этого препарата остаются неионизированными, а остальные 95% приобретают форму заряженного катиона. Величина рКa бупивакаина - 8,1, и в тканях с обычным рН лишь около15% его количества присутствуют в неионизированной форме, а 85% - в форме заряженного катиона. Следовательно, лидокаин, мепивакаин, прилокаин и этидокаин относятся к препаратам с быстрым
наступлением действия (низкие показатели рК), в то время как действие
a
прокаина и тетракаина наступает медленно (высокие величины pKa)(см. табл. 9-2). Бупивакаин занимает промежуточное положение как по величине рКд, так и по срокам наступления его действия [20, 21].
Таблица 9-2. Соотношение рКд к процентному содержанию основных форм и время
развития 50% проводникового блока в изолированном нерве
Препарат |
Химический |
рКа |
Процент ос- |
Начало, мин |
|
класс |
|
нований |
|
|
|
|
при рН = 7,5 |
|
Прилокаин |
Аминоамид |
7,7 |
35 |
2-4 |
Лидокаин |
» |
7,7 |
35 |
2-4 |
Этидокаин |
» |
7,7 |
35 |
2-4 |
Бупивакаин |
» |
8,1 |
20 |
5-8 |
Тетракаин |
Аминоэфир |
8,6 |
5 |
10-15 |
Прокаин |
|
8,9 |
2 |
14-18 |
Наступление блока проводимости in vivo зависит частично и от других условий. Эффект может задерживаться вследствие диффузии препарата через окружающие нерв ткани. Например, лидокаин и прилокаин обладают одина-
ковыми рК и одновременно проявляют свое действие на изолированном
а
нерве. Однако in vivo влияние прилокаина иногда может сказываться позже, чем лидокаина. Это различие обусловлено лучшей способностью последнего диффундировать через различные тканевые структуры. Более важное значение имеет концентрация введенного анестетика. Например, 0,25% бупивакаин замедленно проявляет свое действие, но при повышении концентрации до 0,75% сроки наступления анестезии значительно сокращаются. Быстрое действие хлоропрокаина in vivo можно объяснить не только легкостью его диффузии через тканевые структуры, но и высокой концентрацией(3%) вводи-
мого препарата. У хлоропрокаина рК равна примерно 9, и его действие на
а
изолированном нерве проявляется замедленно [22]. Правда, благодаря низкой токсичности этого препарата его можно назначать в высоких концентрациях. Поэтому быстрый эффект после инъекции хлоропрокаина может объясняться большим количеством его молекул в окружении периферического нерва.
Различия сенсорной и моторной блокады

Важным для клиники фактором является способность локального ан-е стетика избирательно блокировать чувствительные и двигательные волокн.а Предпринимались попытки субарахноидального введения прокаина в -раз личных концентрациях для того, чтобы дифференцирование блокировать чувствительные, симпатические и двигательные волокна. Однако оказалось крайне трудно обеспечить обезболивание, достаточное для хирургического вмешательства, заметно не нарушая при этом двигательную функцию. Бупивакаин оказался первым из препаратов, обладающих относительной специфичностью в отношении чувствительных волокон. Он создавал адекватную сенсорную анестезию/аналгезию, не сопровождающуюся глубоким угнетением движений. Бупивакаин и этидокаин, одинаково мощные и длительно действующие препараты, различаются по своей способности блокировать сенсорную и двигательную активность(рис. 9-3). Бупивакаин широко применяют эпидурально в хирургической и в акушерской практике, а также для устранения послеоперационной боли, используя его способность создавать адекватную аналгезию при минимальной блокаде двигательных волокон. Эти свойства наиболее выражены при введении0,25% или 0,5% раствора. Благодаря этому роженица может быть избавлена от болей, но способна двигать
ногами. Это послужило одной из главных причин широкой популярности длительной эпидуральной анестезии бупивакаином при родах. Повышение концентрации препарата до 0,75% заметно углубляет как сенсорную, так и моторную блокаду, ускоряет наступление анестезии и увеличивает ее продолжительность [23].
Рис. 9-3. Относительная величина сенсорной и моторной блокады призпидуральном введении бупивакаина и этидокаина в различных концентрациях.
Раздельное влияние этидокаина на чувствительность и на моторику не столь выражено (см. рис. 9-3). Адекватная анестезия достигается при эпидуральном введении этидокаина в концентрации 1,5%. При этой дозировке действие препарата проявляется очень быстро и продолжается длительно. Однако обезболивающий эффект сочетается с глубокой двигательной блокадой. Следовательно, этидокаин относится к препаратам, особенно ценным для эпидуральной анестезии в хирургической практике, когда одновременно с
обезболиванием желательна глубокая мышечная релаксация. Этидокаин как раз и обеспечивает быстрый и длительный эффект при хорошей анестезии, сочетающейся с глубокой двигательной блокадой. В то же время столь значительное воздействие этидокаина на двигательную функцию ограничивает его применение в акушерской практике и в устранении послеоперационных болей.
Факторы, объясняющие дифференцированное воздействие бупивакаина на чувствительность и на моторику, изучены недостаточно. Исследования на изолированном нерве показали, что бупивакаин в малых концентрациях раньше всего блокирует немиелинизированные С-волокна и лишь в последующем - спустя некоторое времямиелинизированные А-волокна [24]. Этидокаин блокирует С- и А-волокна примерно с одинаковой скоростью. Предполагается, что замедленная блокада А-волокон бупивакаином связана с
относительно более высоким рК этого препарата. Более мелкие незаряжен-
а
ные молекулы легче диффундируют через тканевые барьеры, окружающие А-волокна (высокая степень их миелинизации и большой диаметр). Сочетание in vivo таких факторов, как замедленная диффузия бупивакаина и его абсорбция из места инъекции, значительно снижает число молекул препарата,
преодолевающих в конечном счете мембрану больших двигательных- А волокон. Это число может оказаться недостаточным для блокады их проводимости. В то же время более слабый барьер вокруг малых С-волокон пропускает достаточно молекул бупивакаина к рецепторам их нервной мембраны, обеспечивая анестезию. Таким образом, бупивакаин, вероятно, обладает оптимальным рКа и липофильностью, требующимися для дифференцированной сенсорной моторной блокады.
Следовательно, фармакологическая активность локальных анестетиков связана главным образом с их физико-химическими свойствами. Однако in vivo активность этих препаратов подвержена влиянию и других факторов, непосредственно не связанных с их физико-химическими свойствами. Возможна следующая классификация анестезирующих препаратов в зависимости от их активности в клинике.
1.Препараты слабой обезболивающей активности и кратковременного действия - прокаин и хлоропрокаин.
2.Препараты промежуточной обезболивающей активности и средней продолжительности действия - лидокаин, мепивакаин и прилокаин.
3.Препараты высокой обезболивающей активности и большой продолжительности действия - тетракаин, бупивакаин и этидокаин.
Вотношении сроков наступления своего действия хлоропрокаин, лидокаин, мепивакаин, прилокаин и этидокаин относятся к препаратам, дающим быстрый эффект. Бупивакаин причисляют к препаратам промежуточного действия, а прокаин и тетракаин - к препаратам, замедленно вызывающим обезболивание.
