
- •Майкл Ферранте
- •Майкл
- •ЗНАЧИМОСТЬ ПРОБЛЕМЫ ПОСЛЕОПЕРАЦИОННОЙ БОЛИ
- •Распространенность проблемы по данным исследований
- •Распространенность проблемы по хирургическим данным
- •Аналгезия, контролируемая пациентом
- •Премедикация и техника анестезии
- •Недостаток рутинной количественной оценки
- •Побочное действие анальгетиков
- •Индивидуальные различия реакции на анальгетики
- •НАПРАВЛЕНИЯ И ПУТИ РЕШЕНИЯ
- •Микроскопическое строение
- •Таблица 2-2.
- •Категории ноцицепторов
- •Миелинизированные ноцицепторы
- •Немиелинизированные ноцицепторы
- •Роль ноцицепторов в перцепции боли
- •Сенсибилизация и гиперсенсибилизация
- •Фермент
- •Трансдукция в глубоких соматических тканях
- •Суставы
- •Кости
- •Трансдукция в висцеральных органах
- •Резюме по вопросам трансдукции
- •ЦЕНТРАЛЬНАЯ НЕРВНАЯ СИСТЕМА
- •Ультраструктура спинного мозга
- •Стволовая часть мозга
- •Таблица 2-4.
- •Главные структуры ствола мозга
- •Таламус
- •Первичные афферентные волокна в спинном мозге
- •Терминалы первичных афферентов
- •Нейротрансмиттеры первичных аффекторов
- •Центральная гиперсенсибилизация, или нервное перевозбуждение
- •Восходящие ноцицептивные проводящие пути
- •Вентральный спиноталамический путь
- •Дорсальный столб постсинаптической спинно-медуллярной системы
- •Проприоспинальная мультисинаптическая восходящая система
- •Таламус
- •Гипоталамус и лимбическая система
- •Кора мозга
- •Резюме по вопросам трансмиссии
- •МОДУЛЯЦИЯ
- •Аналгезия, возникающая при стимуляции
- •Аналгезия, обеспечиваемая опиоидами
- •Мост
- •Продолговатый мозг
- •Кора и промежуточный мозг
- •Серотонин
- •Эндогенные опиоиды
- •Резюме по вопросам модуляции
- •ПУТИ КОНТРОЛЯ ТЕОРИИ БОЛИ
- •ПЕРИФЕРИЧЕСКИЙ ОТДЕЛ АВТОНОМНОЙ НЕРВНОЙ СИСТЕМЫ
- •Гипоталамус
- •Субстанция Р
- •Эндокринные
- •Обменные
- •Обмен липидов
- •ЗАКЛЮЧЕНИЕ
- •СВЯЗКИ
- •1. Нет болей
- •Турникетный болевой тест
- •Карбохолиновые кислоты
- •Салициловые кислоты
- •Уксусная кислота
- •Пиролуксусная кислота
- •Фенилацетиловые кислоты
- •Пропионовые кислоты
- •Нафтипропионовые кислоты
- •ПОБОЧНЫЕ ДЕЙСТВИЯ
- •Кожные реакции
- •СООТНОШЕНИЕ СТРУКТУРЫ И АКТИВНОСТИ
- •Опиоидные рецепторы
- •Прототипы
- •Связывание рецепторов и их реакция: истинная активность
- •Типы рецепторов
- •Пути поступления препаратов
- •С помощью общей абсорбции
- •Проникновение к рецепторам
- •Таблица 8-8. Аналгезические эквиваленты опиоидов
- •ЗАКЛЮЧЕНИЕ
- •Список литературы
- •Химическая структура
- •Дозировка
- •Добавки
- •Смеси
- •Беременность
- •ФАРМАКОКИНЕТИКА
- •Абсорбция
- •Распределение
- •Метаболизм и выведение
- •ТОКСИЧНОСТЬ
- •Общая токсичность
- •Токсичность для центральной нервной системы
- •Токсичность для сердечно-сосудистой системы
- •Различные системные эффекты
- •Аллергические реакции
- •Местное токсическое воздействие
- •ОСЛОЖНЕНИЯ РЕГИОНАЛЬНОЙ АНЕСТЕЗИИ
- •Эпидуральная анестезия
- •Уровень блокады
- •Доза препарата
- •Особенности локального анестетика
- •Дополнительное введение вазоконстрикторов
- •Волемическое состояние, объем циркулирующей крови
- •Спинальная анестезия
- •Кокаин
- •Хлоропрокаин
- •Тетракаин
- •Прилокаин
- •Бупивакаин
- •Этидокаин
- •Бензокаин
- •ЗАКЛЮЧЕНИЕ
- •Определение методов АКП и параметры дозировок
- •Инфузионная технология АКП
- •Характеристика прибора
- •Шприц
- •Безопасность
- •Неблагоприятные реакции и побочное действие
- •Взаимодействие прибора и пользователя
- •Образец (парадигма) АКП
- •Непрерывная инфузионная аналгезия для преодоления острой боли
- •Индивидуализация требований аналгезии
- •Вопросы фармакокинетики
- •Факторы фармакодинамики
- •Психологические факторы
- •ПОДКОЖНАЯ АНАЛГЕЗИЯ, КОНТРОЛИРУЕМАЯ ПАЦИЕНТОМ
- •ЭПИДУРАЛЬНАЯ АНАЛГЕЗИЯ, КОНТРОЛИРУЕМАЯ ПАЦИЕНТОМ
- •ЗАКЛЮЧЕНИЕ
- •Список литературы
- •Механизм действия
- •Значение растворимости в липидах
- •Наступление аналгезии
- •Продолжительность аналгезии
- •Ростральная миграция в ЦСЖ
- •Место инъекции
- •Интермитткрующие инъекции или продолжительные инфузии?
- •Показания к применению
- •СУБАРАХНОИДАЛЬНОЕ ВВЕДЕНИЕ ОПИОИДОВ В КЛИНИКЕ
- •Замечания
- •ПОБОЧНОЕ ДЕЙСТВИЕ СПИНАЛЬНЫХ ОПИОИДОВ
- •Угнетение дыхания
- •Таблица 11-5. Побочное действие спинальных опиоидов
- •Тошнота
- •Задержка мочи
- •Активация латентной герпетической инфекции
- •Угнетение функции желудочно-кишечного тракта
- •Неврологические эффекты
- •МОНИТОРИНГ
- •ЗАКЛЮЧЕНИЕ
- •БАЛАНСИРОВАННАЯ АНАЛГЕЗИЯ
- •ЭПИДУРАЛЬНОЕ ВВЕДЕНИЕ ЛОКАЛЬНЫХ АНЕСТЕТИКОВ
- •Влияние эпидуральной блокады на сердечно-сосудистую систему
- •Интермиттирующие инъекции
- •Дозирующие
- •Продолжительные инфузии
- •Тахифилаксия
- •Общие сведения
- •Механизм тахифилаксии
- •Фармакокинетические
- •Фармакодинамические
- •Нейропластические
- •Синергизм аналгезии
- •Угнетение тахифилаксии
- •Угнетение ноцицептивной трансмиссии: афферентный «барраж»
- •Продолжительность действия
- •Клинические исследования
- •Выявление нарушений
- •Осложнения и побочное действие
- •ЗАКЛЮЧЕНИЕ
- •АНАТОМИЯ
- •МЕХАНИЗМ ДЕЙСТВИЯ
- •Противопоказания
- •ПРИМЕНЕНИЕ В КЛИНИКЕ
- •ЗАКЛЮЧЕНИЕ
- •Список литературы
- •АНАТОМИЯ
- •Симпатическая иннервация верхней конечности
- •МЕТОДИКА
- •Межскаленный подход
- •Подключичный периваскулярный доступ
- •Подключичный (инфраклавикулярный) доступ
- •ПРИМЕНЕНИЕ В КЛИНИКЕ
- •ОСЛОЖНЕНИЯ
- •Токсическое действие локальных анестетиков
- •Повреждение нерва
- •ЗАКЛЮЧЕНИЕ
- •АНАТОМИЯ
- •МЕХАНИЗМ ДЕЙСТВИЯ
- •Выполнение процедуры
- •Возможные технические трудности
- •Варианты методики
- •Выбор локального анестетика и его дозировка
- •Интервалы между повторными введениями
- •ПРИМЕНЕНИЕ В КЛИНИКЕ
- •Пневмоторакс
- •Повреждение сосудов
- •Токсическое действие локального анестетика
- •Повреждение нерва
- •ЗАКЛЮЧЕНИЕ
- •АНАТОМИЯ
- •МЕХАНИЗМ АНАЛГЕЗИИ
- •Положение пациента и ориентиры
- •Выполнение процедуры
- •Объем вводимого раствора
- •Другие локальные анестетики
- •Адреналин
- •Длительные внутриплевральные инфузий
- •ПРИМЕНЕНИЕ В КЛИНИКЕ
- •Продолжительная внутриплевральная инфузия
- •ОСЛОЖНЕНИЯ
- •Пневмоторакс
- •Токсическое действие локального анестетика
- •Противопоказания к внутриплевральной региональной аналгезии
- •ПЛЕВРАЛЬНЫЙ ВЫПОТ
- •СИНДРОМ ГОРНЕРА
- •БЛОКАДА ДИАФРАГМАЛЬНОГО НЕРВА
- •ПРОТИВОПОКАЗАНИЯ
- •ЗАКЛЮЧЕНИЕ
- •АНАТОМИЯ
- •МЕХАНИЗМ ДЕЙСТВИЯ
- •МЕТОДИКА
- •Положение пациента и ориентиры
- •Выполнение
- •Варианты методики
- •ПРИМЕНЕНИЕ В КЛИНИКЕ
- •Пневмоторакс
- •Прокол твердой мозговой оболочки
- •Гипотензия
- •Повреждение сосудов
- •Повреждение нервов
- •ЗАКЛЮЧЕНИЕ
- •Список литературы
- •АНАТОМИЯ
- •МЕТОДИКА
- •Мониторинг и подготовка
- •Положение пациента и ориентиры
- •Выполнение процедуры
- •Околосрединный подход
- •Подход по средней линии
- •Контроль проникновения в эпидуральное пространство
- •Потеря сопротивления
- •Ощущение прокола желтой связки
- •Легкость введения катетера
- •Физиологические реакции
- •Выбор анальгетиков и их дозировка
- •Снижение артериального давления
- •Потребность миокарда в кислороде
- •ПРИМЕНЕНИЕ В КЛИНИКЕ
- •ОСЛОЖНЕНИЯ
- •Прокол твердой мозговой оболочки
- •Прокол вены
- •Парестезия
- •Задержка мочи
- •Тошнота
- •Седация
- •Гипотензия
- •Снижение сердечного резерва
- •ЗАКЛЮЧЕНИЕ
- •ЭПИДУРАЛЬНАЯ ГЕМАТОМА
- •Клинические признаки и патофизиология
- •Эпидуральная гематома после субарахноидальной пункции
- •Имеются явные факторы риска
- •Эпидуральная гематома после эпидуральной анестезии
- •ОРИЕНТИРЫ ДЛЯ КРИТИЧЕСКОГО РЕШИТЕЛЬНОГО АНАЛИЗА
- •Предоперационная оценка
- •Нестероидные противовоспалительные препараты
- •Ведение больного в операционном и послеоперационном периодах
- •Время полувыведения
- •Послеоперационный мониторинг
- •ЗАКЛЮЧЕНИЕ
- •Список литературы
- •ИСТОРИЧЕСКАЯ СПРАВКА
- •МЕХАНИЗМ ДЕЙСТВИЯ
- •ТЕХНИЧЕСКИЕ АСПЕКТЫ
- •Продолжительность импульса
- •Постоянный поток или постоянный вольтаж
- •Форма волн
- •Частотность
- •Амплитуда
- •Установка электродов и множественные каналы стимуляции
- •Электроды
- •Сроки стимуляции
- •Побочное действие
- •Противопоказания
- •Методологические аспекты
- •Абдоминальная хирургия
- •ЧЭСН
- •Ортопедичесчик операции
- •Кардиоторакальная хирургия
- •Разные операции
- •Кардиоторакальные операции
- •Различные операции
- •Ортопедические операции
- •Акушерские операции
- •Операции на сердце и на органах грудной клетки
- •Состояние после ампутации
- •ЗАКЛЮЧЕНИЕ
- •Обучение
- •Гипноз
- •Введение в транс
- •Погружение в транс
- •Гипнотическая работа
- •Завершение
- •Релаксационная реакция
- •Достижение релаксационной реакции
- •ЗАКЛЮЧЕНИЕ
- •ПРЕДОПЕРАЦИОННЫЕ ФАКТОРЫ И ПОДГОТОВКА
- •ОЦЕНКА СТЕПЕНИ ВЫРАЖЕННОСТИ БОЛИ
- •Боль у ребенка, не умеющего говорить
- •Оценка степени боли
- •Неопиоиды
- •Опиоиды
- •Опиоиды
- •Внутримышечное введение
- •Интермиттирующее внутривенное введение опиоидов
- •Продолжительное внутривенное введение опиоидов
- •Региональная анестезия/аналгезия
- •Каудальный блок
- •Эпидуральная аналгезия в поясничном и грудном отделах
- •Блокада подвздошно-пахового и подвздошно-подчревного нервов
- •Блокада дорсального нерва полового члена
- •Блокада бедренного и бокового кожного нервов бедра
- •Блокада отсека подвздошной фасции
- •Внутриплевральная региональная аналгезия
- •Инфильтрационная аналгезия операционной раны
- •ЗАКЛЮЧЕНИЕ
- •Внутривенное введение опиоидов
- •Эпидуральное введение опиоидов
- •Морфин
- •Субарахноидально
- •Меперидин
- •Фентанил
- •Суфентанил
- •Буторфанол
- •Бупренорфин
- •Сочетанное применение препаратов
- •Субарахноидальное введение опиоидов
- •Морфин
- •Фентанил
- •Суфентанил
- •Эпидуральное введение клофелина
- •АНАЛГЕЗИЯ ОПИОИДАМИ И ГРУДНОЕ ВСКАРМЛИВАНИЕ
- •ВЫБОР АНАЛГЕЗИИ ПОСЛЕ КЕСАРЕВА СЕЧЕНИЯ
- •Список литературы
- •Артропластика и протезирование тазобедренного сустава
- •Осложнения, % в группе
- •Тазобедренный сустав
- •Субарахноидальное введение опиоидов
- •Эпидуральное введение опиоидов и локальных анестетиков
- •Тазобедренный сустав
- •Коленный сустав
- •Оба сустава
- •Операции со вскрытием коленного сустава
- •Общее назначение опиоидов
- •Субарахноидальное введение опиоидов
- •Эпидуральное введение опиоидов
- •Эпидуральное введение локального анестетика
- •Комбинированная аналгезия
- •Невральная блокада поясничного сплетения
- •Внутрисуставное введение морфина
- •Блокада плечевого сплетения
- •Эпидуральная анестезия/аналгезия в области шеи
- •Ампутация
- •Открытое вправление и внутренняя фиксация переломов лодыжки
- •Невральная блокада седалищного нерва в подколенной области
- •ЗАКЛЮЧЕНИЕ
- •Межреберная невральная блокада
- •Внутриплевральная региональная аналгезия
- •Паравертебральная невральная блокада
- •Криоаналгезия
- •Чрескожная электростимуляция нерва
- •Субарахноидальное введение опиоидов
- •Эпидуралыюе введение локальных анестетиков и опиоидов
- •Введение локальных анестетиков
- •Введение опиоидов
- •Установка эпидурального катетера в грудном или поясничном отделе
- •Комбинированное применение локальных анестетиков и опиоидов
- •Влияние на дыхание
- •ОСОБЫЕ ПРОБЛЕМЫ АНАЛГЕЗИИ ПОСЛЕ ТОРАКОТОМИИ
- •ЗАКЛЮЧЕНИЕ
- •Сенсибилизация ноцицепторов
- •Глубокая соматическая боль
- •Трансмиссия
- •Иррадиирующая боль
- •Предполагаемые механизмы иррадиирующей боли
- •Последовательные рефлекторные реакции
- •Кортикальные реакции
- •Нарушения функции легких
- •Осложнения со стороны желудочно-кишечного тракта
- •Тромбоэмболия
- •Аналгезия, контролируемая пациентом
- •Межреберная невральная блокада
- •Внутриплевральная региональная аналгезия
- •Аналгезия при ВПА
- •Субарахноидальное введение опиоидов
- •Эпидуральное введение локальных анестетиков и опиоидов
- •Операции на нижнем отделе брюшной полости
- •Аппендэктомия
- •Операции на толстом кишечнике
- •Опорожнение желудка и подвижность тонкого кишечника
- •Моторика толстого кишечника
- •ЗАКЛЮЧЕНИЕ
- •ДВА МНЕНИЯ: АНАЛГЕЗИЯ ПРОТИВ ДИАГНОСТИКИ
- •ФИЗИОЛОГИЧЕСКИЕ НАРУШЕНИЯ, СВЯЗАННЫЕ С ТРАВМОЙ
- •Региональная анестезия/аналгезия
- •Подкожная инфильтрационная анестезия
- •Бупивакаин
- •Фоновая блокада
- •Периферическая невральная блокада
- •Блокада сплетения
- •Внутриплевральная региональная аналгезия
- •Эпидуральная аналгезия
- •Субарахноидальная аналгезия
- •ТРАВМЫ ГОЛОВЫ
- •ТРАВМЫ ГРУДНОЙ КЛЕТКИ
- •ПОВРЕЖДЕНИЯ СКЕЛЕТА
- •ЗАКЛЮЧЕНИЕ
- •КОММУНИКАЦИЯ
- •ВРАЧЕБНЫЙ ВКЛАД
- •КОНЦЕПЦИЯ «ГЛОБАЛЬНОГО ГОНОРАРА»
- •Администрация госпиталей
- •Приобретение оборудования
- •Маркетинг
- •ЗАКЛЮЧЕНИЕ
- •Цели
- •Группа задач, связанных с АКП
- •Распределение препаратов
- •Участие медицинских сестер в переориентировке целей
- •Доза АКП, мг
- •Объекты проведения целевых усилии
- •АЛЬТЕРНАТИВНЫЕ МЕТОДЫ КОНТРОЛЯ БОЛИ
- •Поза, позиционная установка
- •Сон, релаксация
- •Тошнота, рвота
- •Стимуляция активности пациента
- •Психологический статус
- •Дополнительные медикаментозные назначения
- •ЗАКЛЮЧЕНИЕ
- •АНАЛГЕЗИЯ, КОНТРОЛИРУЕМАЯ ПАЦИЕНТОМ
- •Аналгезия, контролируемая пациентом
- •Общие указания
- •Обучение пациента/родственников
- •ПЕРСОНАЛЬНЫЙ ФАКТОР
- •Анестезиолог
- •Сестринская помощь
- •Фармакологическая служба
- •ОБОРУДОВАНИЕ
- •Простота и легкость в обращении
- •Ограничитель скорости потока
- •Приборы для эпидуральной инфузии
- •Вход для инъекций
- •Безопасность
- •Мониторы
- •ПРОЦЕДУРЫ, ПРОВОДИМЫЕ СЛУЖБОЙ ОСТРОЙ БОЛИ
- •Документация
- •ПРОБЛЕМЫ, СТОЯЩИЕ ПЕРЕД СЛУЖБОЙ ОСТРОЙ БОЛИ
- •Проблемы, стоящие перед СОБ
- •МОЛЕКУЛЯРНАЯ ФАРМАКОЛОГИЯ
- •Нейроэндокринная система
- •Сердечно-сосудистая система
- •Дыхательная система
- •Почки
- •Пищеварительная система
- •Центральная нервная система
- •МЕХАНИЗМ АНАЛГЕЗИИ
- •Нейроэндокринные
- •Сердечно-сосудистые
- •Респираторные
- •Желудочно-кишечные
- •Центральная нервная система
- •Эпидуральное назначение
- •Субарахноидальное введение
- •ЗАКЛЮЧЕНИЕ
Общее число наблюдений по внутривенной АКП у детей невелико, но предварительные клинические данные говорят об эффективности этого метода [66-70]. Дозы лекарственных средств, назначаемых при АКП, приведены в табл. 22-3. Внутривенная АКП у детей – это безопасный и эффективный метод, его предпочитают использовать персонал, родители и сами дети, особенно подростки (рис. 22-2). Тем не менее некоторые дети и подростки(хотя и нечасто) не желают пользоваться АКП и предпочитают получать анальгетики традиционными методами. Поэтому АКП нельзя считать универсальным методом преодоления боли после операций, и у пациентов, не чувствующих себя удовлетворенными АКП, нужно применять альтернативные методы обезболивания.
Внутривенную АКП можно назначать детям в возрасте7 лет и старше. Применение ее ограничено возрастом ребенка, который должен понимать цели этого метода и быть в состоянии активировать насос(мышечная слабость или иммобилизация могут препятствовать этому). В последнем случае работу с инфузором иногда доверяют родителям (аналгезия, контролируемая родителями) [68]. Безопасность и эффективность подобного метода еще предстоит уточнить.
Необходимы дальнейшие исследования по сопоставлению эффективности и безопасности АКП у детей и ее преимуществ перед обычно применяемыми методами послеоперационной аналгезии, прежде всего в сравнении с продолжительной внутривенной инфузией опиоидов и с методами региональной анестезии/аналгезии.
Региональная анестезия/аналгезия
Опиоиды очень просты в применении, стоимость их невелика, поэтому они нашли широкое применение в клинике для обезболивания. Однако правильное использование методов региональной анестезии/аналгезии обеспечивает более совершенное обезболивание, особенно после некоторых операций.
Невральная блокада вызывает надежную аналгезию, не сопряженную с опасностью седации и угнетения дыхания. При сочетании региональной и общей анестезии адекватная глубина наркоза обеспечивается во время операции гораздо меньшим количеством ингаляционного анестетика. Благодаря этому после операции быстрее восстанавливается нормальное дыхание и возвращается сознание. Облегчается ранний контакт между ребенком и родителями. Кроме того, невральную блокаду применяют в большинстве случаев операций, выполняемых в амбулаторных условиях [71].
Показанием к невральной блокаде чаще всего служит необходимость длительного обезболивания в послеоперационном периоде. Помимо того, что при региональной аналгезии отпадает необходимость в опиоидах, облегчается сотрудничество с ребенком во время налаживания глубокого и эффективного дыхания, при его переодевании и движениях. Регионарная анесте-
зия/аналгезия также обеспечивает большее удобство после - рекон руктивных операций, сложных пластических операций, вмешательств по поводу врожденных аномалий в нижних отделах желудочно-кишечного тракта и мочевых путей(например, клоакальная пластика, незаращение мочевого пузыря), а также при необходимости послеоперационной иммобилизации или вытяжения конечности.
Все методы региональной анестезии, применяемые у взрослых, могут быть безопасно и эффективно использованы и у детей. Более детальное описание анатомии, физиологии и техники проведения невральной блокады в педиатрии можно найти в ряде последних публикаций [72, 73].
Каудальный блок
Каудальная анестезия/аналгезия относится к наиболее широко применяемому методу невральной блокады при устранении послеоперационной боли у детей. Ее используют при самых различных операциях на нижнем отделе брюшной полости, на промежности и на нижних конечностях. Накопившиеся клинические наблюдения подтверждают, что каудальная анестезия/аналгезия проста в выполнении, надежна и безопасна [74-78].
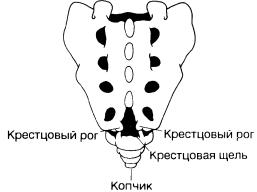
Анатомия. Крестец формируется в результате срастания пяти крестцовых позвонков (рис. 22-3). Однако это слияние неполное, поскольку сохраняется крестцовая щель в результате неполного срастания пластинSV и частично SIV по средней линии. Размеры этого дефекта различны, а по форме он напоминает перевернутые литеры U или V [79, 80]. С каждой стороны крестцовой щели находится крестцовый рог-рудимент суставных отростков. Эти рога служат важным ориентиром при идентификации крестцовой щели и выполнении процедур. Сверху крестцовая щель прикрыта толстой крестцовокопчиковой связкой. После прокола этой связки игла получает прямой доступ в каудальный отдел эпидурального пространства, поскольку сама крестцовая щель является каудальным концом спинномозгового канала. Таким образом, каудальная анестезия/аналгезия по своей сути является одним из методов эпидурального обезболивания. Твердая мозговая оболочка заканчивается на уровне SII, и введение иглы очень глубоко в каудальное эпидуральное пространство может привести к ее проколу.
Рис. 22-3. Крестец формируется при слиянии пяти крестцовых позвонков.
Неполное зарастание пластины SV и частично SIV по средней линии приводит к образованию костного дефектакрестцовой щели. Остатки нижнего суставного отростка SV (крестцовые рога) ограничивают крестцовую щель с обеих сторон.
Установка и ориентиры. Каудальную анестезию/аналгезию очень легко выполняют у детей. Маленьким детям обычно вводят легкий общий анестетик, облегчающий подготовку пациента и выполнение манипуляции.
Необходимость в общем анестетике зависит от возраста ребенка; например, подросткам достаточно назначить седативные препараты.
Пациента укладывают в боковом положении ничком или в положении сгибания с коленями, прижатыми к груди. В первом из этих положений, боковом, нога, находящаяся снизу, слегка согнута в тазобедренном суставе, а верхняя согнута еще сильнее. Преимуществами этого положения является большее удобство для пациента и для работы анестезиолога, а также легкость доступа к дыхательным путям.
В положении ничком под тазовую область пациента подкладывают подушку, а обе ноги ротируют так, чтобы большие пальцы стоп были направлены внутрь. При этом расслабляются ягодичные мышцы и подчеркивается борозда между ягодицами. Недостатком этого положения является затрудненность доступа к дыхательным путям.
Последнее положение с коленями, прижатыми к груди, менее популярно в педиатрии, но применяется, например, у беременных женщин.
Методика выполнения. Кожу очищают и обрабатывают, ориентируясь по костным образованиям. Пациента укладывают, как при проведении люмбальной эпидуральной пункции. Точное определение костных ориентиров служит основным условием успешного выполнения региональной анестезии. У большинства детей выступающие крестцовые рога хорошо определяются и без пальпации. Между рогами видно небольшое углубление крестцовой щели. Если эти ориентиры видны нечетко, то прощупывают копчик и концом пальца скользят кверху, пока не попадают в углубление крестцовой щели с крестцовыми рогами по бокам.

Рис. 22-4. Игла калибра 23 или 25 вводится в крестцовую щель под углом 45 . Прокалывание крестцово-копчиковои связки сопровождается характерным ощущением «хлопка».
Для однократной инъекции используют иглы калибра23-25, длиной 2– 3 см. У детей более старшего возраста предпочтительно пользоваться более прочными иглами калибра 22. Некоторые врачи охотнее применяют чрезыгольные катетеры, обычно используемые для внутривенных инфузий[81]. Если просвет иглы позволяет, через нее можно вводить эпидуральный катетер. Точно так же можно применять детские эпидуральные иглы для установки эпидурального катетера с целью продолжительной инфузии.
Кожу над крестцовой щелью инфильтрируют раствором местного анестетика. Иглу вводят под углом45 град. к поверхности крестцовокопчиковои связки (рис. 22-4), продвигая ее затем вглубь. Прохождение иглы через связки сопровождается характерным ощущением«хлопка». Концом иглы нащупывают переднюю стенку крестцового канала, после чего иглу слегка подтягивают таким образом, чтобы ее конец находился на уровне средней линии спинномозгового канала (рис. 22-5). После этого иглу продвигают в спинномозговой канал на глубину 2-5 мм.
До введения анальгетика следует получить подтверждение правильного положения иглы. Для этого снова проверяют костные ориентиры. При аспирации в шприц не должны поступать ни ликвор, ни кровь, ни воздух. Возможно небольшое кровянистое подкрашивание, так как крестцовый канал обильно васкуляризирован. Через иглу быстро вводят несколько миллилитров физиологического раствора. Если при этом над местом расположения конца иглы появляется припухлость, то это указывает на неправильное положение иглы, конец который находится дорсальное крестца в подкожной клетчатке. В этом случае иглу извлекают, и манипуляцию начинают заново.

Рис. 22-5. После прохождения крестцово-копчиковои связки конец иглы соприкасается с передней стенкой крестцового канала. Иглу последовательно переориентируют в положение вдоль продольной оси крестцового канала.
Выбор локального анестетика и его дозировка. При обезболивании в послеоперационном периоде чаще всего выбирают бупивакаин, используя его способность при низкой концентрации на длительный срок избирательно блокировать сенсорные волокна. При общей дозе 2,5 мг/кг в крови достигается безопасная концентрация препарата, ниже токсического уровня [82]. Для увеличения продолжительности аналгезии используют адреналин в разведении 1:200 000. Наиболее пригоден для однократной каудальной инъекции 0,25% раствор бупивакаина, особенно если региональная аналгезия служит дополнением к общему наркозу [77]. Более низкие концентрации бупивакаина столь же эффективны при введении препарата в конце операции или с целью сохранить моторную функцию[83]. Увеличивать концентрацию до 0,3- 0,375% нецелесообразно [84]. Разработано несколько режимов дозировки локальных анестетиков, учитывающих возраст, массу тела пациента, расстоя-
ние от крестцовой щели до позвонка С , а также ориентированных на число
VII
сегментов, которые требуется блокировать [85-91]. В определенной степени эффективен метод калькуляции по формуле Такасаки для детей в возрасте до 7 лет [88]. Общая доза бупивакаина, рассчитанная по этой формуле, гораздо ниже максимально переносимых доз. Объем 0,25% бупивакаина, требующийся для аналгезии ниже уровня дерматома ТX, рассчитывается следующим образом:
Общий объем (мл) = 0,056•число сегментов•масса тела(кг) = 0,056 мл•12•масса тела (кг) = 0,672•масса тела (кг) == около 0,7 мл•масса тела (кг).
Armitage [76] предложил простой и легко запоминающийся способ расчета необходимого объема 0,25% раствора бупивакаина. Этот способ, оказавшийся эффективным в 98% случаев, заключается в следующем: для крестцовой
аналгезии вводят по 0,5 мг/кг, для нижнегрудной – 1 мл/кг, для среднегруд-
ной-1,25 мл/кг [91 а].
Продолжительность аналгезии. Средняя продолжительность -кау дальной аналгезии после однократного введения 0,25% бупивакаина в дозе 1 мл/кг с адреналином1 : 200000 в начале операции достигает5 ч [92]. По формуле Такасаки при однократном каудальном введении бупивакаина в начале операции расчетная продолжительность аналгезии составляет4–6 ч. По литературным данным, послеоперационное обезболивание было удовлетворительным в 85% случаев [88]. Продолжительная аналгезия может достигаться при каудальной инфузии опиоидов, локальных анестетиков и их комбинаций.
Каудальное введение морфина. Однократное каудальное введение морфина в дозе 0,1 мг/кг вызывает длительную аналгезию в послеоперационном периоде у детей старше1 года [92]. Эта доза обеспечивала обезболивание в течение 12 ч после ортопедических операций на нижних конечностях и после урологических операций. Однако такая же доза морфина при каудальном введении вызвала длительную и опасную для жизни гиповентиляцию у 1,5-годовалого ребенка после операции на половом члене[93]. Более низкие дозы морфина (0,033 мг/кг), назначаемые детям старше 1 года, были столь же эффективны и более безопасны. Правда, продолжительность аналгезии при таких сниженных дозах была короче(10 ± 3,3 ч против 13,3+4,7 ч при дозе 0,1 мг/кг) [94]. По рекомендации авторов, доза морфина 0,033 мг/кг может служить начальной дозой при каудальном введении. При необходимости длительной аналгезии эту дозу можно увеличить. После введения каждой дозы в течение не менее24 ч необходим тщательный монито-
ринг [94].
Побочное действие и осложнения. Истинную частоту побочных реак-
ций при каудальной анестезии/аналгезии установить трудно главным образом потому, что разные авторы по-разному определяют общую дозу анестетика и различно трактуют цель исследования. Однако большинство из них единодушны в том, что рвота в послеоперационном периоде при каудальной анестезии/аналгезии локальными анестетиками наблюдается менее, чем у 30% больных [95-97]. Это сопоставимо с частотой этого побочного /действия после каудальнего введения морфина[92]. У всех детей при использовании каудального метода (0,25% бупивакаина с адреналином 1 :200 000) отмечают небольшую слабость мышц. Задержки мочи или замедленного мочеиспускания после однократного каудального введения 0,25% бупивакаина не регистрировали. Среди других вероятных, но весьма редких осложнений возможны случайное введение анальгетиков в просвет сосуда, в область костного мозга, прокол твердой мозговой оболочки, а также невралгии и инфекция.
