
- •В.И. Вигдорович, с.В. Романцова, н.В. Шель, и.В. Зарапина
- •Оглавление
- •Предисловие
- •Часть I. Основы органической химии
- •Структура органических соединений
- •Теория строения органических соединений а.М. Бутлерова
- •Изомерия органических соединений
- •Индуктивный и мезомерный эффекты
- •Понятие о мезомерном эффекте
- •Типы реакций органических соединений. Понятие о механизме реакции
- •Типы реакций в органической химии
- •Направление и селективность химической реакции
- •Предельные (насыщенные) углеводороды
- •Изомерия алканов.Для алканов характерен один из видов структурной изомерии – изомерия углеродной цепи (строения углеродного скелета). Приведем примеры таких изомеров:
- •Физические свойства алканов
- •Физические характеристики некоторых нормальных углеводородов
- •Влияние разветвления молекул алканов на их физические характеристики
- •Химические свойства алканов
- •Некоторые отдельные представители
- •Экологическая характеристика алканов
- •Задачи по теме
- •Циклоалканы
- •Физические свойства циклоалканов
- •Получение циклоалканов
- •Химические свойства малых циклов
- •Применение циклоалканов
- •Экологическая оценка
- •Непредельные углеводороды Алкены (олефины)
- •Физические свойства олефинов
- •Получение олефиновых углеводородов
- •Химические свойства олефинов
- •Отдельные представители олефинов
- •Экологические характеристики
- •Задачи по теме
- •Алкадиены (диеновые углеводороды)
- •Методы получение диенов
- •Химические свойства диенов
- •Каучуки
- •Экологическая характеристика
- •Задачи по теме
- •Алкины (ацетиленовые углеводороды)
- •Методы получения алкинов
- •Физические свойства алкинов
- •Химические свойства алкинов
- •Экологическая характеристика
- •Задачи по теме
- •Предельные спирты
- •Предельные одноатомные спирты
- •Получение одноатомных спиртов
- •Физические свойства первичных спиртов
- •Химические свойства одноатомных спиртов
- •Отдельные представители
- •Предельные многоатомные спирты
- •Получение двухатомных спиртов
- •Получение трехатомных спиртов
- •Физические свойства многоатомных спиртов
- •Химические свойства многоатомных спиртов
- •Экологическая характеристика
- •Задачи по теме
- •Предельные оксосоединения
- •Альдегиды
- •Получение альдегидов
- •Физические свойства альдегидов
- •Химические свойства альдегидов
- •Отдельные представители
- •Экологическая характеристика
- •Получение кетонов
- •Химические свойства кетонов
- •Отдельные представители
- •Задачи по теме
- •Карбоновые кислоты
- •Электронное строение карбоксильной группы
- •Предельные карбоновые кислоты
- •Физические свойства кислот
- •Получение карбоновых кислот
- •Химические свойства карбоновых кислот
- •Свойства отдельных представителей гомологического ряда
- •Задачи по теме
- •Азотсодержащие органические соединения
- •Нитросоединения
- •Нитрилы и изоцианиды
- •Алифатические амины
- •Физические свойства аминов
- •Получение аминов
- •Химические свойства аминов
- •Отдельные представители
- •Экологическая характеристика
- •Задачи по теме
- •Аминокислоты
- •Физические свойства α-аминокислот
- •Способы получения -аминокислот
- •Способы получения -аминокислот
- •Химические свойства аминокислот
- •Отдельные представители
- •Простые и сложные эфиры Простые эфиры
- •Способы получения простых эфиров
- •Физические свойства простых эфиров
- •Химические свойства простых эфиров
- •Отдельные представители
- •Сложные эфиры карбоновых кислот Получение сложных эфиров карбоновых кислот
- •Химические свойства эфиров карбоновых кислот
- •Физические свойства жиров
- •Химические свойства жиров
- •Сложные липиды
- •Ароматические углеводороды, арены Бензол и его производные
- •Методы получения бензола и его гомологов
- •Получение гомологов бензола
- •Физические свойства аренов
- •Химические свойства
- •Экологиченские характеристики
- •Ароматические оксосоединения Фенолы
- •Некоторые физические и термодинамические характеристики ряда фенолов
- •Получение фенола
- •Некоторые химические свойства фенола
- •Задачи по теме
- •Гетероциклические соединения
- •Пятичленные гетероциклы с одним гетероатомом
- •Химические свойства пиридина
- •Диоксины
- •Физико-химические свойства ксенобиотиков типа диоксинов
- •Источники ксенобиотиков
- •Пестициды
- •Фуллерены. Синтез и свойства соединений на их основе
- •Методы получения гидридов фуллеренов
- •Кислотность фуллеренов
- •Применение фуллеренов
- •Высокомолекулярные соединения
- •Свойства высокомолекулярных соединений
- •Основные химические реакции высокомолекулярных соединений
- •Часть II основы химической термодинамики
- •Понятия и термины химической термодинамики
- •Внутренняя энергия
- •Первое началотермодинамики
- •Следствия из первого начала термодинамики
- •Теплоемкость при постоянном объеме, сv
- •Теплоемкость при постоянном давлении
- •Равновесные процессы. Максимальная работа
- •Термохимия
- •Закон Гесса
- •Следствия из закона Гесса
- •И окончательно
- •Связь h и u химических реакций
- •Зависимость тепловых эффектов от температуры. Закон Кирхгофа
- •Совершенно очевидно, что разности Сi можно выразить через уравнение
- •Средняя теплоемкость
- •Работа тепловой машины. Теорема и цикл Карно
- •Второе начало термодинамики
- •Энтропия как критерий самопроизвольного течения процесса
- •Следовательно, если такой процесс протекает в изолированной системе, то
- •Расчет энтропии
- •Расчет изменения энтропии идеального газа
- •Задачи для самостоятельного решения
- •Принцип локального равновесия
- •Важно найти функции, определяющие зависимость deSиdiSот экспериментально измеряемых величин.
- •Статистическая интерпретация энтропии
- •Химический потенциал и химическое сродство
- •Химический потенциал
- •Химическое сродство
- •Уравнение Клапейрона-Клаузиуса
- •Термодинамические потенциалы
- •Свободная энергия Гиббса
- •Для чистого вещества
- •Условия самопроизвольного протекания процесса
- •Уравнение Гиббса-Гельмгольца
- •Тепловая теорема Нернста. Третий закон термодинамики
- •Некоторые аспекты, связанные с достижением химического равновесия
- •Изотерма химической реакции
- •Изобара химической реакции
- •Задачи для самостоятельного решения
- •Задача 7.Для реакции
- •Задача 8.Для реакции
- •Задача 10.Для реакции
- •Задача 11. Для реакции
- •Литература Основная литература
- •Дополнительная литература
Тепловая теорема Нернста. Третий закон термодинамики
При изложении химической термодинамики мы постоянно старались проводить мысль о том, что этот раздел науки не является чем-то застывшим. Напротив, он постоянно развивается во времени. В качестве одного из доказательств этого указывалось на создание теории неравновесной термодинамики, за что И.Р. Пригожин, бельгийский ученый с русскими корнями получил в 1947 г. нобелевскую премию – высшую награду мирового сообщества ученых.
Пригожин Илья Романович (родился 25 января 1917 в Москве). Бельгийский химик и физико-химик, с 1953 г. член Королевской бельгийской академии наук, литературы и изящных искусств. В 1969 г. становится ее президентом.
Илья Романович окончил Брюссельский университет, с 1962 г. директор Международного института физики и химии в Сольве, с 1967 г. директор научно-исследовательского центра по статистической механике и термодинамике в Техасском университете, г. Остин, США.
Работы И.Р. Пригожина посвящены термодинамике и статистической механике необратимых процессов. Развил представления об устойчивости состояний систем, далеких от равновесия. Заложил основы теории, согласно которой наряду с равновесными структурами в природе имеют место диссипативные структуры, возникающие в системах, далеких от равновесия и существующих благодаря обмену энергией и веществом с окружающей средой. Иностранный член АН СССР.
Другим более ранним доказательством того, что термодинамика как некий живой организм, постоянно развивается, явились работы В. Нернста и М. Планка.
Дело в том, что ранее указывалось на возможность расчетов S различных процессов, но ничего не говорилось о расчетах абсолютной величины энтропии вещества, чего невозможно сделать на базе двух рассмотренных выше начал термодинамики. Кроме того, химиков всего мира постоянно интересовала возможность разработки расчетных методов оценки возможности самопроизвольного течения химических реакций без знания, точнее без экспериментального определения термодинамических величин веществ при конкретных условиях, например, при принятых за стандартные.
В XIX в Бертло постулировал, что реально могут протекать только экзотермические реакции. Тем самым этот постулат вообще отрицал возможность протекания эндотермических реакций, идущих с поглощением теплоты. А, между тем, экспериментально показано, что таких процессов великое множество. Теперь читатели книги знают, что критерием самопроизвольного течения процесса является характер изменения энтропии, либо свободных энергий Гельмгольца или Гиббса, но никак не знак Н.
Однако, с другой стороны, напомним читателю ранее приведенное уравнение
G = H – TS,
из которого естественным образом вытекает зависимость
H = G + TS.
А теперь представим себе, что при некоторых условиях величина произведения TS стала равной нулю или точнее очень близка к нему.
Это возможно при очень низких температурах, если, конечно, с понижением температуры адекватно не возрастает изменение энтропии (А то вообще можно прийти к некоторым условиям, когда TS = const). Если же произведение TS мало, то
H G
и H действительно становится критерием самопроизвольного течения процесса.
Естественно, с учетом сказанного встал вопрос об изучении характера изменения теплоемкости с температурой, так как от величины Ср зависит вычисляемое значение S.
Оказалось, что со снижением температуры уменьшаются величины Ср и соответственно S. Можно было предположить, что при Т = 0 К произведение TS также равно нулю. Тогда становится абсолютно справедливым и принцип Бертло. Если это так, то зависимости H = f(T) и G = f(T) должны иметь одну общую точку при Т = 0. Но если ход кривой, характеризующей H = f(T), можно получить экспериментально, то для зависимости G = f(T) имеет место неопределенность, графически выражаемая в виде множества пунктирных кривых (рис. 23).
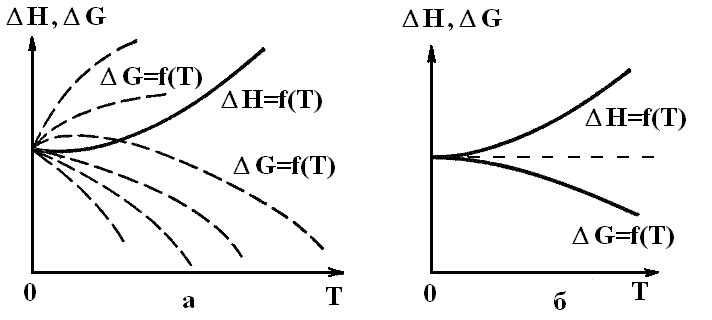
Рис. 23. Возможные виды зависимостей H = f(T) и G = f(T); а – без использования тепловой теоремы Нернста, б – с ее использованием.
Решить задачу уточнения хода зависимости G = f(T) первое и второе начала термодинамики не позволяют. Тогда Вальтер Нернст постулировал, что зависимости H = f(T) и G = f(T) имеют не только общую точку (рис. 23 а), но и общую касательную (рис. 23 б). Иначе говоря,
![]() . (51)
. (51)
Из равенства (51) вытекает, что:
![]() ,
,
иначе говоря, касательная с нулевым тангенсом угла наклона параллельна оси абсцисс (рис. 23б). Это обусловлено следующим. Согласно уравнению Гиббса-Гельмгольца,
![]() .
.
Но, если при Т = 0 К, G = H, то имеем
![]() .
.
Раскрывая эту неопределенность по правилу Лопиталя, получим
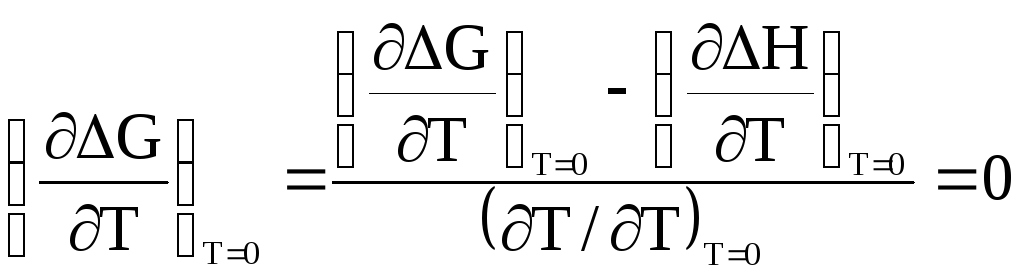 .
.
Следовательно, справедлив случай, показанный на рис. 17.
А теперь, вспомним, что, согласно закону Кирхгофа,
![]() ,
,
где Ср – разность интегральных теплоемкостей продуктов реакции и исходных веществ. Тогда
![]() .
.
Далее было показано и принято, что нулю равны при Т = 0 и сами теплоемкости веществ, то есть
![]() . (52)
. (52)
Но
![]() ,
что было показано нами ранее. Тогда
,
что было показано нами ранее. Тогда
![]() . (53)
. (53)
Отсюда следует, что при любом химическом процессе и Т = 0 энтропия остается постоянной. Этот постулат получил название Тепловой теоремы Нернста. Ее математическая формулировка выражается уравнениями (52) и (53).
В 1912 г. М. Планк уточнил этот постулат, что тем самым позволило, с учетом 1-го и 2-го начал термодинамики, рассчитать абсолютное значение энтропии и решить проблему химического равновесия, о котором речь пойдет дальше. Формулируется постулат М. Планка следующим образом. Энтропия любого индивидуального вещества в состоянии идеального кристалла при абсолютном нуле равна нулю.
S0 =0.
Теперь S = S2 – S1 и при S1 = 0, S = S2.
Таким образом, появилась точка отсчета, от которой легко рассчитать величину S, тем более, что она вообще равна 0. При этом нет нужды в оговорке «идеальный кристалл», так как при Т = 0 устойчиво только это состояние. Такой подход является частичным подтверждением правильности уравнения Больцмана, связывающее величину S с числом микросостояний системы
S0 =kln1; S0 =0,
хотя как указывалось выше, есть и несоответствия.
Теперь величина абсолютной энтропии любого вещества может быть вычислена при произвольно выбранной температуре Т. С этой целью следует начать отсчет от Т = 0 и в уравнении (54) взять первый его интеграл в пределах
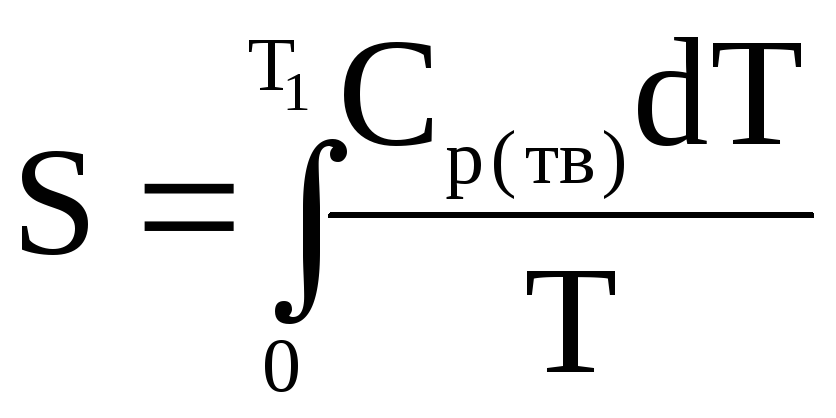 , (54)
, (54)
где Т – температура, начиная с которой известна Ср вещества. Этот интеграл рассчитывают графическим интегрированием (нахождением площади под кривой) экстраполированной к Т = 0 экспериментальной кривой. Следующий интеграл берут в пределах:
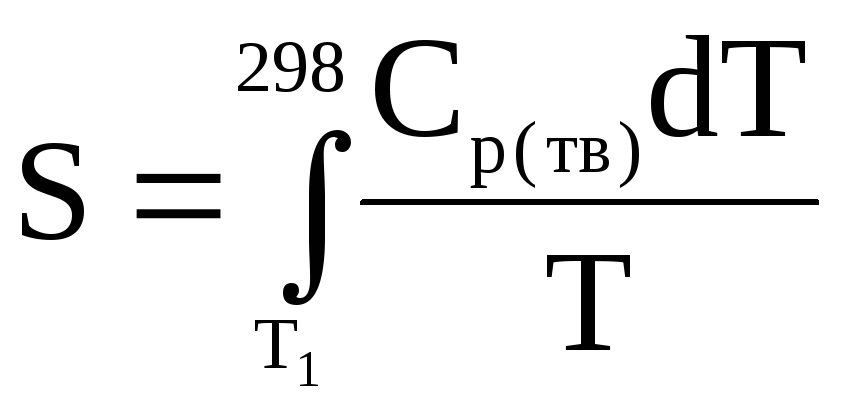 ,
,
если температура плавления рассматриваемого вещества больше 298 К, или
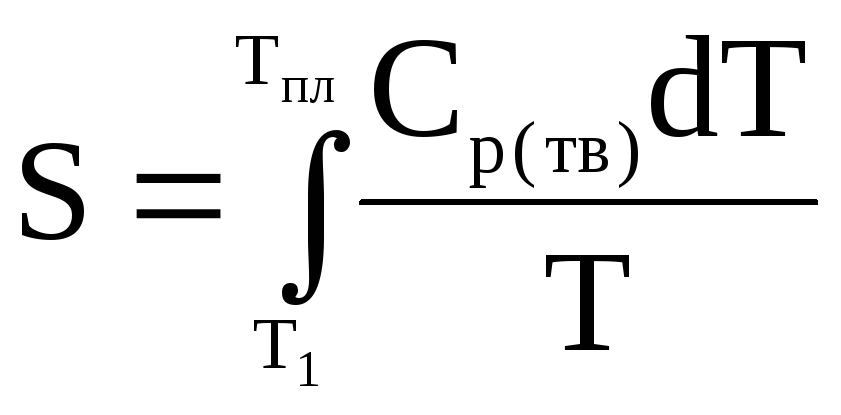 ,
,
если Тпл < 298 К.
