
- •В.И. Вигдорович, с.В. Романцова, н.В. Шель, и.В. Зарапина
- •Оглавление
- •Предисловие
- •Часть I. Основы органической химии
- •Структура органических соединений
- •Теория строения органических соединений а.М. Бутлерова
- •Изомерия органических соединений
- •Индуктивный и мезомерный эффекты
- •Понятие о мезомерном эффекте
- •Типы реакций органических соединений. Понятие о механизме реакции
- •Типы реакций в органической химии
- •Направление и селективность химической реакции
- •Предельные (насыщенные) углеводороды
- •Изомерия алканов.Для алканов характерен один из видов структурной изомерии – изомерия углеродной цепи (строения углеродного скелета). Приведем примеры таких изомеров:
- •Физические свойства алканов
- •Физические характеристики некоторых нормальных углеводородов
- •Влияние разветвления молекул алканов на их физические характеристики
- •Химические свойства алканов
- •Некоторые отдельные представители
- •Экологическая характеристика алканов
- •Задачи по теме
- •Циклоалканы
- •Физические свойства циклоалканов
- •Получение циклоалканов
- •Химические свойства малых циклов
- •Применение циклоалканов
- •Экологическая оценка
- •Непредельные углеводороды Алкены (олефины)
- •Физические свойства олефинов
- •Получение олефиновых углеводородов
- •Химические свойства олефинов
- •Отдельные представители олефинов
- •Экологические характеристики
- •Задачи по теме
- •Алкадиены (диеновые углеводороды)
- •Методы получение диенов
- •Химические свойства диенов
- •Каучуки
- •Экологическая характеристика
- •Задачи по теме
- •Алкины (ацетиленовые углеводороды)
- •Методы получения алкинов
- •Физические свойства алкинов
- •Химические свойства алкинов
- •Экологическая характеристика
- •Задачи по теме
- •Предельные спирты
- •Предельные одноатомные спирты
- •Получение одноатомных спиртов
- •Физические свойства первичных спиртов
- •Химические свойства одноатомных спиртов
- •Отдельные представители
- •Предельные многоатомные спирты
- •Получение двухатомных спиртов
- •Получение трехатомных спиртов
- •Физические свойства многоатомных спиртов
- •Химические свойства многоатомных спиртов
- •Экологическая характеристика
- •Задачи по теме
- •Предельные оксосоединения
- •Альдегиды
- •Получение альдегидов
- •Физические свойства альдегидов
- •Химические свойства альдегидов
- •Отдельные представители
- •Экологическая характеристика
- •Получение кетонов
- •Химические свойства кетонов
- •Отдельные представители
- •Задачи по теме
- •Карбоновые кислоты
- •Электронное строение карбоксильной группы
- •Предельные карбоновые кислоты
- •Физические свойства кислот
- •Получение карбоновых кислот
- •Химические свойства карбоновых кислот
- •Свойства отдельных представителей гомологического ряда
- •Задачи по теме
- •Азотсодержащие органические соединения
- •Нитросоединения
- •Нитрилы и изоцианиды
- •Алифатические амины
- •Физические свойства аминов
- •Получение аминов
- •Химические свойства аминов
- •Отдельные представители
- •Экологическая характеристика
- •Задачи по теме
- •Аминокислоты
- •Физические свойства α-аминокислот
- •Способы получения -аминокислот
- •Способы получения -аминокислот
- •Химические свойства аминокислот
- •Отдельные представители
- •Простые и сложные эфиры Простые эфиры
- •Способы получения простых эфиров
- •Физические свойства простых эфиров
- •Химические свойства простых эфиров
- •Отдельные представители
- •Сложные эфиры карбоновых кислот Получение сложных эфиров карбоновых кислот
- •Химические свойства эфиров карбоновых кислот
- •Физические свойства жиров
- •Химические свойства жиров
- •Сложные липиды
- •Ароматические углеводороды, арены Бензол и его производные
- •Методы получения бензола и его гомологов
- •Получение гомологов бензола
- •Физические свойства аренов
- •Химические свойства
- •Экологиченские характеристики
- •Ароматические оксосоединения Фенолы
- •Некоторые физические и термодинамические характеристики ряда фенолов
- •Получение фенола
- •Некоторые химические свойства фенола
- •Задачи по теме
- •Гетероциклические соединения
- •Пятичленные гетероциклы с одним гетероатомом
- •Химические свойства пиридина
- •Диоксины
- •Физико-химические свойства ксенобиотиков типа диоксинов
- •Источники ксенобиотиков
- •Пестициды
- •Фуллерены. Синтез и свойства соединений на их основе
- •Методы получения гидридов фуллеренов
- •Кислотность фуллеренов
- •Применение фуллеренов
- •Высокомолекулярные соединения
- •Свойства высокомолекулярных соединений
- •Основные химические реакции высокомолекулярных соединений
- •Часть II основы химической термодинамики
- •Понятия и термины химической термодинамики
- •Внутренняя энергия
- •Первое началотермодинамики
- •Следствия из первого начала термодинамики
- •Теплоемкость при постоянном объеме, сv
- •Теплоемкость при постоянном давлении
- •Равновесные процессы. Максимальная работа
- •Термохимия
- •Закон Гесса
- •Следствия из закона Гесса
- •И окончательно
- •Связь h и u химических реакций
- •Зависимость тепловых эффектов от температуры. Закон Кирхгофа
- •Совершенно очевидно, что разности Сi можно выразить через уравнение
- •Средняя теплоемкость
- •Работа тепловой машины. Теорема и цикл Карно
- •Второе начало термодинамики
- •Энтропия как критерий самопроизвольного течения процесса
- •Следовательно, если такой процесс протекает в изолированной системе, то
- •Расчет энтропии
- •Расчет изменения энтропии идеального газа
- •Задачи для самостоятельного решения
- •Принцип локального равновесия
- •Важно найти функции, определяющие зависимость deSиdiSот экспериментально измеряемых величин.
- •Статистическая интерпретация энтропии
- •Химический потенциал и химическое сродство
- •Химический потенциал
- •Химическое сродство
- •Уравнение Клапейрона-Клаузиуса
- •Термодинамические потенциалы
- •Свободная энергия Гиббса
- •Для чистого вещества
- •Условия самопроизвольного протекания процесса
- •Уравнение Гиббса-Гельмгольца
- •Тепловая теорема Нернста. Третий закон термодинамики
- •Некоторые аспекты, связанные с достижением химического равновесия
- •Изотерма химической реакции
- •Изобара химической реакции
- •Задачи для самостоятельного решения
- •Задача 7.Для реакции
- •Задача 8.Для реакции
- •Задача 10.Для реакции
- •Задача 11. Для реакции
- •Литература Основная литература
- •Дополнительная литература
Циклоалканы
Циклоалканы – предельные углеводороды, атомы которых замкнуты в цикл, с общей формулой гомологического ряда СnH2n. Первый член ряда – циклопропан (С3Н6). Различают малые циклы (Сn – 3…4), средние (Сn – 5…7) и макроциклы (Сn 8). Каждый атом углерода находится в состоянии sp3 – гибридизации и, следовательно, образует 4 одинарные -связи.
Ц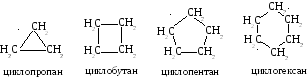 иклоалканы
(нафтеновые углеводороды) различаются
размерами цикла:
иклоалканы
(нафтеновые углеводороды) различаются
размерами цикла:
Номенклатура циклоалканов. Такие соединения называют еще алициклическими, под которыми понимают все карбоциклические соединения, включающие циклы углеродных атомов за исключением ароматических соединений (имеющих бензольное кольцо).
Ц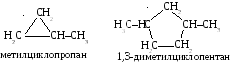 иклоалканы
различают по числу членов в цикле и
числу циклических группировок в
соединении. Соединение с одной такой
группировкой называют в соответствии
с общими правилами, при этом главной
считается цепь, образующая цикл. Перед
ее названием добавляется приставка
«цикло». Нумерацию углеродных атомов
проводят таким образом, чтобы сумма
номеров заместителей была наименьшей.
Номер одного заместителя не указывается.
иклоалканы
различают по числу членов в цикле и
числу циклических группировок в
соединении. Соединение с одной такой
группировкой называют в соответствии
с общими правилами, при этом главной
считается цепь, образующая цикл. Перед
ее названием добавляется приставка
«цикло». Нумерацию углеродных атомов
проводят таким образом, чтобы сумма
номеров заместителей была наименьшей.
Номер одного заместителя не указывается.
Строение циклоалканов. Первоначально считалось, что все атомы цикла расположены в одной плоскости. Тогда должны быть следующими углы между связями: 3-х членный цикл – 60, 4-х членный – 90, 5-ти членный – 108, 6-ти членный – 120. Вместе с тем, для цепей предельных углеродных атомов в отсутствии их возбуждения характерны так называемые тетраэдрические углы – 10928. Была высказана идея (Байер, 1885 г), что с ростом отклонения угла между С–С-связями от тетраэдрического растет напряженность и снижается устойчивость соединений, то есть повышается их химическая активность. За меру подобной напряженности цикла была предложена половина разности (10928фактический валентный угол)/2, которую обозначим через. Ниже показано, как величинасвязана с Сnв цикле:
|
n |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
|
2444 |
944 |
044 |
516 |
933 |
1246 |
3516 |
Таким образом, меньше всего напряжена молекула циклопентана, а наиболее – циклопропана. Действительно, кольцо С3Н6очень легко размыкается под действием галогенов и галогеноводоордов, а исходное соединение интенсивно каталитически гидрируется. Таким образом, прочность циклоалканов возрастает в ряду
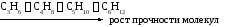
Более того, с n> 5 энергия всех циклоалканов примерно одинакова, что не соответствует указанному выше подходу.
Дело в том, что циклоалканы могут иметь различную пространственную структуру. Примером служит циклогексан, для которого возможны структуры: кресло и ванна (рис. 5).
Изомерия циклоалканов. Для подобных соединений возможна как структурная, так и пространственная изомерия:
1. Изомерия строения углеродного скелета может быть связана с различными причинами:
1а. С разной величиной цикла, например, для условной (эмпирической) молекулярной формулы С5Н10имеем:
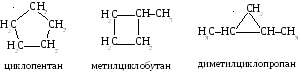
1б. Со строением боковых цепей.
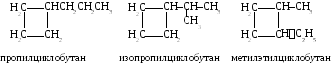
1в. С различным относительным положением в цикле. Покажем это на примере дизамещенного циклобутана (3 изомера).
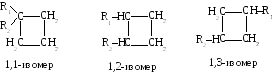
2. Стереоизомерия, возможная при наличии двух заместителей. Два заместителя, находящиеся в молекуле циклоалкана у различных атомов углерода, могут быть расположены:
– по одну сторону от плоскости цикла; такой дизамещённый циклоалкан называют цис-изомером;
– по разные стороны от плоскости цикла; такой дизамещённый циклоалкан называют транс-изомером.
