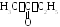- •В.И. Вигдорович, с.В. Романцова, н.В. Шель, и.В. Зарапина
- •Оглавление
- •Предисловие
- •Часть I. Основы органической химии
- •Структура органических соединений
- •Теория строения органических соединений а.М. Бутлерова
- •Изомерия органических соединений
- •Индуктивный и мезомерный эффекты
- •Понятие о мезомерном эффекте
- •Типы реакций органических соединений. Понятие о механизме реакции
- •Типы реакций в органической химии
- •Направление и селективность химической реакции
- •Предельные (насыщенные) углеводороды
- •Изомерия алканов.Для алканов характерен один из видов структурной изомерии – изомерия углеродной цепи (строения углеродного скелета). Приведем примеры таких изомеров:
- •Физические свойства алканов
- •Физические характеристики некоторых нормальных углеводородов
- •Влияние разветвления молекул алканов на их физические характеристики
- •Химические свойства алканов
- •Некоторые отдельные представители
- •Экологическая характеристика алканов
- •Задачи по теме
- •Циклоалканы
- •Физические свойства циклоалканов
- •Получение циклоалканов
- •Химические свойства малых циклов
- •Применение циклоалканов
- •Экологическая оценка
- •Непредельные углеводороды Алкены (олефины)
- •Физические свойства олефинов
- •Получение олефиновых углеводородов
- •Химические свойства олефинов
- •Отдельные представители олефинов
- •Экологические характеристики
- •Задачи по теме
- •Алкадиены (диеновые углеводороды)
- •Методы получение диенов
- •Химические свойства диенов
- •Каучуки
- •Экологическая характеристика
- •Задачи по теме
- •Алкины (ацетиленовые углеводороды)
- •Методы получения алкинов
- •Физические свойства алкинов
- •Химические свойства алкинов
- •Экологическая характеристика
- •Задачи по теме
- •Предельные спирты
- •Предельные одноатомные спирты
- •Получение одноатомных спиртов
- •Физические свойства первичных спиртов
- •Химические свойства одноатомных спиртов
- •Отдельные представители
- •Предельные многоатомные спирты
- •Получение двухатомных спиртов
- •Получение трехатомных спиртов
- •Физические свойства многоатомных спиртов
- •Химические свойства многоатомных спиртов
- •Экологическая характеристика
- •Задачи по теме
- •Предельные оксосоединения
- •Альдегиды
- •Получение альдегидов
- •Физические свойства альдегидов
- •Химические свойства альдегидов
- •Отдельные представители
- •Экологическая характеристика
- •Получение кетонов
- •Химические свойства кетонов
- •Отдельные представители
- •Задачи по теме
- •Карбоновые кислоты
- •Электронное строение карбоксильной группы
- •Предельные карбоновые кислоты
- •Физические свойства кислот
- •Получение карбоновых кислот
- •Химические свойства карбоновых кислот
- •Свойства отдельных представителей гомологического ряда
- •Задачи по теме
- •Азотсодержащие органические соединения
- •Нитросоединения
- •Нитрилы и изоцианиды
- •Алифатические амины
- •Физические свойства аминов
- •Получение аминов
- •Химические свойства аминов
- •Отдельные представители
- •Экологическая характеристика
- •Задачи по теме
- •Аминокислоты
- •Физические свойства α-аминокислот
- •Способы получения -аминокислот
- •Способы получения -аминокислот
- •Химические свойства аминокислот
- •Отдельные представители
- •Простые и сложные эфиры Простые эфиры
- •Способы получения простых эфиров
- •Физические свойства простых эфиров
- •Химические свойства простых эфиров
- •Отдельные представители
- •Сложные эфиры карбоновых кислот Получение сложных эфиров карбоновых кислот
- •Химические свойства эфиров карбоновых кислот
- •Физические свойства жиров
- •Химические свойства жиров
- •Сложные липиды
- •Ароматические углеводороды, арены Бензол и его производные
- •Методы получения бензола и его гомологов
- •Получение гомологов бензола
- •Физические свойства аренов
- •Химические свойства
- •Экологиченские характеристики
- •Ароматические оксосоединения Фенолы
- •Некоторые физические и термодинамические характеристики ряда фенолов
- •Получение фенола
- •Некоторые химические свойства фенола
- •Задачи по теме
- •Гетероциклические соединения
- •Пятичленные гетероциклы с одним гетероатомом
- •Химические свойства пиридина
- •Диоксины
- •Физико-химические свойства ксенобиотиков типа диоксинов
- •Источники ксенобиотиков
- •Пестициды
- •Фуллерены. Синтез и свойства соединений на их основе
- •Методы получения гидридов фуллеренов
- •Кислотность фуллеренов
- •Применение фуллеренов
- •Высокомолекулярные соединения
- •Свойства высокомолекулярных соединений
- •Основные химические реакции высокомолекулярных соединений
- •Часть II основы химической термодинамики
- •Понятия и термины химической термодинамики
- •Внутренняя энергия
- •Первое началотермодинамики
- •Следствия из первого начала термодинамики
- •Теплоемкость при постоянном объеме, сv
- •Теплоемкость при постоянном давлении
- •Равновесные процессы. Максимальная работа
- •Термохимия
- •Закон Гесса
- •Следствия из закона Гесса
- •И окончательно
- •Связь h и u химических реакций
- •Зависимость тепловых эффектов от температуры. Закон Кирхгофа
- •Совершенно очевидно, что разности Сi можно выразить через уравнение
- •Средняя теплоемкость
- •Работа тепловой машины. Теорема и цикл Карно
- •Второе начало термодинамики
- •Энтропия как критерий самопроизвольного течения процесса
- •Следовательно, если такой процесс протекает в изолированной системе, то
- •Расчет энтропии
- •Расчет изменения энтропии идеального газа
- •Задачи для самостоятельного решения
- •Принцип локального равновесия
- •Важно найти функции, определяющие зависимость deSиdiSот экспериментально измеряемых величин.
- •Статистическая интерпретация энтропии
- •Химический потенциал и химическое сродство
- •Химический потенциал
- •Химическое сродство
- •Уравнение Клапейрона-Клаузиуса
- •Термодинамические потенциалы
- •Свободная энергия Гиббса
- •Для чистого вещества
- •Условия самопроизвольного протекания процесса
- •Уравнение Гиббса-Гельмгольца
- •Тепловая теорема Нернста. Третий закон термодинамики
- •Некоторые аспекты, связанные с достижением химического равновесия
- •Изотерма химической реакции
- •Изобара химической реакции
- •Задачи для самостоятельного решения
- •Задача 7.Для реакции
- •Задача 8.Для реакции
- •Задача 10.Для реакции
- •Задача 11. Для реакции
- •Литература Основная литература
- •Дополнительная литература
Химические свойства альдегидов
1. Реакции присоединения (за счет разрыва двойной связи карбонильной группы).
1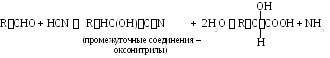 .1.
Присоединение синильной кислоты.
.1.
Присоединение синильной кислоты.
1.2. Присоединение водорода (гидрирование).
СН3СНО + Н2![]() СН3СН2ОН
СН3СН2ОН
1.3. Реакции конденсации.

2. Реакции замещения атома кислорода в карбонильной группе
2.1. Взаимодействие с гидроксиламином.
СН3СНО +NН2ОНСН3СН=NОH+ Н2O
оксим уксусного альдегида
2.2.Взаимодействие с гидразином (NН2NH2– компонент ракетного топлива).
СН3СНО +NН2NH2СН3СН=NNH2+ Н2O
гидразон уксусного альдегида
2.3. Взаимодействие с пентагалогенидом фосфора.
СН3СНО +PCl5СН3СНCl2+POCl3
оксотрихлорид фосфора
2 .4.
Взаимодействие со спиртами.
.4.
Взаимодействие со спиртами.
3. Реакции с участием атома водорода в -положении к карбонильной группе. Этот атом имеет повышенную реакционную способность.
Взаимодействие с галогенами.
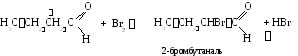
4. Окисление.
RCHO + [O] RCOOH
Реакция серебряного зеркала.
У прощенный
вариант записи:
прощенный
вариант записи:
RCHO + Ag2O RCOOH + 2Ag
Помимо альдегидов эта реакция характерна для муравьиной кислоты.
5 .
Взаимодействие с гидроксидом меди (II).
.
Взаимодействие с гидроксидом меди (II).
Реакции (4) и (5) используются как качественные на альдегиды.
6. Реакция полимеризации (для формальдегида).
nH2C=O [CH2O]n
Отдельные представители
Формальдегид (муравьиный альдегид) H2C=O. При обычных условиях газ с неприятным запахом, хорошо растворимый в Н2О. 40 %-ный раствор – формалин (консервант для погибших живых организмов). Используется для получения фенолформальдегидных смол, уротропина.

Уксусный (ацет)альдегид. Жидкость с резким неприятным запахом. Пары вызывают удушье. Хорошо растворим в воде и во многих органических растворителях. Используется для получения СН3СООН, С2Н5ОН, синтетических смол, производства пластмасс, синтетических волокон.
Экологическая характеристика
Метаналь оказывает наркотическое действие, раздражает слизистую оболочку глаз. С ростом nСв молекуле алльдегидов наркотическое действие усиливается, раздражающее – снижается. Непредельные альдегиды оказывают более сильное токсическое действие, чем предельные. Действие НСНО обусловлено, прежде всего, примесями СН3ОН. При СНСНО0,001 мг/л раздражение верхних дыхательных путей. Прием внутрь 100 … 200 мл 5 %-го формалина ведет к летальному исходу.
Ацетальдегид. Порог органолептического восприятия – 10–4мг/л, при 0,004 мг/л ощущение резкого запаха. Концентрация в 0,1 … 0.4 мг/л вызывает обратимое раздражение верхних дыхательных путей, слизистой оболочки глаз. Большие концентрации ведут к рвоте, учащению пульса, воспалению легких. ПДКр.з.= 5 мг/м3, ПДКв= 0,2 мг/л. Класс опасности – 3.
Пропаналь: ПДКр.з.= 5 мг/м3, БПК5= 1,13 мгО2/г в-ва, ХПК = 2,20 мгО2/г в-ва.
Кетоны
Физические свойства ряда соединений этого класса приведены в таблице 9. Название их заканчивается суффиксом «он». Модель молекулы диметилкетона показана на рис. 15.
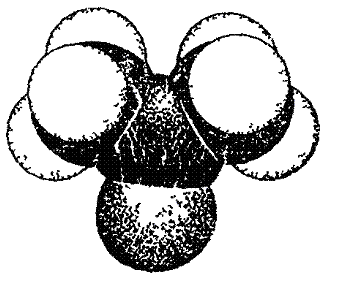
Рис. 15. Модель молекулы ацетона.
Таблица 9
Некоторые физические свойства простейших кетонов
|
Формула |
Название |
Тпл,С |
Ткип,С |
(дипольный момент), Дебай |
|
|
2-пропанон (ацетон) |
95,0 |
56,5 |
2,72 |
|
|
2-бутанон (метилэтилкетон) |
86,4 |
79,6 |
2,79 |
|
|
2-пентанон (метилпропилкетон) |
77,8 |
101,7 |
2,72 |
|
|
3-пентанон (диэтилкетон) |
42 |
102,7 |
2,72 |