- •В.И. Вигдорович, с.В. Романцова, н.В. Шель, и.В. Зарапина
- •Оглавление
- •Предисловие
- •Часть I. Основы органической химии
- •Структура органических соединений
- •Теория строения органических соединений а.М. Бутлерова
- •Изомерия органических соединений
- •Индуктивный и мезомерный эффекты
- •Понятие о мезомерном эффекте
- •Типы реакций органических соединений. Понятие о механизме реакции
- •Типы реакций в органической химии
- •Направление и селективность химической реакции
- •Предельные (насыщенные) углеводороды
- •Изомерия алканов.Для алканов характерен один из видов структурной изомерии – изомерия углеродной цепи (строения углеродного скелета). Приведем примеры таких изомеров:
- •Физические свойства алканов
- •Физические характеристики некоторых нормальных углеводородов
- •Влияние разветвления молекул алканов на их физические характеристики
- •Химические свойства алканов
- •Некоторые отдельные представители
- •Экологическая характеристика алканов
- •Задачи по теме
- •Циклоалканы
- •Физические свойства циклоалканов
- •Получение циклоалканов
- •Химические свойства малых циклов
- •Применение циклоалканов
- •Экологическая оценка
- •Непредельные углеводороды Алкены (олефины)
- •Физические свойства олефинов
- •Получение олефиновых углеводородов
- •Химические свойства олефинов
- •Отдельные представители олефинов
- •Экологические характеристики
- •Задачи по теме
- •Алкадиены (диеновые углеводороды)
- •Методы получение диенов
- •Химические свойства диенов
- •Каучуки
- •Экологическая характеристика
- •Задачи по теме
- •Алкины (ацетиленовые углеводороды)
- •Методы получения алкинов
- •Физические свойства алкинов
- •Химические свойства алкинов
- •Экологическая характеристика
- •Задачи по теме
- •Предельные спирты
- •Предельные одноатомные спирты
- •Получение одноатомных спиртов
- •Физические свойства первичных спиртов
- •Химические свойства одноатомных спиртов
- •Отдельные представители
- •Предельные многоатомные спирты
- •Получение двухатомных спиртов
- •Получение трехатомных спиртов
- •Физические свойства многоатомных спиртов
- •Химические свойства многоатомных спиртов
- •Экологическая характеристика
- •Задачи по теме
- •Предельные оксосоединения
- •Альдегиды
- •Получение альдегидов
- •Физические свойства альдегидов
- •Химические свойства альдегидов
- •Отдельные представители
- •Экологическая характеристика
- •Получение кетонов
- •Химические свойства кетонов
- •Отдельные представители
- •Задачи по теме
- •Карбоновые кислоты
- •Электронное строение карбоксильной группы
- •Предельные карбоновые кислоты
- •Физические свойства кислот
- •Получение карбоновых кислот
- •Химические свойства карбоновых кислот
- •Свойства отдельных представителей гомологического ряда
- •Задачи по теме
- •Азотсодержащие органические соединения
- •Нитросоединения
- •Нитрилы и изоцианиды
- •Алифатические амины
- •Физические свойства аминов
- •Получение аминов
- •Химические свойства аминов
- •Отдельные представители
- •Экологическая характеристика
- •Задачи по теме
- •Аминокислоты
- •Физические свойства α-аминокислот
- •Способы получения -аминокислот
- •Способы получения -аминокислот
- •Химические свойства аминокислот
- •Отдельные представители
- •Простые и сложные эфиры Простые эфиры
- •Способы получения простых эфиров
- •Физические свойства простых эфиров
- •Химические свойства простых эфиров
- •Отдельные представители
- •Сложные эфиры карбоновых кислот Получение сложных эфиров карбоновых кислот
- •Химические свойства эфиров карбоновых кислот
- •Физические свойства жиров
- •Химические свойства жиров
- •Сложные липиды
- •Ароматические углеводороды, арены Бензол и его производные
- •Методы получения бензола и его гомологов
- •Получение гомологов бензола
- •Физические свойства аренов
- •Химические свойства
- •Экологиченские характеристики
- •Ароматические оксосоединения Фенолы
- •Некоторые физические и термодинамические характеристики ряда фенолов
- •Получение фенола
- •Некоторые химические свойства фенола
- •Задачи по теме
- •Гетероциклические соединения
- •Пятичленные гетероциклы с одним гетероатомом
- •Химические свойства пиридина
- •Диоксины
- •Физико-химические свойства ксенобиотиков типа диоксинов
- •Источники ксенобиотиков
- •Пестициды
- •Фуллерены. Синтез и свойства соединений на их основе
- •Методы получения гидридов фуллеренов
- •Кислотность фуллеренов
- •Применение фуллеренов
- •Высокомолекулярные соединения
- •Свойства высокомолекулярных соединений
- •Основные химические реакции высокомолекулярных соединений
- •Часть II основы химической термодинамики
- •Понятия и термины химической термодинамики
- •Внутренняя энергия
- •Первое началотермодинамики
- •Следствия из первого начала термодинамики
- •Теплоемкость при постоянном объеме, сv
- •Теплоемкость при постоянном давлении
- •Равновесные процессы. Максимальная работа
- •Термохимия
- •Закон Гесса
- •Следствия из закона Гесса
- •И окончательно
- •Связь h и u химических реакций
- •Зависимость тепловых эффектов от температуры. Закон Кирхгофа
- •Совершенно очевидно, что разности Сi можно выразить через уравнение
- •Средняя теплоемкость
- •Работа тепловой машины. Теорема и цикл Карно
- •Второе начало термодинамики
- •Энтропия как критерий самопроизвольного течения процесса
- •Следовательно, если такой процесс протекает в изолированной системе, то
- •Расчет энтропии
- •Расчет изменения энтропии идеального газа
- •Задачи для самостоятельного решения
- •Принцип локального равновесия
- •Важно найти функции, определяющие зависимость deSиdiSот экспериментально измеряемых величин.
- •Статистическая интерпретация энтропии
- •Химический потенциал и химическое сродство
- •Химический потенциал
- •Химическое сродство
- •Уравнение Клапейрона-Клаузиуса
- •Термодинамические потенциалы
- •Свободная энергия Гиббса
- •Для чистого вещества
- •Условия самопроизвольного протекания процесса
- •Уравнение Гиббса-Гельмгольца
- •Тепловая теорема Нернста. Третий закон термодинамики
- •Некоторые аспекты, связанные с достижением химического равновесия
- •Изотерма химической реакции
- •Изобара химической реакции
- •Задачи для самостоятельного решения
- •Задача 7.Для реакции
- •Задача 8.Для реакции
- •Задача 10.Для реакции
- •Задача 11. Для реакции
- •Литература Основная литература
- •Дополнительная литература
Теория строения органических соединений а.М. Бутлерова
Современный подход к строению химических соединений вообще и органических, в частности, прошел длинный и сложный путь. Мы не будем рассматривать историю решения этого вопроса, проиллюстрируем лишь ниже, как изображали формулы химических соединений выдающиеся химики второй половины XIXвека, показав одновременно, насколько упростилось современное изображение молекулярных формул тех же соединений.
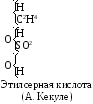
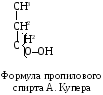
Понимание структуры органических соединений удалось достичь с помощью теории строения химических соединений Александра Михайловича Бутлерова, сформулированной и впервые им представленной в докладе «О теории химического строения» на Международном съезде естествоиспытателей в 1861 г.
Русский химик А.М. Бутлеров, с 1874 г академик Петербургской Академии Наук, родился 15 ноября 1828 г в городе Чистополе. В 1849 г окончил Казанский университет, где с 1857 г работал в должности профессора, а с 1863 г – его ректора. В 1868 г перешел на работу в Петербургский университет. А.М. Бутлеров – создатель теории химического строения органических соединений, лежащей в основе современной химии. Помимо этого он сделал в химии очень многое:
1. Открыл новый способ синтеза метиленйодида.
2. Синтезировал диацетат метилена и получил продукт его омыления – полимер формальдегида, а затем на основе его – гексаметилентетрамин (уротропин).
3. Предсказал и объяснил изомерию многих органических соединений, в частности, двух изомеров бутана, трех изомерных представителей пентана, различных спиртов и многое другое. Создал школу русских химиков (В.В. Марковников, А.М. Зайцев, Е.Е. Вагнер, А.Е. Фаворский и др.). Поборник высшего образования для женщин в России. Скончался ученый 17 августа 1886 г.
Основные положения теории химического строения А.М. Бутлерова следующие.
1. Атомы в молекулах соединены между собой в определенном порядке, согласно их валентности. Причем все валентности должны быть целиком затрачены на соединение атомов друг с другом.
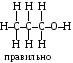

Благодаря этому положению удается полностью избежать хаоса в представлении молекулярных формул органических соединений.
2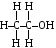 .
Свойства органических веществ зависят
не только от их качественного (элементного)
состава, но определяются и их строением.
Например, соединение С2Н6О
может быть этиловым спиртом
.
Свойства органических веществ зависят
не только от их качественного (элементного)
состава, но определяются и их строением.
Например, соединение С2Н6О
может быть этиловым спиртом
, для которого характерны все свойства одноатомных спир-
тов, не содержащих в молекулах ненасыщенных связей, Тпл= 114,15 °С, Ткип= 78,39 °С, смешивается с водой в любых отношениях
и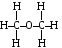 диметиловым эфиром
диметиловым эфиром
, с Тпл=138,5С, Ткип=23,65С. Веществом химически
инертным, не реагирующим с металлическим натрием, с сильными кислотами и щелочами при умеренных температурах.
3. Имеет место взаимное влияние атомов и функциональных групп в молекулах химических соединений. Например, атомы водорода и кислорода в гидроксильной группе этанола соединяются очень прочно, в результате чего этиловый спирт практически не обладает кислотными свойствами в водных растворах.
Замена этильного радикала –С2Н5на фенильный –С6Н5приводит к перераспределению электронной плотности в молекуле фенола С6Н5ОН, в результате чего на атоме водорода гидроксильной группы образуется больший частичный положительный заряд, чем в молекуле этанола, что увеличивает вероятность его отщепления в водном растворе. Фенол обладает хорошо выраженными в воде кислотными свойствами с константой диссоциации по уравнению
С6Н5ОН⇄ С6Н5О+ Н+,
равной 1010. Поэтому фенол по тривиальной номенклатуре называют карболовой кислотой.
Можно привести и другой пример. Бензол С6Н6с большим трудом вступает во взаимодействие по реакции замещения, лишь в жестких условиях (в присутствии катализаторов – безводныхAlCl3илиFeCl3).

В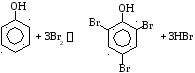 то же время взаимодействие фенола с
молекулярным бромом (бромной водой) по
реакции
то же время взаимодействие фенола с
молекулярным бромом (бромной водой) по
реакции
протекает очень легко с образованием 2,4,6-трибромфенола. В этом четко проявляется влияние ОН-группы на подвижность атомов водорода бензольного ядра.
4. Строение молекул может быть установлено посредством изучения химических свойств соединений. Например, их кислотные свойства целесообразно связать с наличием карбоксильной группы –СООН, способность к реакции серебряного зеркала – с присутствием в молекуле группы–СНО и т. д.,
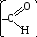
структура которых имеет вид: и .