
- •В.И. Вигдорович, с.В. Романцова, н.В. Шель, и.В. Зарапина
- •Оглавление
- •Предисловие
- •Часть I. Основы органической химии
- •Структура органических соединений
- •Теория строения органических соединений а.М. Бутлерова
- •Изомерия органических соединений
- •Индуктивный и мезомерный эффекты
- •Понятие о мезомерном эффекте
- •Типы реакций органических соединений. Понятие о механизме реакции
- •Типы реакций в органической химии
- •Направление и селективность химической реакции
- •Предельные (насыщенные) углеводороды
- •Изомерия алканов.Для алканов характерен один из видов структурной изомерии – изомерия углеродной цепи (строения углеродного скелета). Приведем примеры таких изомеров:
- •Физические свойства алканов
- •Физические характеристики некоторых нормальных углеводородов
- •Влияние разветвления молекул алканов на их физические характеристики
- •Химические свойства алканов
- •Некоторые отдельные представители
- •Экологическая характеристика алканов
- •Задачи по теме
- •Циклоалканы
- •Физические свойства циклоалканов
- •Получение циклоалканов
- •Химические свойства малых циклов
- •Применение циклоалканов
- •Экологическая оценка
- •Непредельные углеводороды Алкены (олефины)
- •Физические свойства олефинов
- •Получение олефиновых углеводородов
- •Химические свойства олефинов
- •Отдельные представители олефинов
- •Экологические характеристики
- •Задачи по теме
- •Алкадиены (диеновые углеводороды)
- •Методы получение диенов
- •Химические свойства диенов
- •Каучуки
- •Экологическая характеристика
- •Задачи по теме
- •Алкины (ацетиленовые углеводороды)
- •Методы получения алкинов
- •Физические свойства алкинов
- •Химические свойства алкинов
- •Экологическая характеристика
- •Задачи по теме
- •Предельные спирты
- •Предельные одноатомные спирты
- •Получение одноатомных спиртов
- •Физические свойства первичных спиртов
- •Химические свойства одноатомных спиртов
- •Отдельные представители
- •Предельные многоатомные спирты
- •Получение двухатомных спиртов
- •Получение трехатомных спиртов
- •Физические свойства многоатомных спиртов
- •Химические свойства многоатомных спиртов
- •Экологическая характеристика
- •Задачи по теме
- •Предельные оксосоединения
- •Альдегиды
- •Получение альдегидов
- •Физические свойства альдегидов
- •Химические свойства альдегидов
- •Отдельные представители
- •Экологическая характеристика
- •Получение кетонов
- •Химические свойства кетонов
- •Отдельные представители
- •Задачи по теме
- •Карбоновые кислоты
- •Электронное строение карбоксильной группы
- •Предельные карбоновые кислоты
- •Физические свойства кислот
- •Получение карбоновых кислот
- •Химические свойства карбоновых кислот
- •Свойства отдельных представителей гомологического ряда
- •Задачи по теме
- •Азотсодержащие органические соединения
- •Нитросоединения
- •Нитрилы и изоцианиды
- •Алифатические амины
- •Физические свойства аминов
- •Получение аминов
- •Химические свойства аминов
- •Отдельные представители
- •Экологическая характеристика
- •Задачи по теме
- •Аминокислоты
- •Физические свойства α-аминокислот
- •Способы получения -аминокислот
- •Способы получения -аминокислот
- •Химические свойства аминокислот
- •Отдельные представители
- •Простые и сложные эфиры Простые эфиры
- •Способы получения простых эфиров
- •Физические свойства простых эфиров
- •Химические свойства простых эфиров
- •Отдельные представители
- •Сложные эфиры карбоновых кислот Получение сложных эфиров карбоновых кислот
- •Химические свойства эфиров карбоновых кислот
- •Физические свойства жиров
- •Химические свойства жиров
- •Сложные липиды
- •Ароматические углеводороды, арены Бензол и его производные
- •Методы получения бензола и его гомологов
- •Получение гомологов бензола
- •Физические свойства аренов
- •Химические свойства
- •Экологиченские характеристики
- •Ароматические оксосоединения Фенолы
- •Некоторые физические и термодинамические характеристики ряда фенолов
- •Получение фенола
- •Некоторые химические свойства фенола
- •Задачи по теме
- •Гетероциклические соединения
- •Пятичленные гетероциклы с одним гетероатомом
- •Химические свойства пиридина
- •Диоксины
- •Физико-химические свойства ксенобиотиков типа диоксинов
- •Источники ксенобиотиков
- •Пестициды
- •Фуллерены. Синтез и свойства соединений на их основе
- •Методы получения гидридов фуллеренов
- •Кислотность фуллеренов
- •Применение фуллеренов
- •Высокомолекулярные соединения
- •Свойства высокомолекулярных соединений
- •Основные химические реакции высокомолекулярных соединений
- •Часть II основы химической термодинамики
- •Понятия и термины химической термодинамики
- •Внутренняя энергия
- •Первое началотермодинамики
- •Следствия из первого начала термодинамики
- •Теплоемкость при постоянном объеме, сv
- •Теплоемкость при постоянном давлении
- •Равновесные процессы. Максимальная работа
- •Термохимия
- •Закон Гесса
- •Следствия из закона Гесса
- •И окончательно
- •Связь h и u химических реакций
- •Зависимость тепловых эффектов от температуры. Закон Кирхгофа
- •Совершенно очевидно, что разности Сi можно выразить через уравнение
- •Средняя теплоемкость
- •Работа тепловой машины. Теорема и цикл Карно
- •Второе начало термодинамики
- •Энтропия как критерий самопроизвольного течения процесса
- •Следовательно, если такой процесс протекает в изолированной системе, то
- •Расчет энтропии
- •Расчет изменения энтропии идеального газа
- •Задачи для самостоятельного решения
- •Принцип локального равновесия
- •Важно найти функции, определяющие зависимость deSиdiSот экспериментально измеряемых величин.
- •Статистическая интерпретация энтропии
- •Химический потенциал и химическое сродство
- •Химический потенциал
- •Химическое сродство
- •Уравнение Клапейрона-Клаузиуса
- •Термодинамические потенциалы
- •Свободная энергия Гиббса
- •Для чистого вещества
- •Условия самопроизвольного протекания процесса
- •Уравнение Гиббса-Гельмгольца
- •Тепловая теорема Нернста. Третий закон термодинамики
- •Некоторые аспекты, связанные с достижением химического равновесия
- •Изотерма химической реакции
- •Изобара химической реакции
- •Задачи для самостоятельного решения
- •Задача 7.Для реакции
- •Задача 8.Для реакции
- •Задача 10.Для реакции
- •Задача 11. Для реакции
- •Литература Основная литература
- •Дополнительная литература
Физические свойства алканов
Исходя из самых общих закономерностей, можно отметить следующее. При нормальных условиях (н. у.) алканы с числом углеродных атомов в молекуле С1…С4 – газы, С5…С15 – жидкости, С16 и Сi с i > 16 при н. у. – твердые вещества. В таблице 1 приведены некоторые физические характеристики алканов.
Таблица 1
Физические характеристики некоторых нормальных углеводородов
|
Формула |
Название |
Тпл, С |
Ткип, С |
Плотность,
d |
* |
|
СН4 |
метан |
184,0 |
161,5 |
0,4150 (164 С) |
2,6 |
|
С2Н6 |
этан |
172,0 |
88,3 |
0,5610 (100 С) |
2,6 |
|
С3Н8 |
пропан |
189,9 |
42,17 |
0,5853 (44,5 С) |
6,3 |
|
С4Н10 |
бутан |
135,0 |
0,6…0,3 |
0,60 (0 С) |
8,2 |
|
С5Н12 |
пентан |
131,6 |
36,2 |
0,6260 |
1,9 |
|
С6Н14 |
гексан |
94,3 |
69,0 |
0,6603 |
13,7 |
|
С7Н16 |
гептан |
90,5 |
98,4 |
0,6838 |
15,6 |
|
С8Н18 |
октан |
56,5 |
125,8 |
0,7036 |
— |
|
С9Н20 |
нонан |
53,7 |
150,8 |
0,7176 |
— |
|
С10Н22 |
декан |
30…32 |
174,0 |
0,7301 |
— |
|
С15Н32 |
пентадекан |
10 |
270,5 |
0,7689 |
— |
* поляризуемость молекул
Легко видеть, что наблюдается тенденция возрастания Тпл и Ткип алканов с ростом их молекулярной массы или увеличение числа атомов углерода в молекуле. Это объясняется существенной зависимостью дисперсионного типа межмолекулярного взаимодействия (взаимодействия Ван-дер-Ваальса) от массы молекул. Ранее (Ч I настоящего пособия) приведена известная зависимость, характеризующая энергию дисперсионного взаимодействия, которая имеет вид (Ф. Лондон, 1930 г):
![]() ,
,
где h – постоянная М. Планка, - частота колебаний, соответствующая энергии частиц (атомов) при абсолютном нуле (Т = 0 К), - поляризуемость частиц, r – расстояние между молекулами. Ориентационным и индукционным взаимодействиями применительно к молекулам алканов можно пренебречь, так как их дипольный момент равен нулю. Таким образом, опосредованно молярная масса алканов учтена в величине их поляризуемости. Более подробно зависимость температуры плавления нормальных парафиновых углеводородов показана на рис. 10 (данные А.Н. Несмеянова и Н.А. Несмеянова).
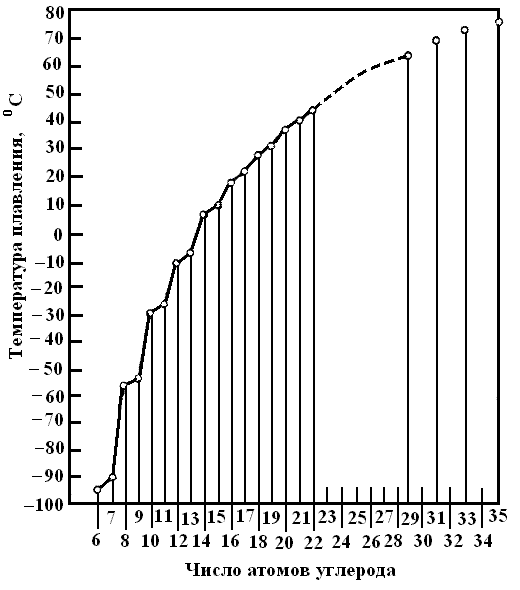
Рис. 10. Зависимость температуры плавления нормальных парафиновых углеводородов от числа атомов углерода в молекуле.
Интересно было выяснить, как влияет разветвление алканов на физические характеристики соединений. Соответствующие данные представлены в таблице 2.
Таким образом, разветвленные алканы кипят и плавятся при более низких температурах, чем вещества нормального строения. В ряде случаев это связывается с большим размером расстояний между отдельными взаимодействующими молекулами в конденсированном (твердом и жидком) состоянии, что выражается в снижении константы дисперсионного взаимодействия. На научном языке это связывается со стерическим (упаковочным) фактором. Чем меньше степень разветвления, тем плотнее упаковка молекул, например, в твёрдом состоянии, тем сильнее силы взаимного притяжения между ними и тем больше энергии (в том числе тепловой) требуется для перевода вещества в жидкое состояние.
Таблица 2
