- •В.И. Вигдорович, с.В. Романцова, н.В. Шель, и.В. Зарапина
- •Оглавление
- •Предисловие
- •Часть I. Основы органической химии
- •Структура органических соединений
- •Теория строения органических соединений а.М. Бутлерова
- •Изомерия органических соединений
- •Индуктивный и мезомерный эффекты
- •Понятие о мезомерном эффекте
- •Типы реакций органических соединений. Понятие о механизме реакции
- •Типы реакций в органической химии
- •Направление и селективность химической реакции
- •Предельные (насыщенные) углеводороды
- •Изомерия алканов.Для алканов характерен один из видов структурной изомерии – изомерия углеродной цепи (строения углеродного скелета). Приведем примеры таких изомеров:
- •Физические свойства алканов
- •Физические характеристики некоторых нормальных углеводородов
- •Влияние разветвления молекул алканов на их физические характеристики
- •Химические свойства алканов
- •Некоторые отдельные представители
- •Экологическая характеристика алканов
- •Задачи по теме
- •Циклоалканы
- •Физические свойства циклоалканов
- •Получение циклоалканов
- •Химические свойства малых циклов
- •Применение циклоалканов
- •Экологическая оценка
- •Непредельные углеводороды Алкены (олефины)
- •Физические свойства олефинов
- •Получение олефиновых углеводородов
- •Химические свойства олефинов
- •Отдельные представители олефинов
- •Экологические характеристики
- •Задачи по теме
- •Алкадиены (диеновые углеводороды)
- •Методы получение диенов
- •Химические свойства диенов
- •Каучуки
- •Экологическая характеристика
- •Задачи по теме
- •Алкины (ацетиленовые углеводороды)
- •Методы получения алкинов
- •Физические свойства алкинов
- •Химические свойства алкинов
- •Экологическая характеристика
- •Задачи по теме
- •Предельные спирты
- •Предельные одноатомные спирты
- •Получение одноатомных спиртов
- •Физические свойства первичных спиртов
- •Химические свойства одноатомных спиртов
- •Отдельные представители
- •Предельные многоатомные спирты
- •Получение двухатомных спиртов
- •Получение трехатомных спиртов
- •Физические свойства многоатомных спиртов
- •Химические свойства многоатомных спиртов
- •Экологическая характеристика
- •Задачи по теме
- •Предельные оксосоединения
- •Альдегиды
- •Получение альдегидов
- •Физические свойства альдегидов
- •Химические свойства альдегидов
- •Отдельные представители
- •Экологическая характеристика
- •Получение кетонов
- •Химические свойства кетонов
- •Отдельные представители
- •Задачи по теме
- •Карбоновые кислоты
- •Электронное строение карбоксильной группы
- •Предельные карбоновые кислоты
- •Физические свойства кислот
- •Получение карбоновых кислот
- •Химические свойства карбоновых кислот
- •Свойства отдельных представителей гомологического ряда
- •Задачи по теме
- •Азотсодержащие органические соединения
- •Нитросоединения
- •Нитрилы и изоцианиды
- •Алифатические амины
- •Физические свойства аминов
- •Получение аминов
- •Химические свойства аминов
- •Отдельные представители
- •Экологическая характеристика
- •Задачи по теме
- •Аминокислоты
- •Физические свойства α-аминокислот
- •Способы получения -аминокислот
- •Способы получения -аминокислот
- •Химические свойства аминокислот
- •Отдельные представители
- •Простые и сложные эфиры Простые эфиры
- •Способы получения простых эфиров
- •Физические свойства простых эфиров
- •Химические свойства простых эфиров
- •Отдельные представители
- •Сложные эфиры карбоновых кислот Получение сложных эфиров карбоновых кислот
- •Химические свойства эфиров карбоновых кислот
- •Физические свойства жиров
- •Химические свойства жиров
- •Сложные липиды
- •Ароматические углеводороды, арены Бензол и его производные
- •Методы получения бензола и его гомологов
- •Получение гомологов бензола
- •Физические свойства аренов
- •Химические свойства
- •Экологиченские характеристики
- •Ароматические оксосоединения Фенолы
- •Некоторые физические и термодинамические характеристики ряда фенолов
- •Получение фенола
- •Некоторые химические свойства фенола
- •Задачи по теме
- •Гетероциклические соединения
- •Пятичленные гетероциклы с одним гетероатомом
- •Химические свойства пиридина
- •Диоксины
- •Физико-химические свойства ксенобиотиков типа диоксинов
- •Источники ксенобиотиков
- •Пестициды
- •Фуллерены. Синтез и свойства соединений на их основе
- •Методы получения гидридов фуллеренов
- •Кислотность фуллеренов
- •Применение фуллеренов
- •Высокомолекулярные соединения
- •Свойства высокомолекулярных соединений
- •Основные химические реакции высокомолекулярных соединений
- •Часть II основы химической термодинамики
- •Понятия и термины химической термодинамики
- •Внутренняя энергия
- •Первое началотермодинамики
- •Следствия из первого начала термодинамики
- •Теплоемкость при постоянном объеме, сv
- •Теплоемкость при постоянном давлении
- •Равновесные процессы. Максимальная работа
- •Термохимия
- •Закон Гесса
- •Следствия из закона Гесса
- •И окончательно
- •Связь h и u химических реакций
- •Зависимость тепловых эффектов от температуры. Закон Кирхгофа
- •Совершенно очевидно, что разности Сi можно выразить через уравнение
- •Средняя теплоемкость
- •Работа тепловой машины. Теорема и цикл Карно
- •Второе начало термодинамики
- •Энтропия как критерий самопроизвольного течения процесса
- •Следовательно, если такой процесс протекает в изолированной системе, то
- •Расчет энтропии
- •Расчет изменения энтропии идеального газа
- •Задачи для самостоятельного решения
- •Принцип локального равновесия
- •Важно найти функции, определяющие зависимость deSиdiSот экспериментально измеряемых величин.
- •Статистическая интерпретация энтропии
- •Химический потенциал и химическое сродство
- •Химический потенциал
- •Химическое сродство
- •Уравнение Клапейрона-Клаузиуса
- •Термодинамические потенциалы
- •Свободная энергия Гиббса
- •Для чистого вещества
- •Условия самопроизвольного протекания процесса
- •Уравнение Гиббса-Гельмгольца
- •Тепловая теорема Нернста. Третий закон термодинамики
- •Некоторые аспекты, связанные с достижением химического равновесия
- •Изотерма химической реакции
- •Изобара химической реакции
- •Задачи для самостоятельного решения
- •Задача 7.Для реакции
- •Задача 8.Для реакции
- •Задача 10.Для реакции
- •Задача 11. Для реакции
- •Литература Основная литература
- •Дополнительная литература
Химические свойства одноатомных спиртов
1. Реакции с участием атома водорода гидроксильной группы.
2. Участие в реакции ОН-группы целиком.
3. Реакции окисления с одновременным участием ОН и С-радикала.
1-й маршрут
1.1. Кислотно-основные свойства
2C2H5OH + 2Na 2C2H5ONa + H2.
Алкоголяты легко гидролизуются:
С2H5ONa + НОН ⇄ C2H5OH + NaOH
1.2. Взаимодействие со щелочами.
C 2H5OH
+ NaOH ⇄
C2H5ONa
+ H2O
2H5OH
+ NaOH ⇄
C2H5ONa
+ H2O
сдвиг равновесия
влево
Надо удалять воду, тогда равновесие реакции сдвинется вправо.
1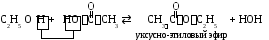 .3.
Этерификация.
.3.
Этерификация.
1.4. Взаимодействие с магнийорганическими соединениями (реакция Чугаева).
СН3СН2ОН +IMgCH3СН3СН2ОMgI+CH4
2-й маршрут
2.1. Дегидратация (межмолекулярная).
R1OH
+ R2OH
![]() R1OR2
+ H2O
R1OR2
+ H2O
2.2. Дегидратация (внутримолекулярная).
СН3СН2СНOHСН3
![]() СН3СН=СНСН3
+ НОН
СН3СН=СНСН3
+ НОН
2-бутанол 2-бутен
Внутримолекулярная дегидратация протекает при более высокой температуре, чем межмолекулярная.
Водород отщепляется от наименее гидрогенизированного атома углерода, соседствующего с атомом углерода, несущим ОН-группу.
2.3. Взаимодействие с галогеноводородами.
C2H5OH + HCl ⇄ C2H5Cl + H2O
3-й маршрут
3.1. Горение (полное окисление)
C2H5OH+ 3О22СО2+ 3H2O–Н1
C4H9OH+ 6О24СО2+ 5H2O–Н2
3.2. Окисление. Первичные спирты окисляются до альдегидов, вторичные – до кетонов; для окисления третичных спиртов требуются очень жёсткие условия и протекает реакция с разрывом связи С–С и с образованием карбоновых кислот.
3СН3СН2ОН ![]() 3СН3СНО
+ K2SO4
+ Cr2(SO4)3
+ 7H2O
3СН3СНО
+ K2SO4
+ Cr2(SO4)3
+ 7H2O
СН3СН2ОН + CuO СН3СНО + Cu + H2O
СН3СНОНСН3![]() СН3СО–СН3
СН3СО–СН3
Отдельные представители
СН3ОН – бесцветная жидкость со слабым спиртовым запахом. Сильнейший яд: 5 г – слепота, 30 г – смерть. Более подвижная жидкость, чемC2H5OH.
C2H5OH– прозрачная жидкость. В медицине – компонент спиртовых настоек, горючее.
С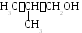 ивушные
масла – маслянистые жидкости с неприятным
запахом. Содержат 90 мас. % н-пропанола,
первичный изобутанол ,
ивушные
масла – маслянистые жидкости с неприятным
запахом. Содержат 90 мас. % н-пропанола,
первичный изобутанол ,
амиловые (С5) спирты. Кроме того, в состав некоторых сивушных масел входят жирные кислоты и азотистые соединения.
Предельные многоатомные спирты
Как уже отмечалось, эти соединения содержат две и более групп ОН.
Двухатомные спирты – диолы, гликоли. Их общая формула CnH2n(OH)2, ОН-группы принадлежат разным атомам углерода.
Изомерия. Наиболее часто встречаются 2 вида структурной изомерии:
1. Изомерия по строению углеродного скелета.
2. Изомерия по положению ОН-группы.
СН2ОНСНОНСН2СН31,2-бутандиол (-гликоль)
СН2ОНСН2СНОНСН31,3-бутандиол (-гликоль)
СН2ОНСН2СН2СН2ОН 1,4-бутандиол (-гликоль)
СН3СНОНСНОНСН32,3-бутандиол
По расположению гидроксильных групп: -гликоли (ОН у С-атомов, находящихся рядом),-гликоли (ОН в положении 1,3),-гликоли (ОН в положении 1,4).
Возможны также изомерия функциональной группы и пространственная изомерия.
Получение двухатомных спиртов
1. Гидролиз дигалогенпроизводных предельных углеводородов или хлоргидринов.
СН3CH2СНClСН2Cl+ 2H2O⇄СН3CH2СНOHСН2OH+ 2HCl
СН3CH2СНOHСН2Cl+HOH⇄ СН3CH2СНOHСН2OH+HCl
хлоргидрин
2. Гидратация -окисей.
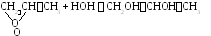
3. Окисление олефинов пероксидом водорода Н2О2.