
- •В.И. Вигдорович, с.В. Романцова, н.В. Шель, и.В. Зарапина
- •Оглавление
- •Предисловие
- •Часть I. Основы органической химии
- •Структура органических соединений
- •Теория строения органических соединений а.М. Бутлерова
- •Изомерия органических соединений
- •Индуктивный и мезомерный эффекты
- •Понятие о мезомерном эффекте
- •Типы реакций органических соединений. Понятие о механизме реакции
- •Типы реакций в органической химии
- •Направление и селективность химической реакции
- •Предельные (насыщенные) углеводороды
- •Изомерия алканов.Для алканов характерен один из видов структурной изомерии – изомерия углеродной цепи (строения углеродного скелета). Приведем примеры таких изомеров:
- •Физические свойства алканов
- •Физические характеристики некоторых нормальных углеводородов
- •Влияние разветвления молекул алканов на их физические характеристики
- •Химические свойства алканов
- •Некоторые отдельные представители
- •Экологическая характеристика алканов
- •Задачи по теме
- •Циклоалканы
- •Физические свойства циклоалканов
- •Получение циклоалканов
- •Химические свойства малых циклов
- •Применение циклоалканов
- •Экологическая оценка
- •Непредельные углеводороды Алкены (олефины)
- •Физические свойства олефинов
- •Получение олефиновых углеводородов
- •Химические свойства олефинов
- •Отдельные представители олефинов
- •Экологические характеристики
- •Задачи по теме
- •Алкадиены (диеновые углеводороды)
- •Методы получение диенов
- •Химические свойства диенов
- •Каучуки
- •Экологическая характеристика
- •Задачи по теме
- •Алкины (ацетиленовые углеводороды)
- •Методы получения алкинов
- •Физические свойства алкинов
- •Химические свойства алкинов
- •Экологическая характеристика
- •Задачи по теме
- •Предельные спирты
- •Предельные одноатомные спирты
- •Получение одноатомных спиртов
- •Физические свойства первичных спиртов
- •Химические свойства одноатомных спиртов
- •Отдельные представители
- •Предельные многоатомные спирты
- •Получение двухатомных спиртов
- •Получение трехатомных спиртов
- •Физические свойства многоатомных спиртов
- •Химические свойства многоатомных спиртов
- •Экологическая характеристика
- •Задачи по теме
- •Предельные оксосоединения
- •Альдегиды
- •Получение альдегидов
- •Физические свойства альдегидов
- •Химические свойства альдегидов
- •Отдельные представители
- •Экологическая характеристика
- •Получение кетонов
- •Химические свойства кетонов
- •Отдельные представители
- •Задачи по теме
- •Карбоновые кислоты
- •Электронное строение карбоксильной группы
- •Предельные карбоновые кислоты
- •Физические свойства кислот
- •Получение карбоновых кислот
- •Химические свойства карбоновых кислот
- •Свойства отдельных представителей гомологического ряда
- •Задачи по теме
- •Азотсодержащие органические соединения
- •Нитросоединения
- •Нитрилы и изоцианиды
- •Алифатические амины
- •Физические свойства аминов
- •Получение аминов
- •Химические свойства аминов
- •Отдельные представители
- •Экологическая характеристика
- •Задачи по теме
- •Аминокислоты
- •Физические свойства α-аминокислот
- •Способы получения -аминокислот
- •Способы получения -аминокислот
- •Химические свойства аминокислот
- •Отдельные представители
- •Простые и сложные эфиры Простые эфиры
- •Способы получения простых эфиров
- •Физические свойства простых эфиров
- •Химические свойства простых эфиров
- •Отдельные представители
- •Сложные эфиры карбоновых кислот Получение сложных эфиров карбоновых кислот
- •Химические свойства эфиров карбоновых кислот
- •Физические свойства жиров
- •Химические свойства жиров
- •Сложные липиды
- •Ароматические углеводороды, арены Бензол и его производные
- •Методы получения бензола и его гомологов
- •Получение гомологов бензола
- •Физические свойства аренов
- •Химические свойства
- •Экологиченские характеристики
- •Ароматические оксосоединения Фенолы
- •Некоторые физические и термодинамические характеристики ряда фенолов
- •Получение фенола
- •Некоторые химические свойства фенола
- •Задачи по теме
- •Гетероциклические соединения
- •Пятичленные гетероциклы с одним гетероатомом
- •Химические свойства пиридина
- •Диоксины
- •Физико-химические свойства ксенобиотиков типа диоксинов
- •Источники ксенобиотиков
- •Пестициды
- •Фуллерены. Синтез и свойства соединений на их основе
- •Методы получения гидридов фуллеренов
- •Кислотность фуллеренов
- •Применение фуллеренов
- •Высокомолекулярные соединения
- •Свойства высокомолекулярных соединений
- •Основные химические реакции высокомолекулярных соединений
- •Часть II основы химической термодинамики
- •Понятия и термины химической термодинамики
- •Внутренняя энергия
- •Первое началотермодинамики
- •Следствия из первого начала термодинамики
- •Теплоемкость при постоянном объеме, сv
- •Теплоемкость при постоянном давлении
- •Равновесные процессы. Максимальная работа
- •Термохимия
- •Закон Гесса
- •Следствия из закона Гесса
- •И окончательно
- •Связь h и u химических реакций
- •Зависимость тепловых эффектов от температуры. Закон Кирхгофа
- •Совершенно очевидно, что разности Сi можно выразить через уравнение
- •Средняя теплоемкость
- •Работа тепловой машины. Теорема и цикл Карно
- •Второе начало термодинамики
- •Энтропия как критерий самопроизвольного течения процесса
- •Следовательно, если такой процесс протекает в изолированной системе, то
- •Расчет энтропии
- •Расчет изменения энтропии идеального газа
- •Задачи для самостоятельного решения
- •Принцип локального равновесия
- •Важно найти функции, определяющие зависимость deSиdiSот экспериментально измеряемых величин.
- •Статистическая интерпретация энтропии
- •Химический потенциал и химическое сродство
- •Химический потенциал
- •Химическое сродство
- •Уравнение Клапейрона-Клаузиуса
- •Термодинамические потенциалы
- •Свободная энергия Гиббса
- •Для чистого вещества
- •Условия самопроизвольного протекания процесса
- •Уравнение Гиббса-Гельмгольца
- •Тепловая теорема Нернста. Третий закон термодинамики
- •Некоторые аспекты, связанные с достижением химического равновесия
- •Изотерма химической реакции
- •Изобара химической реакции
- •Задачи для самостоятельного решения
- •Задача 7.Для реакции
- •Задача 8.Для реакции
- •Задача 10.Для реакции
- •Задача 11. Для реакции
- •Литература Основная литература
- •Дополнительная литература
Фуллерены. Синтез и свойства соединений на их основе
Фуллерены, прежде всего образования С60и С70можно рассматривать как сравнительно новые аллотропные видоизменения углерода. Вид одного из них показан на рис. 18. С другой стороны, фуллерены образуют многочисленные углеводородные соединения и даже более сложные образования.
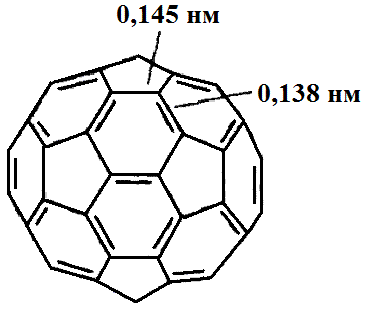
Рис. 18. Длины 6–5 и 6–6 – связей и их положение в молекуле С60.
О б
их реакционной способности известно
сегодня достаточно много. Так, С60проявляет высокую реакционную способность
при взаимодействии с нуклеофильными
реагентами, свободными радикалами,
галогенами. Активно участвует в реакциях
циклоприсоединения. В частности, при
взаимодействии с антраценом.
б
их реакционной способности известно
сегодня достаточно много. Так, С60проявляет высокую реакционную способность
при взаимодействии с нуклеофильными
реагентами, свободными радикалами,
галогенами. Активно участвует в реакциях
циклоприсоединения. В частности, при
взаимодействии с антраценом.
Из рис. 18 следует, что в структуре С60имеется два типа С – С связей: более короткие и прочные двойные, являющиеся общей стороной двух шестигранников (6 – 6 связи) и более длинные и слабые одинарные – общая сторона шисти- и пятигранников (6 – 5-связи).
В структуре С70присутствуют пять типов углеродных атомов и соответственно восемь типов С–С-связи. Четыре из них являются общими сторонами шестигранников и четыре другие – образуются при слиянии пяти- и шестичленных колец. Для фуллеренов С60и С70наиболее реакционноспособны 6 – 6 связи и именно по ним происходит взаимодействие.
Простейший вид химического модифицирования фуллеренов – гидрирование по двойным связям. Их восстановление (гидрирование) представляет интерес для получения аккумуляторов водорода. Согласно теоретическим представлениям, атомы водорода могут располагаться как внутри (эндоэдрально), так и снаружи (экзоэдрально) сферы фуллерена. Так изомер С60Н60может быть получен только в том случае, если 10 атомов Н будут связан эндоэдрально.
Методы получения гидридов фуллеренов
1. Восстановление фуллеренов по Берчу.
С60
![]() С60Н2n.
С60Н2n.
С60Н2nпредставляет собой смесь двух видов продуктов: С60Н36и С60Н18. Процесс, ведущий к их образованию, обратим.
Восстановление С70дает С70Н30. Наиболее стабильный гидрофуллерен возникает при присоединении по 1,4-положениям.
2. Гидрирование фуллеренов гидридами. В 1-й стадии получают С60Н2по реакции:
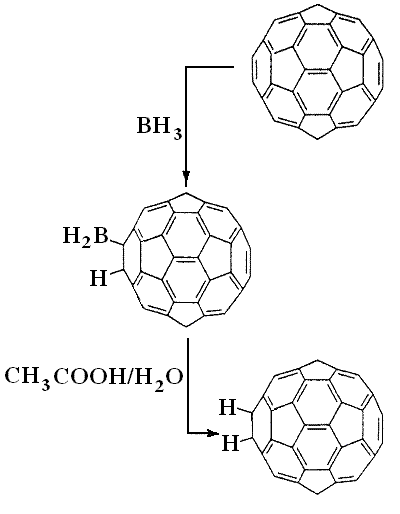
И далее во второй стадии.
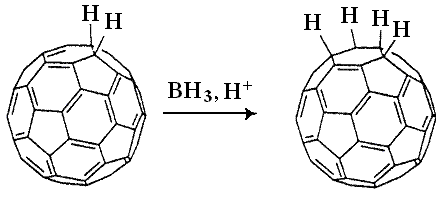
3. Восстановление фуллеренов углеводородами. При высоких температурах фуллерены становятся дегидрирующими агентами по отношению к углеводородам.
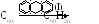
I– 9,10-дигидроантрацен,n= 18 и 36.
В качестве восстановителя можно использовать 1,4-циклогексадиен.
Гидрирование С70протекает по реакции:
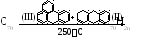
II– дигидроантрацен,III– бензатрен, выступающий в роли катализатора.
Получаются гидриды с большим содержанием водорода С60Н44и С70Н36.
Этим методом получают и дейтеропроизводные С60и С70.
4. Гидрирование фуллеренов водородом. Водород чаще всего присоединяется экзоэдрально.
С60
![]() С60Н2n,
n = 36.
С60Н2n,
n = 36.
При 540 – 750 С и давлении (1,3 – 6,6) 104 Па протекают реакции:
С60 + Н2(г) С60Н+ Н(г)
С60 + Н(г) С60Н(г)
С60Н+ Н2(г)С60Н2(г)+ Н(г)
2С60Н (г)С60Н2(г)+ С60
Гидрофуллерен С60Н60получить не удается в силу, видимо, его нестабильности.
Главные продукты гидрирования С60Н36и С70Н36. Но и они медленно разлагаются в растворе. Твердые образцы гидридов фуллеренов даже при одинаковой молекулярной формуле, синтезированные различными методами, существенно различаются по растворимости, устойчивости к действиюhи воздуха. Это вызвано структурными различиями полигидрофуллеренов.
При электрохимическом катодном насыщении водородом фуллерита (твердый продукт) С60образуется С60Н24и даже С60Н56. Внедренные молекулы существуют в виде пара и ортоводорода.
