
- •В.И. Вигдорович, с.В. Романцова, н.В. Шель, и.В. Зарапина
- •Оглавление
- •Предисловие
- •Часть I. Основы органической химии
- •Структура органических соединений
- •Теория строения органических соединений а.М. Бутлерова
- •Изомерия органических соединений
- •Индуктивный и мезомерный эффекты
- •Понятие о мезомерном эффекте
- •Типы реакций органических соединений. Понятие о механизме реакции
- •Типы реакций в органической химии
- •Направление и селективность химической реакции
- •Предельные (насыщенные) углеводороды
- •Изомерия алканов.Для алканов характерен один из видов структурной изомерии – изомерия углеродной цепи (строения углеродного скелета). Приведем примеры таких изомеров:
- •Физические свойства алканов
- •Физические характеристики некоторых нормальных углеводородов
- •Влияние разветвления молекул алканов на их физические характеристики
- •Химические свойства алканов
- •Некоторые отдельные представители
- •Экологическая характеристика алканов
- •Задачи по теме
- •Циклоалканы
- •Физические свойства циклоалканов
- •Получение циклоалканов
- •Химические свойства малых циклов
- •Применение циклоалканов
- •Экологическая оценка
- •Непредельные углеводороды Алкены (олефины)
- •Физические свойства олефинов
- •Получение олефиновых углеводородов
- •Химические свойства олефинов
- •Отдельные представители олефинов
- •Экологические характеристики
- •Задачи по теме
- •Алкадиены (диеновые углеводороды)
- •Методы получение диенов
- •Химические свойства диенов
- •Каучуки
- •Экологическая характеристика
- •Задачи по теме
- •Алкины (ацетиленовые углеводороды)
- •Методы получения алкинов
- •Физические свойства алкинов
- •Химические свойства алкинов
- •Экологическая характеристика
- •Задачи по теме
- •Предельные спирты
- •Предельные одноатомные спирты
- •Получение одноатомных спиртов
- •Физические свойства первичных спиртов
- •Химические свойства одноатомных спиртов
- •Отдельные представители
- •Предельные многоатомные спирты
- •Получение двухатомных спиртов
- •Получение трехатомных спиртов
- •Физические свойства многоатомных спиртов
- •Химические свойства многоатомных спиртов
- •Экологическая характеристика
- •Задачи по теме
- •Предельные оксосоединения
- •Альдегиды
- •Получение альдегидов
- •Физические свойства альдегидов
- •Химические свойства альдегидов
- •Отдельные представители
- •Экологическая характеристика
- •Получение кетонов
- •Химические свойства кетонов
- •Отдельные представители
- •Задачи по теме
- •Карбоновые кислоты
- •Электронное строение карбоксильной группы
- •Предельные карбоновые кислоты
- •Физические свойства кислот
- •Получение карбоновых кислот
- •Химические свойства карбоновых кислот
- •Свойства отдельных представителей гомологического ряда
- •Задачи по теме
- •Азотсодержащие органические соединения
- •Нитросоединения
- •Нитрилы и изоцианиды
- •Алифатические амины
- •Физические свойства аминов
- •Получение аминов
- •Химические свойства аминов
- •Отдельные представители
- •Экологическая характеристика
- •Задачи по теме
- •Аминокислоты
- •Физические свойства α-аминокислот
- •Способы получения -аминокислот
- •Способы получения -аминокислот
- •Химические свойства аминокислот
- •Отдельные представители
- •Простые и сложные эфиры Простые эфиры
- •Способы получения простых эфиров
- •Физические свойства простых эфиров
- •Химические свойства простых эфиров
- •Отдельные представители
- •Сложные эфиры карбоновых кислот Получение сложных эфиров карбоновых кислот
- •Химические свойства эфиров карбоновых кислот
- •Физические свойства жиров
- •Химические свойства жиров
- •Сложные липиды
- •Ароматические углеводороды, арены Бензол и его производные
- •Методы получения бензола и его гомологов
- •Получение гомологов бензола
- •Физические свойства аренов
- •Химические свойства
- •Экологиченские характеристики
- •Ароматические оксосоединения Фенолы
- •Некоторые физические и термодинамические характеристики ряда фенолов
- •Получение фенола
- •Некоторые химические свойства фенола
- •Задачи по теме
- •Гетероциклические соединения
- •Пятичленные гетероциклы с одним гетероатомом
- •Химические свойства пиридина
- •Диоксины
- •Физико-химические свойства ксенобиотиков типа диоксинов
- •Источники ксенобиотиков
- •Пестициды
- •Фуллерены. Синтез и свойства соединений на их основе
- •Методы получения гидридов фуллеренов
- •Кислотность фуллеренов
- •Применение фуллеренов
- •Высокомолекулярные соединения
- •Свойства высокомолекулярных соединений
- •Основные химические реакции высокомолекулярных соединений
- •Часть II основы химической термодинамики
- •Понятия и термины химической термодинамики
- •Внутренняя энергия
- •Первое началотермодинамики
- •Следствия из первого начала термодинамики
- •Теплоемкость при постоянном объеме, сv
- •Теплоемкость при постоянном давлении
- •Равновесные процессы. Максимальная работа
- •Термохимия
- •Закон Гесса
- •Следствия из закона Гесса
- •И окончательно
- •Связь h и u химических реакций
- •Зависимость тепловых эффектов от температуры. Закон Кирхгофа
- •Совершенно очевидно, что разности Сi можно выразить через уравнение
- •Средняя теплоемкость
- •Работа тепловой машины. Теорема и цикл Карно
- •Второе начало термодинамики
- •Энтропия как критерий самопроизвольного течения процесса
- •Следовательно, если такой процесс протекает в изолированной системе, то
- •Расчет энтропии
- •Расчет изменения энтропии идеального газа
- •Задачи для самостоятельного решения
- •Принцип локального равновесия
- •Важно найти функции, определяющие зависимость deSиdiSот экспериментально измеряемых величин.
- •Статистическая интерпретация энтропии
- •Химический потенциал и химическое сродство
- •Химический потенциал
- •Химическое сродство
- •Уравнение Клапейрона-Клаузиуса
- •Термодинамические потенциалы
- •Свободная энергия Гиббса
- •Для чистого вещества
- •Условия самопроизвольного протекания процесса
- •Уравнение Гиббса-Гельмгольца
- •Тепловая теорема Нернста. Третий закон термодинамики
- •Некоторые аспекты, связанные с достижением химического равновесия
- •Изотерма химической реакции
- •Изобара химической реакции
- •Задачи для самостоятельного решения
- •Задача 7.Для реакции
- •Задача 8.Для реакции
- •Задача 10.Для реакции
- •Задача 11. Для реакции
- •Литература Основная литература
- •Дополнительная литература
Получение фенола
Фенол входит в состав каменноугольной смолы. Дополнительное его количество (мировое производство фенола достигает миллионов тонн) получают следующими методами:
1. Сплавление со щелочью соли бензолсульфокислоты
C6H5SO3Na + NaOH C6H5OH + Na2SO3
2. Гидролиз хлорбензола.
C6H5Cl
+ H2O
![]() C6H5OH
+ HCl
C6H5OH
+ HCl
3. Перспективен метод разложения перекиси кумола разбавленными кислотами. Процесс состоит в следующем.
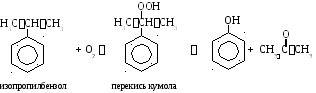
Некоторые химические свойства фенола
1. Взаимодействие по функциональной гидроксильной группе.
1.1. Образование фенолятов
ArOH
+ NaOH
![]() ArONa+
+ H2O,
ArONa+
+ H2O,
Ar – бензольное ядро.
1.2. Образование простых эфиров алкилированием фенолятов
ArONa + RI ArOR + NaI
ArONa + (CH3O)2SO2 ArOCH3 + CH3O–SO2ONa
1.3. Образование сложных эфиров
2. Реакции ароматического ядра
2.1. Галоидирование


2.2. Сульфирование. Приводит к образованию смеси о- и п-фенолсульфокислот. При высоких температурах (t > 100 С) доля п-изомера может составлять до 96 %. При снижении температуры увеличивается доля о-изомера и при 20 С может достигать 49 %.
2.3. Нитрование. Для получения мононитрофенола гидроксибензол нитруют на холоду разбавленной HNO3.
Гидроксибензол применяется для многотоннажного получения фенол-формальдегидных и других полимеров, красителей, пластификаторов, ПАВ, использование С6Н5ОН и п-бензилфенола как антисептика.
Феноло-формальдегидные смолы – продукты поликонденсации фенола с формальдегидом. Природа продуктов реакции зависит от вида катализатора – кислотного или основного типа и молярного соотношения фенола и формальдегида. При взаимодействии в эквимолярных соотношениях в кислой среде в феноле замещаются атомы водорода в о- и п-положении к ОН – группе и образуются соответствующие изомеры оксибензилового спирта.

Гидроксибензиловые спирты устойчивы только в щелочной среде при низкой температуре. В нейтральной и кислой среде они легко вступают в реакцию поликонденсации.
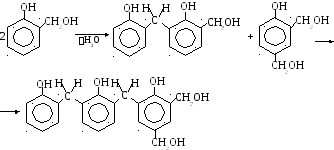
Рассмотрим некоторые токсикологические характеристики гидроксибензола. По нормативным документам нашей страны фенол – вещество 2-го класса опасности (высокоопасное), выраженный аллерген. Относительная интегральная опасность C6H5OH (А) составляет 537 т/на 1 т СО (опасность СО условно принята за 1). При оценке величины А учитывается относительная опасность присутствия фенола в воздухе, вдыхаемом человеком, вероятность его накопления в окружающей среде и пищевых цепях, действия оксибензола на различные реципиенты, вероятность образования вторичных продуктов. В частности, малеиновой кислоты (НООССНСНСООН), временная допустимая концентрация которой в воздухе рабочей зоны 2,6 мг/м3 и в местах проживания людей 4 103 мг/м3 (расчет авторов). Для самого фенола эти требования более жесткие. Его ориентировочные предельно-допустимые концентрации в газовой фазе (рабочая зона 0,3 мг/м3), мест постоянного проживания людей 0,003 мг/м3, в воде рыбохозяйственного назначения ( 0,001 мг/л) и общедоступных водоемов ( 0,3 мг/л).
Острые отравления фенолом при попадании на кожу наблюдаются при содержании его в атмосфере 8,8 … 12,2 мг/м3. Порог чувствительности 4 мг/м3, растворимость в воде – 8,2 масс. % (15 С). Давление насыщенного пара фенола (Рн.п.) можно получить из зависимости
lg
Рн.п.
= A
–
![]() ,
,
где t С; А = 7,6385; В = 1913,8; С = 280.
Рассмотрим кратко пути адсорбционного удаления гидроксибензола из промышленных сточных вод двух типов:
1. Концентрированных с Сисх, составляющей до 4 … 5 г/л.
2. Разбавленных с Сисх, равной 20 … 100 мг/л.
В первом случае адсорбционное удаление гидроксибензола (на 95 – 98 %) проводится техническим углеродом с последующей регенерацией адсорбента и утилизацией фенола. Во втором – используется адсорбционная очистка сточных вод на природных минералах. Так, с использованием концентрата глауконита, позволяющего очищать воды на 99 % при остаточной концентрации фенола (2 –6) 103 мг/л. Некоторые результаты в качестве примера представлены на рис. 17.

Рис. 17. Влияние продолжительности сорбции, рН исходного раствора и высоты (h) слоя адсорбента 95 %-го концентрата глауконита на глубину извлечения фенола (). рН: 3 – 1 и 7; 7 – 2, 5, 7 и 8; 10 – 3 и 6;h, см: 10 – 1, 2, 3 и 7; 5, 2 – 4, 5, 6 и 8.
