
- •Э.А. Гюннер, в.Ф. Шульгин общая химия
- •Введение Предмет и структура химии
- •1. Химическая атомистика
- •1.1. Основные положения и понятия химической атомистики
- •1.2. Стехиометрические законы химии
- •1.3. Методы определения молекулярных масс и атомных масс
- •Методы определения молекулярных масс.
- •1.3.2. Методы определения атомных масс.
- •2. Основы теории строения атома
- •2.1. Предпосылки возникновения квантово-механической теории
- •2.2. Постулаты квантово-механической теории
- •2.3. Волновая функция. Уравнение Шредингера
- •2.4. Атом водорода. Одноэлектронные атомарные ионы
- •2.5. Многоэлектронные атомы
- •3. Периодический закон д.И. Менделеева в свете квантово-механических представлений
- •3.1. Современная формулировка Периодического закона
- •3.2. Структура периодической системы элементов: периоды, группы, подгруппы элементов
- •3.3. Закономерности изменения свойств элементов в периодах и подгруппах периодической системы
- •3.3.1. Эффективный заряд ядра.
- •3.3.2. Атомные радиусы.
- •3.3.3. Энергия ионизации.
- •3.3.4. Сродство к электрону.
- •3.3.5. Электроотрицательность.
- •3.3.6. Степени окисления элементов.
- •3.4. Элементы-аналоги. Виды аналогии в периодической системе элементов
- •3.4.1. Групповая аналогия.
- •3.4.2. Типовая аналогия.
- •3.4.3. Электронная аналогия.
- •VI группа I группа
- •3.4.4. Слоевая аналогия.
- •3.4.5. Контракционная аналогия (шринк-аналогия).
- •3.4.6. Горизонтальная аналогия.
- •3.4.7. Диагональная аналогия.
- •4. Атомное ядро. Радиоактивность
- •4.1. Элементарные частицы
- •4.2. Теория строения атомных ядер
- •4.3. Ядерные реакции
- •4.4.Радиоактивность. Типы радиоактивного распада
- •4.5. Законы радиоактивного распада
- •4.6. Естественная радиоактивность. Радиоактивные ряды. Радиоактивное равновесие
- •4.7. Искусственная радиоактивность. Изотопная индикация
- •4.8. Новые химические элементы
- •4.9. Эволюция элементов во Вселенной
- •5. Химическая связь и строение молекул
- •5.1. Химическая связь. Параметры химической связи. Валентность
- •5.2. Метод валентных связей
- •5.2.1. Основные принципы метода валентных связей.
- •5.2.2. Насыщаемость ковалентной связи. Механизм образования двухцентровой связи.
- •5.2.3. Направленность ковалентной связи. Гибридизация электронных орбиталей.
- •5.2.4. Кратность ковалентной связи.
- •5.2.5. Делокализованные многоцентровые связи. Теория резонанса.
- •5.2.6. Предсказание геометрической формы молекул.
- •5.2.7. Неполярные и полярные связи. Типы ковалентных молекул.
- •5.2.8. Недостатки метода валентных связей.
- •5.3. Метод молекулярных орбиталей
- •5.3.1. Основные принципы метода молекулярных орбиталей.
- •5.3.2. Применение метода молекулярных орбиталей.
- •5.3.2.1. Двухатомные молекулы.
- •5.3.2.2. Молекулы, состоящие из трех и более атомов.
- •5.4. Ионная связь
- •5.4.1. Особенности ионной связи. Свойства ионных соединений.
- •5.4.2. Типы кристаллических решеток ионных соединений. Ионные радиусы.
- •5.3.3. Энергия ионной кристаллической решетки.
- •5.4.4. Поляризация ионов.
- •5.5. Металлическая связь. Зонная теория кристаллов
- •5.6. Межмолекулярное взаимодействие
- •5.7. Водородная связь
- •6. Координационные соединения
- •6.1. Координационные соединения. Основные положения координационной теории
- •6.2. Классификация координационных соединений
- •6.3. Номенклатура координационных соединений
- •6.4. Изомерия координационных соединений
- •6.5. Химическая связь в координационных соединениях
- •6.5.1. Метод валентных связей
- •6.2. Теория кристаллического поля
- •6.3. Метод молекулярных орбиталей
- •6.7. Реакции внешнесферного и внутрисферного замещения. Принцип транс-влияния
- •7. Агрегатные состояния вещества
- •7.1. Типы агрегатного состояния
- •7.2. Твердое состояние вещества
- •7.2.1. Кристаллическое состояние.
- •7.2.2. Аморфное состояние.
- •7.3. Жидкое состояние вещества
- •7.4. Газообразное состояние вещества
- •7.5. Плазма
- •8. Теория химических процессов
- •8.1. Предмет и основные понятия теории химических процессов
- •8.2. Основы химической термодинамики
- •8.2.1. Термодинамические функции. Внутренняя энергия и первый закон термодинамики. Энтальпия.
- •8.2.2. Термохимия. Закон Гесса.
- •8.2.3. Энтропия. Второй и третий законы термодинамики.
- •8.2.4. Свободная энергия Гиббса. Направление химического процесса.
- •8. Химическая кинетика
- •8.3.1. Предмет химической кинетики. Скорость химической реакции. Энергия активации.
- •8.3.2. Факторы, влияющие на скорость химической реакции. Катализаторы и катализ.
- •8.3.3. Кинетическая классификация реакций.Молекулярность и порядок реакции. Механизмы реакций.
- •8.3.4. Некоторые типы многостадийных реакций.
- •8.4. Химическое равновесие
- •8.4.1. Обратимые и необратимые реакции. Состояние химического равновесия.
- •8.4.2. Смещение химического равновесия.
- •9. Растворы
- •9.1. Общая характеристика растворов
- •9.2. Разбавленные растворы неэлектролитов. Коллигативные свойства растворов
- •9.3. Растворы электролитов
- •9.3.1. Электролиты. Теория электролитической диссоциации (ионизации).
- •9.3.2. Теория растворов слабых электролитов.
- •9.3.2.1. Степень ионизации слабых электролитов и методы ее определения.
- •9.3.2.2. Равновесия в растворах слабых электролитов.
- •6,5·10-4 Моль/л
- •9.3.3. Теория сильных электролитов.
- •9.3.4. Обменные реакции в растворах электролитов.
- •9.3.4.1. Типы обменных реакций в растворах электролитов.
- •9.3.4.2. Гидролиз солей.
- •9.3.5. Теории кислот и оснований.
- •9.3.6. Окислительно-восстановительные реакции в растворах.
- •9.3.6.1.Общая характеристика окислительно-восстановительных реакций.
- •9.3.6.2. Составление уравнений окислительно-восстановительных реакций.
- •9.3.6.3. Электродные потенциалы. Направление окислительно-восстановительных реакций. Гальванический элемент.
- •9.3.6.4. Электролиз.
- •9.4. Коллоидные растворы
- •9.4.1. Общая характеристика коллоидных растворов и методы их получения.
- •9.4.2. Строение коллоидных частиц.
- •9.5. Твердые растворы
- •Список рекомендуемой литературы
8.4. Химическое равновесие
8.4.1. Обратимые и необратимые реакции. Состояние химического равновесия.
Химические реакции могут быть подразделены на необратимые и обратимые процессы. Необратимые реакции протекают в направлении превращения реагентов в продукты реакции до тех пор, пока хотя бы один из реагентов не прореагирует количественно. Примером необратимых процессов могут служить реакции
2KClO3 = 2KCl + 3O2,
Cu + 4HNO3 = Cu(NO3)2 + 2NO2 + 2H2O
Обратимые реакции способны протекать одновременно в двух противоположных направлениях; в случае таких процессов взаимодействие исходных веществ приводит к образованию продуктов реакции (прямая реакция), которые, однако, способны взаимодействовать друг с другом с образованием исходных веществ (обратная реакция). К таким реакциям можно отнести взаимодействие азота с водородом:
N2
+ 3H2
![]() 2NH3
2NH3
Заметим, что многие реакции, кажущиеся необратимыми, фактически таковыми не являются. Например, реакция осаждения сульфата бария или реакция нейтрализации
Ba2+
+
SO![]() =
BaSO4↓,
=
BaSO4↓,
H+ + OH- = H2O
являются, строго говоря, обратимыми, так как сульфат бария в какой-то мере растворим, а вода, пусть крайне незначительно, но все же диссоциирует на ионы водорода и гидроксила. О таких реакциях говорят, что они практически необратимы.
Пусть в системе протекает обратимая гомогенная одностадийная реакция
aA + bB dD + eE (8-59)
Кинетические уравнения, отвечающие этой реакции, имеют вид:
![]() (прямая
реакция),
(8-60)
(прямая
реакция),
(8-60)
![]() (обратная
реакция)
(8-61)
(обратная
реакция)
(8-61)
Если смешать некоторые количества веществ А и В, то в первый момент скорость прямой реакции будет максимальна, а скорость обратной реакции будет равна нулю, так как веществ D и Е в системе нет. По мере образования веществ D и Е скорость прямой реакции будет уменьшаться, а скорость обратной реакции - увеличиваться. В конце концов, скорость прямой реакции станет равна скорости обратной реакции, после чего изменение концентраций реагентов и продуктов реакции прекратится: в единицу времени будет образовываться столько молей D и Е, сколько молей этих веществ будет превращаться в А и В.
Состояние системы, в котором скорости прямой и обратной реакции равны, называется химическим равновесием.
Концентрации реагентов и продуктов реакции, при которых система находится в состоянии равновесия, называются равновесными концентрациями. Равновесные концентрации обычно обозначают, заключая формулу соответствующего соединения в квадратные скобки.
Если система находится в состоянии равновесия (v1=v2), правые части уравнений (8-60) и (8-61) равны, т.е.
k1[A]a[B]b = k2[D]d[E]e,
откуда
![]()
Отношение констант скорости есть величина постоянная, не зависящая от концентрации. Эта величина называется константой равновесия
![]() (8-62)
(8-62)
Таким
образом, для системы, находящейся в
состоянии равновесия, отношение
произведения концентраций продуктов
реакции к произведению концентраций
реагентов является постоянной для
данной реакции и данной температуры
величиной, называемой константой
равновесия. Константа равновесия не
зависит от концентраций, но зависит от
природы реагирующих веществ и температуры.
Заметим, что любое равновесие может
устанавливаться при различных значениях
равновесных концентраций. Необходимо
лишь, чтобы выражение
![]() равнялось константе равновесия вне
зависимости от того, чему равны величины
[A], [B], [D] и [E].
равнялось константе равновесия вне
зависимости от того, чему равны величины
[A], [B], [D] и [E].
Если реакция протекает между газообразными веществами, то концентрации взаимодействующих веществ в уравнении (8-63) могут быть заменены парциальными давлениями газов в газовой смеси, так как давление газа пропорционально его концентрации. В этом случае

Поскольку, согласно уравнению состояния идеального газа (1-9),
![]() ,
,
численные значения К и К′ будут различными.
Пусть реакция
А + 2В АВ2 (8-63)
протекает в две стадии
А
+ В
АВ;
![]() (8-64)
(8-64)
AB
+ B
AB2;
![]() (8-65)
(8-65)
Найдем произведение констант равновесия реакций (8-64) и (8-65):
![]() =
К
(8-66)
=
К
(8-66)
Произведение К1.К2 есть константа равновесия реакции (8-63), рассчитанная в предположении, что эта реакция одностадийна. Таким образом, независимо от числа промежуточных стадий стехиометрические коэффициенты уравнения реакции входят в уравнение константы равновесия как показатели степени при соответствующих концентрациях. Так, реакция
N2 + 3H2 2NH3
явно не может быть одностадийной, однако для нее
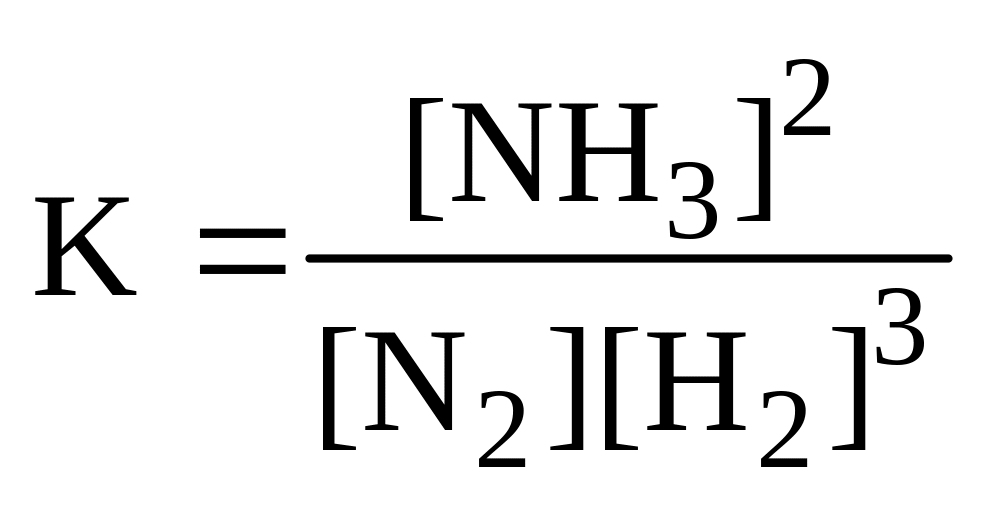
Рассмотрим, в какой мере уравнение (8-62) может быть применено к гетерогенным процессам. Пусть вещества В и Е в уравнении (8-59) являются кристаллическими. Тогда скорости прямой и обратной реакции будут пропорциональны не концентрациям, а поверхностям (S) веществ В и Е:
![]() ,
,
![]()
В состоянии равновесия поверхности SВ и SЕ будут постоянны и войдут в значение константы равновесия. Отсюда для гетерогенного процесса
![]()
Таким образом, уравнение (8-62) применимо и для гетерогенных процессов, но концентрации веществ, образующих индивидуальную фазу, в него не включаются. Например, для реакции
СаСО3(к) СаО(к) + СО2(г)
K = [CO2]
т.е. равновесие устанавливается тогда, когда концентрация (или давление) диоксида углерода достигает определенного значения.
Еще раз подчеркнем, что установление химического равновесия отнюдь не означает, что в системе прекращается протекание прямой и обратной реакций. Эти реакции продолжают протекать, но с одинаковой скоростью. Химическое равновесие, таким образом, является динамическим, т.е. подвижным.
Рассмотрим термодинамические условия установления состояния равновесия. Химическое равновесие всегда устанавливается самопроизвольно и, следовательно, является состоянием, наиболее устойчивым в данных условиях. Независимо от того, скорость какого процесса, прямого или обратного, преобладает в неравновесной системе, переход к равновесию сопровождается понижением свободной энергии Гиббса. Отсюда следует, что в состоянии равновесия энергия Гиббса принимает минимальное значение. Это значение G будет сохраняться, пока равновесие не будет нарушено. Отсюда следует, что пока система пребывает в состоянии равновесия, ΔG для нее равно нулю. Константа равновесия связана с изменением энергии Гиббса уравнением
![]() ,
(8-67)
,
(8-67)
где
![]() - изменение энергии Гиббса при температуре
Т, стандартном давлении и концентрациях
веществ, участвующих во взаимодействии,
равных 1 моль/л. Вывод уравнения (8-67)
будет рассмотрен в курсе физической
химии.
- изменение энергии Гиббса при температуре
Т, стандартном давлении и концентрациях
веществ, участвующих во взаимодействии,
равных 1 моль/л. Вывод уравнения (8-67)
будет рассмотрен в курсе физической
химии.
