
- •Э.А. Гюннер, в.Ф. Шульгин общая химия
- •Введение Предмет и структура химии
- •1. Химическая атомистика
- •1.1. Основные положения и понятия химической атомистики
- •1.2. Стехиометрические законы химии
- •1.3. Методы определения молекулярных масс и атомных масс
- •Методы определения молекулярных масс.
- •1.3.2. Методы определения атомных масс.
- •2. Основы теории строения атома
- •2.1. Предпосылки возникновения квантово-механической теории
- •2.2. Постулаты квантово-механической теории
- •2.3. Волновая функция. Уравнение Шредингера
- •2.4. Атом водорода. Одноэлектронные атомарные ионы
- •2.5. Многоэлектронные атомы
- •3. Периодический закон д.И. Менделеева в свете квантово-механических представлений
- •3.1. Современная формулировка Периодического закона
- •3.2. Структура периодической системы элементов: периоды, группы, подгруппы элементов
- •3.3. Закономерности изменения свойств элементов в периодах и подгруппах периодической системы
- •3.3.1. Эффективный заряд ядра.
- •3.3.2. Атомные радиусы.
- •3.3.3. Энергия ионизации.
- •3.3.4. Сродство к электрону.
- •3.3.5. Электроотрицательность.
- •3.3.6. Степени окисления элементов.
- •3.4. Элементы-аналоги. Виды аналогии в периодической системе элементов
- •3.4.1. Групповая аналогия.
- •3.4.2. Типовая аналогия.
- •3.4.3. Электронная аналогия.
- •VI группа I группа
- •3.4.4. Слоевая аналогия.
- •3.4.5. Контракционная аналогия (шринк-аналогия).
- •3.4.6. Горизонтальная аналогия.
- •3.4.7. Диагональная аналогия.
- •4. Атомное ядро. Радиоактивность
- •4.1. Элементарные частицы
- •4.2. Теория строения атомных ядер
- •4.3. Ядерные реакции
- •4.4.Радиоактивность. Типы радиоактивного распада
- •4.5. Законы радиоактивного распада
- •4.6. Естественная радиоактивность. Радиоактивные ряды. Радиоактивное равновесие
- •4.7. Искусственная радиоактивность. Изотопная индикация
- •4.8. Новые химические элементы
- •4.9. Эволюция элементов во Вселенной
- •5. Химическая связь и строение молекул
- •5.1. Химическая связь. Параметры химической связи. Валентность
- •5.2. Метод валентных связей
- •5.2.1. Основные принципы метода валентных связей.
- •5.2.2. Насыщаемость ковалентной связи. Механизм образования двухцентровой связи.
- •5.2.3. Направленность ковалентной связи. Гибридизация электронных орбиталей.
- •5.2.4. Кратность ковалентной связи.
- •5.2.5. Делокализованные многоцентровые связи. Теория резонанса.
- •5.2.6. Предсказание геометрической формы молекул.
- •5.2.7. Неполярные и полярные связи. Типы ковалентных молекул.
- •5.2.8. Недостатки метода валентных связей.
- •5.3. Метод молекулярных орбиталей
- •5.3.1. Основные принципы метода молекулярных орбиталей.
- •5.3.2. Применение метода молекулярных орбиталей.
- •5.3.2.1. Двухатомные молекулы.
- •5.3.2.2. Молекулы, состоящие из трех и более атомов.
- •5.4. Ионная связь
- •5.4.1. Особенности ионной связи. Свойства ионных соединений.
- •5.4.2. Типы кристаллических решеток ионных соединений. Ионные радиусы.
- •5.3.3. Энергия ионной кристаллической решетки.
- •5.4.4. Поляризация ионов.
- •5.5. Металлическая связь. Зонная теория кристаллов
- •5.6. Межмолекулярное взаимодействие
- •5.7. Водородная связь
- •6. Координационные соединения
- •6.1. Координационные соединения. Основные положения координационной теории
- •6.2. Классификация координационных соединений
- •6.3. Номенклатура координационных соединений
- •6.4. Изомерия координационных соединений
- •6.5. Химическая связь в координационных соединениях
- •6.5.1. Метод валентных связей
- •6.2. Теория кристаллического поля
- •6.3. Метод молекулярных орбиталей
- •6.7. Реакции внешнесферного и внутрисферного замещения. Принцип транс-влияния
- •7. Агрегатные состояния вещества
- •7.1. Типы агрегатного состояния
- •7.2. Твердое состояние вещества
- •7.2.1. Кристаллическое состояние.
- •7.2.2. Аморфное состояние.
- •7.3. Жидкое состояние вещества
- •7.4. Газообразное состояние вещества
- •7.5. Плазма
- •8. Теория химических процессов
- •8.1. Предмет и основные понятия теории химических процессов
- •8.2. Основы химической термодинамики
- •8.2.1. Термодинамические функции. Внутренняя энергия и первый закон термодинамики. Энтальпия.
- •8.2.2. Термохимия. Закон Гесса.
- •8.2.3. Энтропия. Второй и третий законы термодинамики.
- •8.2.4. Свободная энергия Гиббса. Направление химического процесса.
- •8. Химическая кинетика
- •8.3.1. Предмет химической кинетики. Скорость химической реакции. Энергия активации.
- •8.3.2. Факторы, влияющие на скорость химической реакции. Катализаторы и катализ.
- •8.3.3. Кинетическая классификация реакций.Молекулярность и порядок реакции. Механизмы реакций.
- •8.3.4. Некоторые типы многостадийных реакций.
- •8.4. Химическое равновесие
- •8.4.1. Обратимые и необратимые реакции. Состояние химического равновесия.
- •8.4.2. Смещение химического равновесия.
- •9. Растворы
- •9.1. Общая характеристика растворов
- •9.2. Разбавленные растворы неэлектролитов. Коллигативные свойства растворов
- •9.3. Растворы электролитов
- •9.3.1. Электролиты. Теория электролитической диссоциации (ионизации).
- •9.3.2. Теория растворов слабых электролитов.
- •9.3.2.1. Степень ионизации слабых электролитов и методы ее определения.
- •9.3.2.2. Равновесия в растворах слабых электролитов.
- •6,5·10-4 Моль/л
- •9.3.3. Теория сильных электролитов.
- •9.3.4. Обменные реакции в растворах электролитов.
- •9.3.4.1. Типы обменных реакций в растворах электролитов.
- •9.3.4.2. Гидролиз солей.
- •9.3.5. Теории кислот и оснований.
- •9.3.6. Окислительно-восстановительные реакции в растворах.
- •9.3.6.1.Общая характеристика окислительно-восстановительных реакций.
- •9.3.6.2. Составление уравнений окислительно-восстановительных реакций.
- •9.3.6.3. Электродные потенциалы. Направление окислительно-восстановительных реакций. Гальванический элемент.
- •9.3.6.4. Электролиз.
- •9.4. Коллоидные растворы
- •9.4.1. Общая характеристика коллоидных растворов и методы их получения.
- •9.4.2. Строение коллоидных частиц.
- •9.5. Твердые растворы
- •Список рекомендуемой литературы
4.8. Новые химические элементы
Крупным достижением ядерной химии является получение ряда химических элементов, которые по причине неустойчивости их ядер не содержатся в сколько-нибудь ощутимых количествах в земной коре.
Можно выделить две группы подобных элементов. К первой группе следует отнести четыре элемента, расположенных в периодической системе до урана; этим элементам отвечают порядковые номера 43 (технеций), 61 (прометий), 85 (астат) и 87 (франций). Вторую группу образуют элементы, заряды ядер которых превышают заряд ядра урана (трансурановые элементы).
Элементы с порядковыми номерами 43, 61, 85 и 87 были синтезированы в 30х-40х годах путем бомбардировки соответствующих мишеней протонами, дейтронами или ядрами гелия, разогнанными на циклотроне. Ниже приведены ядерные реакции, использованные при синтезе этих элементов:
![]()
![]()
![]()
![]()
Технеций, прометий и франций накапливаются также в продуктах распада урана в ядерных реакторах.
Для синтеза трансурановых элементов используют различные приемы, из которых наиболее важными являются метод нейтронной бомбардировки, бомбардировка -частицами, бомбардировка тяжелыми ионами.
Так, при облучении урана нейтронами наблюдается образование ряда трансурановых элементов по схеме:
![]()
Ядерные реакции с участием -частиц были применены для синтеза элементов с порядковыми номерами от 96 до 101; в качестве мишени обычно используют трансурановые элементы с более низкими порядковыми номерами. В качестве примера приведем реакции синтеза некоторых изотопов кюрия и менделевия:
![]()
![]()
Бомбардировка тяжелыми ионами позволяет синтезировать элементы с порядковыми номерами, превышающими 101. Так 105-й и 107-й элементы удалось получить, используя для бомбардировки тяжелые ионы неона и хрома:
![]()
![]()
Элемент 110 был получен в количестве 40 ядер бомбардировкой тория ионами кальция.
Синтез
трансурановых элементов с очень высокими
порядковыми номерами затруднен тем,
что с ростом заряда ядра быстро уменьшается
устойчивость ядер. Если период полураспада
наиболее устойчивого из синтезированных
изотопов плутония составляет 81 млн. лет
(![]() ),
то для калифорния эта величина равна
900 лет (
),
то для калифорния эта величина равна
900 лет (![]() ),
для фермия - 100 суток (
),
для фермия - 100 суток (![]() ),
для менделевия - 56 суток (
),
для менделевия - 56 суток (![]() ),
для курчатовия - 70 с (
),
для курчатовия - 70 с (![]() ),
а для 107-го элемента - 0,001 с. Тем не менее,
возможность существования относительно
устойчивых ядер в области очень высоких
значений порядковых номеров не исключена.
Особые надежды возлагают на дважды
магический изотоп
),
а для 107-го элемента - 0,001 с. Тем не менее,
возможность существования относительно
устойчивых ядер в области очень высоких
значений порядковых номеров не исключена.
Особые надежды возлагают на дважды
магический изотоп
![]() ,
содержащий 126 протонов и 184 нейтрона.
Можно ожидать, что период полураспада
такого ядра будет величиной порядка
миллиона лет. Однако синтезировать
элемент 126 пока не удалось.
,
содержащий 126 протонов и 184 нейтрона.
Можно ожидать, что период полураспада
такого ядра будет величиной порядка
миллиона лет. Однако синтезировать
элемент 126 пока не удалось.
4.9. Эволюция элементов во Вселенной
Вселенная поражает наше воображение своими размерами. Так, диаметр нашей Галактики составляет около 90 тыс. световых лет1, то есть 8,51017 км; в ее пределах насчитывается около 150 млрд. звезд. Расстояние между галактиками представляют величины порядка 1,5 млн. световых лет, причем уже в сфере радиусом 3109 световых лет число галактик измеряется сотнями миллионов. Во Вселенной сосредоточено огромное количество материи в вещественной форме, образованной теми же элементами, которые известны и на Земле - никаких новых элементов в космосе не обнаружено. Однако при постоянстве качественного состава Вселенной ее количественный элементный состав непрерывно меняется в результате протекания разнообразных ядерных реакций, местом осуществления которых являются звезды, бесчисленные природные ядерные синтезаторы. Вопрос об эволюции элементного состава Вселенной рассматривается в настоящем разделе.
Можно выделить два носителя материи в космосе: это космические тела (звезды, планеты, кометы и т.д.) и космическая диффузная материя (межзвездный газ и космическая пыль).
Одним из основных носителей материи в космосе является межзвездный газ - рассеянные в космическом пространстве атомы различных элементов. Концентрация межзвездного газа очень низка - 1-2 атома в кубическом сантиметре; однако в объеме куба с длиной ребра, равной одному световому году, его масса во много раз превышает массу космических тел в том же объеме. Главными составными частями межзвездного газа являются атомы водорода (90%) и гелия (9%), на долю всех остальных элементов приходится около 1 % общего числа атомов.
Если в некотором объеме космического пространства концентрация диффузной материи окажется достаточно высокой, начинается гравитационное сжатие вещества, сопровождающееся его разогреванием. После того как температура достигнет некоторой критической величины, атомы водорода ионизируются, образуя водородную плазму. После того как температура достигает 10-20 млн. К, в водородной плазме начинает протекает термоядерная реакция синтеза гелия. Этот момент является началом существования звезды.
Ядерный синтез гелия по схеме
![]()
является многостадийным процессом и сопровождается выделением огромного количества энергии (около 650 млн. кДж на моль превращенного водорода). При слишком высоких температурах он протекает по так называемому протон-протонному циклу, включающему три стадии:
![]()
![]()
![]()
На этой стадии звезда является саморегулирующейся системой: с повышением температуры увеличивается объем звезды, уменьшается концентрация водорода и замедляется процесс синтеза ядер гелия, что влечет за собой понижение температуры, сжатие звезды, ускорение термоядерной реакции и повышение температуры.
По мере "выгорания" водорода образующийся гелий накапливается в центральной части звезды, температура в этой области повышается. При 150 млн. К становятся возможными термоядерные реакции гелия, сопровождающиеся образованием ядер с четным зарядом и массой, кратной четырем:
![]()
![]()
![]()
Ядро
![]() крайне неустойчиво, ядра
крайне неустойчиво, ядра
![]() стабильны. С появлением ядер
стабильны. С появлением ядер
![]() становится возможным синтез гелия по
углерод-азотному циклу, в котором ядра
являются своеобразным катализатором:
становится возможным синтез гелия по
углерод-азотному циклу, в котором ядра
являются своеобразным катализатором:
![]()
![]()
![]()
![]()
![]()
![]()
В молодых звездах этот цикл, требующий высоких температур, осуществляется в их ядрах, а протон-протонный цикл - в периферийных областях.
При температурах около 600 млн. К в ядре звезды начинают протекать термоядерные реакции углерода:
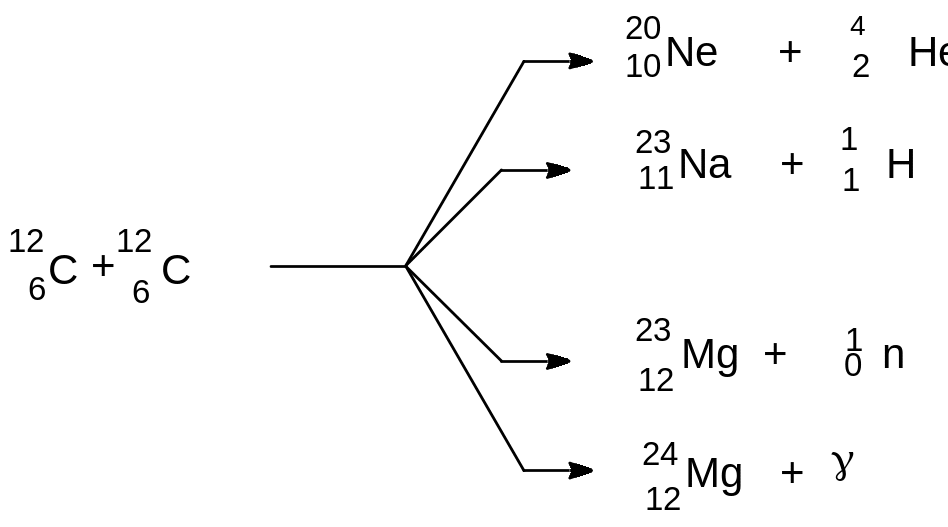
Образующиеся при этом ядра могут взаимодействовать с протонами и ядрами гелия, образуя различные изотопы как с четными так и с нечетными порядковыми номерами, например,
![]()
![]()
В центральной части звезды накапливаются ядра титана, хрома, марганца, железа, кобальта, никеля, меди.
По мере протекания этих процессов усиливается элементное и температурное различие центральной и периферийной зон звезды. Возникает красный гигант - огромная звезда (диаметр красного гиганта может в сотни и тысячи раз превышать диметр Солнца) с горячим ядром (порядка 108 К) и низкотемпературной поверхностью (порядка 2000 К). В недрах красного гиганта становится возможным протекание реакций с участием нейтронов, что приводит к синтезу элементов вплоть до висмута.
Резкое
отличие элементного состава и
температурного режима ядра звезды и ее
оболочки приводит к нарушению равновесия.
Медленные реакции захвата нейтронов
уступают место быстрым, протекающим
лавинообразно, и при температуре ядра
порядка 1010
К происходит взрыв сверхновой звезды.
При взрыве мощные потоки нейтронов
приводят к образованию ядер тяжелых
элементов, вплоть до
![]() .
Огромные количества ядер самых разных
элементов выбрасываются в космос
.
Огромные количества ядер самых разных
элементов выбрасываются в космос
Взорвавшаяся звезда затем сжимается и превращается в белый карлик. Температура белого карлика низка, что исключает протекание термоядерных реакций. Однако в белом карлике могут протекать процессы радиоактивного распада тяжелых ядер.
Выброшенное при взрывах звезд вещество принимает участие в образовании новых космических тел - звезд следующего поколения, более богатых тяжелыми элементами. Таким образом, мировое вещество эволюционирует в направлении уменьшения содержания во Вселенной ядер водорода и увеличения количества более тяжелых ядер.
