- •Э.А. Гюннер, в.Ф. Шульгин общая химия
- •Введение Предмет и структура химии
- •1. Химическая атомистика
- •1.1. Основные положения и понятия химической атомистики
- •1.2. Стехиометрические законы химии
- •1.3. Методы определения молекулярных масс и атомных масс
- •Методы определения молекулярных масс.
- •1.3.2. Методы определения атомных масс.
- •2. Основы теории строения атома
- •2.1. Предпосылки возникновения квантово-механической теории
- •2.2. Постулаты квантово-механической теории
- •2.3. Волновая функция. Уравнение Шредингера
- •2.4. Атом водорода. Одноэлектронные атомарные ионы
- •2.5. Многоэлектронные атомы
- •3. Периодический закон д.И. Менделеева в свете квантово-механических представлений
- •3.1. Современная формулировка Периодического закона
- •3.2. Структура периодической системы элементов: периоды, группы, подгруппы элементов
- •3.3. Закономерности изменения свойств элементов в периодах и подгруппах периодической системы
- •3.3.1. Эффективный заряд ядра.
- •3.3.2. Атомные радиусы.
- •3.3.3. Энергия ионизации.
- •3.3.4. Сродство к электрону.
- •3.3.5. Электроотрицательность.
- •3.3.6. Степени окисления элементов.
- •3.4. Элементы-аналоги. Виды аналогии в периодической системе элементов
- •3.4.1. Групповая аналогия.
- •3.4.2. Типовая аналогия.
- •3.4.3. Электронная аналогия.
- •VI группа I группа
- •3.4.4. Слоевая аналогия.
- •3.4.5. Контракционная аналогия (шринк-аналогия).
- •3.4.6. Горизонтальная аналогия.
- •3.4.7. Диагональная аналогия.
- •4. Атомное ядро. Радиоактивность
- •4.1. Элементарные частицы
- •4.2. Теория строения атомных ядер
- •4.3. Ядерные реакции
- •4.4.Радиоактивность. Типы радиоактивного распада
- •4.5. Законы радиоактивного распада
- •4.6. Естественная радиоактивность. Радиоактивные ряды. Радиоактивное равновесие
- •4.7. Искусственная радиоактивность. Изотопная индикация
- •4.8. Новые химические элементы
- •4.9. Эволюция элементов во Вселенной
- •5. Химическая связь и строение молекул
- •5.1. Химическая связь. Параметры химической связи. Валентность
- •5.2. Метод валентных связей
- •5.2.1. Основные принципы метода валентных связей.
- •5.2.2. Насыщаемость ковалентной связи. Механизм образования двухцентровой связи.
- •5.2.3. Направленность ковалентной связи. Гибридизация электронных орбиталей.
- •5.2.4. Кратность ковалентной связи.
- •5.2.5. Делокализованные многоцентровые связи. Теория резонанса.
- •5.2.6. Предсказание геометрической формы молекул.
- •5.2.7. Неполярные и полярные связи. Типы ковалентных молекул.
- •5.2.8. Недостатки метода валентных связей.
- •5.3. Метод молекулярных орбиталей
- •5.3.1. Основные принципы метода молекулярных орбиталей.
- •5.3.2. Применение метода молекулярных орбиталей.
- •5.3.2.1. Двухатомные молекулы.
- •5.3.2.2. Молекулы, состоящие из трех и более атомов.
- •5.4. Ионная связь
- •5.4.1. Особенности ионной связи. Свойства ионных соединений.
- •5.4.2. Типы кристаллических решеток ионных соединений. Ионные радиусы.
- •5.3.3. Энергия ионной кристаллической решетки.
- •5.4.4. Поляризация ионов.
- •5.5. Металлическая связь. Зонная теория кристаллов
- •5.6. Межмолекулярное взаимодействие
- •5.7. Водородная связь
- •6. Координационные соединения
- •6.1. Координационные соединения. Основные положения координационной теории
- •6.2. Классификация координационных соединений
- •6.3. Номенклатура координационных соединений
- •6.4. Изомерия координационных соединений
- •6.5. Химическая связь в координационных соединениях
- •6.5.1. Метод валентных связей
- •6.2. Теория кристаллического поля
- •6.3. Метод молекулярных орбиталей
- •6.7. Реакции внешнесферного и внутрисферного замещения. Принцип транс-влияния
- •7. Агрегатные состояния вещества
- •7.1. Типы агрегатного состояния
- •7.2. Твердое состояние вещества
- •7.2.1. Кристаллическое состояние.
- •7.2.2. Аморфное состояние.
- •7.3. Жидкое состояние вещества
- •7.4. Газообразное состояние вещества
- •7.5. Плазма
- •8. Теория химических процессов
- •8.1. Предмет и основные понятия теории химических процессов
- •8.2. Основы химической термодинамики
- •8.2.1. Термодинамические функции. Внутренняя энергия и первый закон термодинамики. Энтальпия.
- •8.2.2. Термохимия. Закон Гесса.
- •8.2.3. Энтропия. Второй и третий законы термодинамики.
- •8.2.4. Свободная энергия Гиббса. Направление химического процесса.
- •8. Химическая кинетика
- •8.3.1. Предмет химической кинетики. Скорость химической реакции. Энергия активации.
- •8.3.2. Факторы, влияющие на скорость химической реакции. Катализаторы и катализ.
- •8.3.3. Кинетическая классификация реакций.Молекулярность и порядок реакции. Механизмы реакций.
- •8.3.4. Некоторые типы многостадийных реакций.
- •8.4. Химическое равновесие
- •8.4.1. Обратимые и необратимые реакции. Состояние химического равновесия.
- •8.4.2. Смещение химического равновесия.
- •9. Растворы
- •9.1. Общая характеристика растворов
- •9.2. Разбавленные растворы неэлектролитов. Коллигативные свойства растворов
- •9.3. Растворы электролитов
- •9.3.1. Электролиты. Теория электролитической диссоциации (ионизации).
- •9.3.2. Теория растворов слабых электролитов.
- •9.3.2.1. Степень ионизации слабых электролитов и методы ее определения.
- •9.3.2.2. Равновесия в растворах слабых электролитов.
- •6,5·10-4 Моль/л
- •9.3.3. Теория сильных электролитов.
- •9.3.4. Обменные реакции в растворах электролитов.
- •9.3.4.1. Типы обменных реакций в растворах электролитов.
- •9.3.4.2. Гидролиз солей.
- •9.3.5. Теории кислот и оснований.
- •9.3.6. Окислительно-восстановительные реакции в растворах.
- •9.3.6.1.Общая характеристика окислительно-восстановительных реакций.
- •9.3.6.2. Составление уравнений окислительно-восстановительных реакций.
- •9.3.6.3. Электродные потенциалы. Направление окислительно-восстановительных реакций. Гальванический элемент.
- •9.3.6.4. Электролиз.
- •9.4. Коллоидные растворы
- •9.4.1. Общая характеристика коллоидных растворов и методы их получения.
- •9.4.2. Строение коллоидных частиц.
- •9.5. Твердые растворы
- •Список рекомендуемой литературы
5.2.6. Предсказание геометрической формы молекул.
Представления о направленности связи и теория гибридизации электронных орбиталей позволяют объяснить геометрическую форму молекул веществ с ковалентными связями, но не предсказать ее. Теоретический расчет геометрической конфигурации частицы квантово-механическими методами представляет собой очень сложную и не всегда имеющую однозначное решение задачу. Однако существует довольно простой прием, позволяющий с достаточно высокой надежностью качественно оценить геометрию молекул. Этот прием был разработан Р.Гиллеспи и получил название теории отталкивания электронных пар валентной оболочки, так как связывает форму частицы с силами отталкивания, действующими между электронными парами, сформированными при образовании соответствующей молекулы. Чтобы определить геометрическую форму молекулы по методу Гиллеспи, необходимо знать электронные конфигурации атомов, порядок соединения этих атомов в молекуле, число - и -связей в образовавшейся частице. Теория Гиллеспи особо результативна для молекул, образованных s- и р-элементами.
Теория отталкивания электронных пар валентной оболочки может быть сведена к следующим основным положениям:
1. На геометрическую форму молекулы основное влияние оказывает число электронных пар валентной оболочки (ЭПВО), к которым относятся электронные пары, образующие -связи и остающиеся неподеленными; ЭПВО обычно занимают гибридные орбитали. Электронные пары, образующие -связи, занимают "чистые" атомные орбитали и не влияют принципиально на геометрию молекул. Чтобы узнать число ЭПВО для того или иного атома необходимо сложить число валентных электронов данного атома с числом электронов, предоставленных присоединенными атомами для образования связей, а затем из полученной суммы вычесть число электронов, пошедших на образование -связей, которое равно удвоенному числу -связей, и разделить полученный результат на два. Так, например, в случае молекулы СО2, имеющей две - и две -связи, каждый атом кислорода предоставляет по два электрона на образование связей с атомом углерода, а атом углерода предоставляет по два электрона на образование связей с каждым атомом кислорода. Соответственно число ЭПВО для атома углерода равно
![]()
а для атома кислорода
![]()
![]()
Число связывающих ЭПВО (nC) равно числу -связей, образуемых рассматриваемым атомом (n); разность
nН = NЭПВО - n
равна числу неподеленных ЭПВО.
2. Поведение электронных пар валентной оболочки аналогично поведению точечных одноименных зарядов на поверхности сферы: электронные пары ориентируются так, чтобы отталкивание между ними, а следовательно и энергия системы, были минимальны. Это положение позволяет определить тип гибридизации, характерный для того или иного числа ЭВПО.
Пусть валентная оболочка атома в молекуле включает две электронные пары. Два одноименных точечных заряда, оказавшись на поверхности сферы, расположатся на концах диметра большого круга; соответственно две ЭПВО должны занять орбитали, обеспечивающие валентный угол 180. Отсюда можно заключить, что в случае двух ЭПВО атом подвергается sp-гибридизации (например, атом углерода в молекуле СО2).
С помощью несложных расчетов можно показать, что максимальному удалению и минимальному отталкиванию трех ЭПВО будет отвечать ориентация орбиталей от центра к вершинам равностороннего треугольника, лежащего в плоскости большого круга, т.е. sp2-гибридизация. Четырем ЭПВО соответствует тетраэдрическая конфигурация (sp3-гибридизация). В случае пяти ЭПВО наиболее выгодным является распределение электронных пар по орбиталям, направленным к вершинам тригональной бипирамиды (sp3d-гибридизация). Шести ЭПВО соответствует октаэдрическая конфигурация, обеспечиваемая sp3d2-гибридизацией. Если на валентной оболочке находится более шести электронных пар, вопрос о конфигурации не может быть решен однозначно. Так семи ЭПВО с равной вероятностью могут отвечать три формы координационного многогранника: пентагональная бипирамида, октаэдр с дополнительной вершиной над одной из граней и тригональная призма с дополнительной вершиной над боковой гранью.
3. Неподеленные электронные пары, сосредоточенные возле одного атома занимают больший объем околоядерного пространства, чем связывающие электронные пары, распределенные между двумя атомами. В результате наибольшее отталкивание имеет место между двумя неподеленными парами, наименьшее - между двумя связывающими парами. Следствием неэквивалентности неподеленных и связывающих электронных пар является искажение валентных углов.
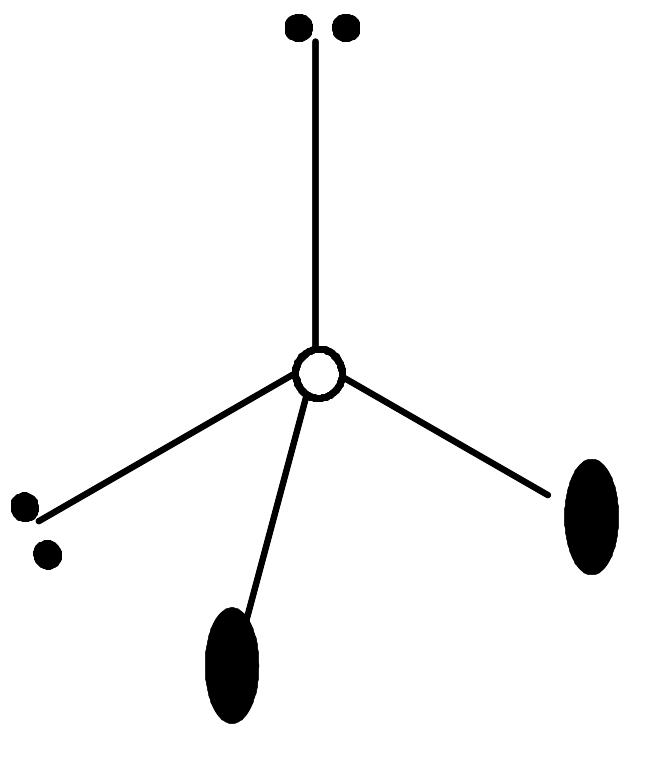
4. Форма молекулы определяется соотношением связывающих и неподеленных ЭПВО. Если центральный атом, для которого устанавливается тип гибридизации, не имеет неподеленных пар, форма молекулы определяется только типом гибридизации этого атома. При наличии неподеленных пар, занимающих гибридные орбитали, форма координационного многогранника изменяется в зависимости от числа неподеленных пар. Идеальные геометрические формы, отвечающие различным значениям числа ЭПВО и неподеленных электронных пар (nH), приведены в табл. 11. В табл. 11 включены также примеры молекул той или иной формы; в скобках указан атом, для которого определяется тип гибридизации.
Как следует из табл. 11, в случае двух ЭПВО возможно образование только линейных молекул. Для трех ЭПВО молекулы могут быть треугольными (nH = 0), угловыми (nH = 1) и линейными (nH =2). Наличие в валентной оболочке четырех электронных пар допускает образование тетраэдрических (nH = O), тригонально-пирамидальных (nH = 1), угловых (nH = 2) и линейных (nH = 3) молекул.
Если число ЭПВО равно пяти и все пары являются связывающими, молекула имеет форму тригональной бипирамиды. При наличии неподеленных ЭПВО для определения геометрии молекулы необходимо знать, какие орбитали, аксиальные или экваториальные, занимают неподеленные электронные пары. Расчет показывает, что более выгодным является экваториальное положение; действительно, занимающие экваториальное положение неподеленные пары имеют только двух ближайших соседей под углом 90 , тогда как при аксиальном положении таких соседей было бы три, что привело бы к более сильному отталкиванию. В результате молекула с одной неподеленной парой имеет форму бисфеноида, с двумя - Т-форму, а трем неподеленным парам соответствуют линейные молекулы.
В случае шести ЭПВО неподеленные пары, стремясь к максимальному взаимному удалению, занимают в октаэдре транс-положения друг относительно друга. В силу этого для шести ЭПВО реализуются следующие формы молекул: октаэдр (nH = 0), тетрагональная пирамида (nH = 1), квадрат (nH = 2), Т-форма (nH = 3). Четырем и пяти неподеленным парам должны отвечать линейные молекулы, однако обнаружить подобные соединения не удалось.
Приведенные в табл. 11 геометрические формы молекул являются идеальными; в реальных же молекулах возможны определенные искажения их геометрии. Рассмотрим причины, обуславливающие эти искажения.
1. Наличие в молекуле неподеленных электронных пар. В соответствии с третьим положением теории Гиллеспи наличие неподеленных пар приводит к сжатию валентных углов в молекулах. Так, например, в идеальном случае валентные углы молекулы SF4 (NЭПВО = 5, nH = 1) равнялись бы 180 (FаксSFакс), 120 (FэквSFэкв) и 90 (FаксSFэкв); в действительности соответствующие углы равны 173,1 , 101,5 и 87,8. Искажение валентных углов тем сильнее, чем ниже в соответствующей подгруппе находится данный элемент.
2. Наличие в молекуле двойных и тройных связей. Двойные и тройные связи короче одинарных и занимают больший объем у центрального атома, что приводит к сжатию валентных углов между парами, образующими одинарную связь. Так для молекулы COCl2, в которой атом кислорода образует с углеродом двойную связь, а атомы хлора - одинарные, числа ЭПВО и неподеленных пар составляют
![]()
nH = 3 - 3 = 0
В соответствии с табл. 11 молекула COCl2 должна иметь форму равностороннего треугольника с валентными углами, равными 120. В действительности же эта молекула имеет форму равнобедренного треугольника (dC=O = 117 пм, dC-Cl = 175 пм, ClCO = 124 , СlCCl = 111 ).
3. Неравноценность присоединенных атомов. Если присоединенные атомы имеют различные радиусы, то и длины связей, и валентные углы в образовавшейся молекуле не будут одинаковы. Так, для молекулы CCl4 и CHCl3 число ЭПВО и неподеленных пар одинаково (NЭПВО = 4, nН = 0). Однако молекула тетрахлорида углерода имеет форму правильного тетраэдра (dC-Cl = 176 пм, ClCCl = 109,5 ), а молекула хлороформа является искаженным тетраэдром (dC-Cl =176 пм, dC-H = 110 пм, ClCCl = 111,3 , HCCl = 107,5).
Таблица 12.
Типы молекул, отвечающие различным числам связывающих и неподеленных
электронных пар
Число ЭПВО
|
Тип гибри-дизации |
Число неподеленных пар |
|||
0 |
1 |
2 |
3 |
||
2 |
sp |
линейная BeF2 (Be) |
линейная AlF (Al) |
|
|
3 |
sp2 |
треугольник BF3 (B) |
угловая SnCl2 (Sn) |
линейная NH (N) |
|
4 |
sp3 |
тетраэдр CF4 (C) |
тригональная пирамида NH3 (N) |
угловая Н2О (О) |
линейная IF (I) |
5 |
sp3d |
тригональная бипирамида PF5 (P) |
бисфеноид SF4 (S)
|
T-форма IF3 (I) |
Линейная XeF2 (Xe) |
6 |
sp3d2 |
октаэдр SF6 (S)
|
тетрагона-льная пирамида BrI5 (Br) |
квадрат XeF4 (Xe) |
Т-форма [XeF3]- (Xe) |
Рассмотрим несколько примеров определения формы молекул по методу Гиллеспи.
Если в молекуле отсутствуют цепочки, содержащие более трех атомов, то для определения ее геометрии достаточно установить тип гибридизации и число неподеленных ЭПВО центрального атома, выбрать по табл. 11 идеальный тип молекулы и внести коррективы, связанные с ожидаемым искажением формы молекулы. Пусть, например, необходимо определить форму молекулы оксофторида ксенона XeO2F2, в которой центральным является атом ксенона, образующий четыре - и две -связи. Числа ЭПВО и неподеленных пар для этой молекулы составляют
![]() ;
nН
= 5 - 4 = 1
;
nН
= 5 - 4 = 1
В соответствии с табл. 11 ксенон подвергается sp3d-гибридизации, а образующаяся молекула имеет форму бисфеноида, в котором атомы кислорода образуют связи за счет экваториальных орбиталей, обеспечивающих этим атомам максимальное удаление от орбитали, занятой неподеленной парой, а атомы фтора, имеющие по три неподеленные пары, находятся в транс-положении. Можно ожидать, что длина двойных связей Xe=O будет меньше длины одинарных связей Xe-F, а углы OXeO и FXeF в связи с наличием неподеленной пары на экваториальной орбитали будут меньше 120 и 180 соответственно. Эти предположения хорошо согласуются с результатами экспериментального определения формы рассматриваемой частицы (рис. 15,а): молекула XeO2F2 действительно имеет форму слегка искаженного бисфеноида (dXe=O = 171 пм, dXe-F = 190 пм, OXeO = 105,7 , FXeF = 174,7).
При определении геометрии сложных молекул, содержащих цепочки из четырех и более атомов, рационально разбить молекулу на фрагменты и определить геометрию каждой из таких частей. Например, при определении формы газообразного метабората натрия Na-O-B=O следует порознь определить форму фрагментов O=B-O и B-O-Na. Для атома бора в O=B-O
![]() nH
= 2 - 2 = 0
nH
= 2 - 2 = 0
т.е. этот фрагмент имеет линейную форму. Для атома кислорода в B-O-Na
![]() nH
= 4 - 2 = 2
nH
= 4 - 2 = 2
Этот фрагмент, таким образом, имеет угловую форму, а валентный угол близок к 109,5 . Как следует из рис. 15,б, молекула NaBO2 действительно представляет собой сочетание линейного и углового фрагментов с валентными углами 180 и 109 . Можно было ожидать, что в молекуле метабората натрия длина связи B=O будет меньше длины связи B-O, однако этого не наблюдается. Возможно причиной этого является делокализация -связи в рассматриваемой частице (см.разд.5.2.5).

Рис. 15. Определение геометрии молекул XeOF2(а), NaBO2(б), SO2(в) и Fe(CO)5(г) по методу Гиллеспи
Если частица является ионом, то при расчете числа ЭПВО следует вычесть заряд иона из числа валентных электронов. Определим геометрию иона IO2F2-. Для атома иода, являющегося центральным и образующего четыре - и две -связи
![]() nH
= 5 - 4 = 1
nH
= 5 - 4 = 1
Рассматриваемый ион должен иметь форму бисфеноида, что подтверждено экспериментально.
Число ЭПВО можно рассчитать также, исходя из электронных конфигураций ионов, образующих данную частицу. Например, ион [AlF6]3- образован ионом Al3+ и шестью ионами F-; связи в этой частице образованы по донорно-акцепторному механизму, причем ион F- предоставляет для образования связи электронную пару. Отсюда для атома алюминия
![]() nH
= 6 - 6 = 0
nH
= 6 - 6 = 0
Алюминий, таким образом, подвергается sp3d2-гибридизации, а ион [AlF6]3- имеет форму октаэдра.
Если в частице имеются нелокализованные связи, следует определить геометрию всех канонических форм, а затем усреднить полученные структуры. Например, для молекулы диоксида серы возможны две канонические формы, отличающиеся тем, с каким атомом кислорода (правым или левым) атом серы образует двойную связь:
![]()
Для атома серы
![]()
(являющийся акцептором атом кислорода электронов на образование связи не предоставляет); отвечающая этой канонической форме частица должна иметь угловое строение и разные длины связей S=O и SO. Усреднение структур канонических форм приводит к симметричной угловой молекуле, в которой длины связей сера-кислород одинаковы (рис. 15,в).
Надежность метода Гиллеспи применительно к соединениям s- и p-элементов весьма высока: вероятность правильного предсказания геометрии молекул составляет 90-95%.
Применение теории отталкивания ЭПВО к соединениям d-элементов встречает определенные затруднения, однако в ряде случаев дает вполне удовлетворительные результаты, особенно для элементов, содержащих на валентном уровне от одного до семи, а также десять электронов. При этом для d-элементов, имеющих вакантные d-орбитали, становятся возможными некоторые типы гибридизации, не реализующиеся в случае s- и p-элементов. Так, для шести, пяти и четырех ЭПВО, наряду с гибридизацией типа sp3d2, sp3d, sp3 становятся возможными и энергетически более предпочтительными d2sp3-, dsp3 и d3s-гибридизация. При расчете числа ЭПВО для атомов d-элементов следует брать от центрального атома не все валентные электроны, а лишь то число их, которое обеспечивает проявляемую атомом степень окисления. Так, например, при определении геометрической формы пентахлорида вольфрама WCl5 от атома вольфрама следует брать не шесть, а пять электронов, так как в рассматриваемом соединении вольфрам имеет степень окисления +5. Тогда
![]()
Вольфрам, таким образом, подвергается dsp3-гибридизации, а молекула пентахлорида вольфрама имеет форму тригональной бипирамиды.
В качестве второго примера определим форму иона [Fe(CN)6]3-. Этот ион можно представить как результат сочетания иона Fe3+, не вносящего вклад в валентную оболочку, и шести ионов CN-, каждый из которых, выступая в роли донора, предоставляет для образования связей электронную пару. Соответственно для атома железа
![]() =
0
=
0
Атом железа находится в состоянии d2sp3-гибридизации, а ион [Fe(CN)6]3- имеет форму октаэдра.
Для элементов, содержащих на d-подуровне 8-9 электронов, надежность предсказания формы молекул понижается. В этом случае, в частности, четырем ЭПВО может отвечать не только sp3- или d3s-гибридизация, что приводит к образованию тетраэдрических молекул, но и dsp2-гибридизация, в результате которой образуются частицы квадратной формы. Например, ионы [NiCl4]2- и [PdCl4]2- изоэлектронны; связь в обеих частицах образуется по донорно-акцепторному механизму. В результате как для никеля, так и для палладия
![]() ,
,
что соответствует образованию тетраэдрических молекул. В действительности же форму тетраэдра имеет лишь ион [NiCl4]2-, тогда как ион [PdCl4]2- является квадратным (dsp2-гибридизация).
Последовательно принимая за центральный различные атомы, можно установить типы гибридизации всех атомов, образующих данную молекулу. Пусть, например, необходимо определить геометрию и типы гибридизации всех атомов молекулы пентакарбонила железа - Fe(CO)5. В этом соединении пять молекул :СО: присоединены к атому железа по донорно-акцепторному механизму за счет неподеленной электронной пары атома углерода. Для геометрии молекулы необходимо определить форму фрагментов FeC5 и FeCO. Принимая атом железа за центральный и учитывая, что степень окисления железа в пентакарбониле равна нулю, имеем
![]()
Атом железа, таким образом, подвергается dsp3-гибридизации, а фрагмент FeC5 имеет форму тригональной бипирамиды. Для атома углерода в фрагменте Fe-CO
![]()
Фрагмент Fe-CO, таким образом, линеен, атом углерода находится в состоянии sp-гибридизации. Для атома кислорода
![]()
что указывает на sp-гибридизацию атома кислорода. В целом форма молекулы Fe(CO)5 показана на рис. 15,г.
Случаи несовпадения реальной и предсказанной по методу Гиллеспи геометрии молекул относительно редки. Так, например, в молекулах газообразных дигалогенидов кальция атом металла имеет две ЭПВО, чему соответствует sp-гибридизация и линейная форма молекул. По экспериментальным данным молекулы CaCl2, CaBr2 и CaI2 действительно линейны: однако молекула CaF2 является угловой с валентным углом, равным 140 . Для атома кислорода в гидроксиде натрия NЭПВО = 4, nH = 2; в соответствие с табл. 11 молекула гидроксида натрия должна быть угловой. В действительности же молекула NaOH линейная.
Приведенные исключения не дают, однако, оснований разочаровываться в методе отталкивания электронных пар валентной оболочки, который при всей его простоте в большинстве случаев позволяет правильно предсказывать форму даже весьма сложных молекул.