
- •08.05.2001 Р., протокол № 4
- •XiMiKo-технологiчного унiверситету, м.Днiпропетровськ;
- •1.1. Прогностическая ценность и теоретическая достаточность
- •Глава 1. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •1.1.1. Природа взаимодействия компонентов каменноугольной смолы. Фенолы, пиридиновые основания, ароматические углеводороды
- •Глава 1. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава 1. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава I. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава I. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава I. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава 1. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава 1. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава I. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава 1. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава 1. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава 1. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава 1. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •1.3. Теоретико-информационный подход к исследованию
- •Глава1. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава 1. Новые подходы к идентификации каменноугольной смолы как физико- химической системы
- •Глава 1. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава 1. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава I. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава I. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава 1. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •ГлаваI. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
- •Глава I. Новые подходы к идентификации каменноугольной смолы кик физико-химической системы
- •Глава 2. Фракционирование каменноугольной смолы. Теоретические и технологические аспекты
- •Глава 2
- •Глава 2. Фракционирование каменноугольной смолы. Теоретические и технологические аспекты
- •Глава 2. Фракционирование каменноугольной смолы. Теоретические и технологические аспекты
- •Глава 2. Фракционирование каменноугольной смолы. Теоретические и технологические аспекты
- •Глава 2. Фракционирование каменноугольной смолы. Теоретические и технологические аспекты
- •Глава 2. Фракционирование каменноугольной смолы. Теоретические и технологические аспекты
- •Глава 2. Фракционирование каменноугольной смолы. Теоретические и технологические аспекты
- •I сборник смолы; 2,5,7-трубчатая печь; 3-испаритель I ступени; 4 -
- •I , ректификационные колонны; 8- узел ввода дополнительного тепла в
- •Глава 2. Фракционирование каменноугольной смолы. Теоретические и технологические аспекты
- •Глава 2. Фракционирование каменноугольной смолы. Теоретические и технологические аспекты
- •Глава 2. Фракционирование каменноугольной смолы. Теоретические и технологические аспекты
- •Глава 2. Фракционирование каменноугольной смолы. Теоретические и технологические аспекты
- •Глава 3
- •Высококипящие фракции каменноугольной
- •Смолы как сырьевая база для получения
- •Полициклических ароматических соединений
- •3.1. Поглотительная фракция
- •Глава 3. Высококипящие фракции каменноугольной смолы как сырьевая база для получения полициклических ароматических соединений
- •Глава 3. Высококипящие фракции каменноугольной смолы как сырьевая база для получения полициклических ароматических соединений
- •3.1.3. Взаимосвязь температуры кристаллизации каменноугольного поглотительного масла с его компонентным составом
- •Глава 3. Высококипящие фракции каменноугольной смолы как сырьевая база для получения полициклических ароматических соединений
- •Глава 3. Высококипящие фракции каменноугольной смолы как сырьевая база для получения полициклических ароматических соединений
- •Глава 3. Высококипящие фракции каменноугольной смолы как сырьевая база для получения полициклических ароматических соединений
- •Глава 3. Высококипящие фракции каменноугольной смолы как сырьевая база для получения полициклических ароматических соединений
- •Глава 3. Высококипящие фракции каменноугольной смолы как сырьевая база для получения полициклических ароматических соединений
- •Глава 3. Высококипящие фракции каменноугольной смолы как сырьевая база для получения полициклических ароматических соединений
- •3.2. Антраценовая фракция
- •3.2.1. Получение сырого антрацена
- •Глава 3. Высококипящие фракции каменноугольной смолы как сырьевая база для получения полициклических ароматических соединений
- •Глава 3. Высококипящие фракции каменноугольной смолы как сырьевая база для
- •Глава 3. Высококипящие фракции каменноугольной смолы как сырьевая база для получения полициклических ароматических соединений
- •Глава 3. Высококипящие фракции каменноугольной смолы как сырьевая база для получения полициклических ароматических соединений
- •Глава 3. Высококипящие фракции камеяноугольной смолы как сырьевая база для получения полициклических ароматических соединений
- •3.3.I. Методы выделения и аналитический контроль высококонденси-рованных ароматических углеводородов с получением индивидуальных соединений высокой степени чистоты
- •Глава 3. Высококипящие фракции каменноугольной смолы как сырьевая база для получения полициклических ароматических соединений
- •Глава 3. Высококипящие фракции каменноугольной смолы как сырьевая база для получения полициклических ароматических соединений
- •Глава 3. Высококипящие фракции каменноугольной смолы как сырьевая база для получения полициклических ароматических соединений
- •Глава 3. Высококипящие фракции каменноугольной смолы как сырьевая база для получения полициклических ароматических соединений
- •Глава 4
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •4.3.2. Исследование режима ректификации исходного сырья для получения обогащенных фракций
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •4.3.6. Технологическая схема комплексной переработки
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •4.3.7. Исследование состава и свойств промежуточных продуктов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Глава 4. Переработка высококипящих фракций с получением индивидуальных полициклических углеводородов
- •Заключение
Глава 1. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
весь набор взаимодействий между соединениями смолы, не прибегнув к попущениям и ограничениям, делающим такую оценку лишенной прогностической ценности.
1.1.1. Природа взаимодействия компонентов каменноугольной смолы. Фенолы, пиридиновые основания, ароматические углеводороды
Для упрощения поставленной задачи и в то же время для получения однозначных и достоверных данных о природе полиазеотропии в системе КУС были выполнены исследования, направленные на изучение взаимодействия фенолов и пиридиновых оснований с ароматическими углеводородами [12, 13].
Вопрос о причинах образования азеотропных смесей до настоящего времени не получил однозначного ответа. Некоторые авторы придерживаются феноменологической точки зрения о причинах образования нераздельно кипящих смесей, высказанной в свое время еще Д.Н. Коноваловым. Другие авторы рассматривают азеотропизм как следствие неидеальности раствора, образованного химически невзаимодействующими компонентами [14]. Данная точка зрения предполагает, что на молекулярном уровне азеотроп ничем не отличается от исходных компонентов. Альтернативной таким взглядам является химическая модель азеотропизма, согласно которой фазовые переходы в жидкой и паровой фазах протекают одновременно с обратимыми химическими реакциями между компонентами.
Хотя химическая природа азеотропизма ряда систем подтверждена экспериментально [15], причины образования азеотропов при ректификации КУС и ее фракций до настоящего времени полностью не раскрыты.
Известно, что в состав КУС и ее фракций входят компоненты нейтрального, кислого и основного характера, которые вступают друг с другом в различного рода взаимодействия. Состав и свойства азеотропов, образующихся при ректификации КУС, определяются природой тех взаимодействий, которые имеют место между компонентами КУС при нормальных условиях (t = 25 °С). Следовательно, изучение механизма взаимодействия компонентов, входящих в состав исходной смолы при нормальных условиях, должно способствовать углублению наших знаний о КУС – сложной многокомпонентной физико-химической системе, с одной стороны, и разработке более обоснованных и рациональных приемов переработки КУС, с другой стороны. В процессе нагревания при ректификацииэти взаимодействия могут усиливаться или ослабляться.
-6-
-7-
Е. Т. КОВАЛЕВ. Научные основы и технология переработки высококипящих фракций каменноугольной смолы с получением полициклических углеводородов
Глава 1. Новые подходы к идентификации каменноугольной смолы как физико-химической системы
Взаимодействие веществ КУС кислого и основного характера хорошо изучено [16]. Гораздо менее исследовано взаимодействие с участием углеводородов «нейтрального» характера. Однако за последнее время появилось много данных, свидетельствующих о проявлении «нейтральными» углеводородами кислотно-основных свойств, и все шире распространяется представление об углеводородах как о кислотах и основаниях [17].
Наличие химического взаимодействия «нейтральных» ароматических углеводородов с другими компонентами КУС подтверждается экспериментальными данными [18, 19]. Так, в работе [18] показано, что нафталин образует с фенолом π-комплекс состава 1:1 за счет водородной связи. Этим объясняется искажение результатов определения нафталина в маслах коксохимического производства криоскопическим методом. Авторы работы [19] обнаружили наличие сильного взаимодействия между нейтральным углеводородом - фенантреном и составляющими каменноугольного пека - α2-фракцией, которое, по их мнению, связано с образованием α-комплексов. Этот факт заставил автора расширить изучение взаимодействия ароматических углеводородов с другими компонентами КУС.
В качестве изучаемых объектов были выбраны нейтральные ароматические углеводороды (а- и (3-метилнафталины, диметилнафталины, фе-нантрен, флуорен, аценафтен, пирен) и различные фенолы (крезолы, кси-ленолы, нафтолы). Продукты были предварительно очищены по соответствующим методикам и высушены.
Изучение взаимодействия между компонентами проводили методом ИК-спектроскопии в четыреххлористом углероде. Записи спектров индивидуальных соединений и бинарных смесей производили на спектрофотометре Specord-75 IR в кюветах 0,154 мм с окошками из КВr при масштабе 7,5 и 15 мм/100 см-1. Время записи 4,4 мин [12].
Ниже приведены значения максимумов поглощения в ИК-спектрах бинарных систем фенол - ароматический углеводород:
Фенол Ароматический углеводород Положение максимума
(АУ) поглощения, см-1
о-Крезол Нафталин 3560-3550
2,3-Ксиленол «» 3560-3550
3,4-Ксиленол «» 3560-3550
3,5-Ксиленол «» 3560-3550
2,5-Ксиленол «» 3560-3550
о-Пропилфенол «» 3560-3550
п-Этилфенол «» 3560-3550
2,4,5-Триметилфенол «» 3560-3550
α-Нафтол «» 3560-3550
|
β-Нафтол |
«» |
|
|
3560-3550 |
|
Мезитол |
«» |
увеличение |
полосы 3610 см-1 |
|
|
о-Нитрофенол |
«» |
межмолекулярная водородная |
||
|
|
|
|
связь не образуется |
|
|
Фенол |
β-Метилнафталин |
|
3560-3550 |
|
|
3,5-Ксиленол |
"" |
|
|
3560-3550 |
|
Фенол |
α-Метилнафталин |
|
3560-3550 |
|
|
0-Пропилфенол |
«» |
|
|
3560-3550 |
|
Фенол |
1,7-Диметилнафталин |
|
3550-3540 |
|
|
3,4-Ксиленол |
«» |
|
|
3550-3540 |
|
п-Этилфенол |
«» |
|
|
3550-3540 |
|
Мезитол |
«» |
|
|
3550-3540 |
|
Фенол |
Фенантрен |
|
|
3560-3550 |
|
Фенол |
Аценафтен |
|
|
3560-3550 |
|
а-Нафтол |
Аценафтен |
|
|
3560-3550 |
|
[i-Нафтол |
«» |
|
|
3560-3550 |
|
Фенол |
Флуорен |
|
|
3560-3550 |
|
Фенол |
Пирен |
|
|
3560-3550 |
Как видно из рис. 1.1-1.3, в спектрах ароматических углеводородов отсутствуют характерные полосы поглощения в области 3800-3200 см-1 (полосы поглощения фенолов в этой области ИК-спектра подробно рассмотрены Л. Беллами в [20]).
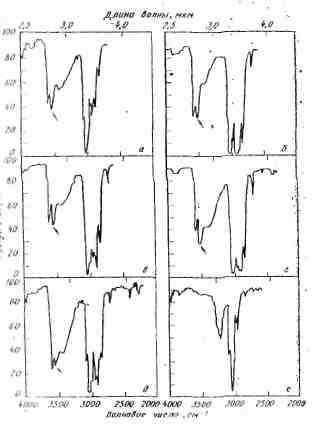
Рис. 1.1 ИК-спектры смесей фенолов с АУ-производными нафталина в СС14 (стрелкой показано положение полосы поглощения 3560-3540 см-1 ,принадлежащей соединению фенол-АУ):
а - 3,5-ксиленол + нафталин; б - а-метилнафталин + о-пропил-фенол; в - b-метилнафталин + 3,5-ксиленол; г - фенол + 1,7-диметилнафталин; д - нафталин + 2,4,5-триметилфенол; е - нафталин + о-нитрофенол. Концентрация фенола 60 г/л, нафталина 120 г/л (насыщенный раствор)
-9-
Е. Т. КОВАЛЕВ. Научные основы и технология переработки высококипящих фракций каменноугольной смолы с получением полициклических углеводородов
В ИК-спектрах фенолов отсутствует узкая полоса 3550 см-1, в то же время в спектрах растворов смесей фенолов и ароматических углеводородов наблюдается четкая узкая полоса при 3560-3550 см .
Появление данной полосы свидетельствует об образовании молекулярных связей между соответствующими фенолами и ароматическим углеводородом за счет водородной связи, образующейся между гидроксильной группой фенола и π-электронной системой ароматического углеводорода [18].
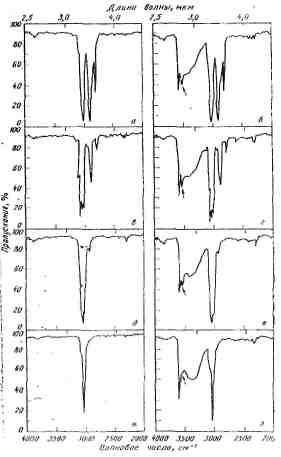
Рис. 1.2 ИК-спектры некоторых АУ и их смесей с фенолом в СС14:
а - аценафтен; б - аценафтен + фенол; в - флуорен; г - флуорен + фенол; д - фенантрен; е - фенантрен + фенол; ж - пирен; з - пирен + фенол. Концентрация фенола 60 г/л, по АУ - насыщенный раствор
Анализ приведенных данных показывает, что значения волнового числа (Vmax) максимума полосы поглощения молекулярного комплекса фенол-ароматический углеводород весьма близки друг к другу и находятся в интервале 3560-3540 см-1. Исключением являются мезитол и о-нитрофенол, в смесях которых с нафталином полоса молекулярного я-комплекса 3560-3540 см-1 не обнаружена.
Полученные результаты спектральных исследований позволяют сделать заключение, что положение полосы молекулярного π-комплекса фенол - ароматический углеводород зависит от трех факторов:
-
основности ароматического углеводорода и кислотности фенола;
-
наличия стерических затруднений, препятствующих образованию межмолекулярной водородной связи;
-
наличия в молекуле фенола прочных внутримолекулярных водородных связей.
Интересно отметить, что полоса межмолекулярной водородной связи в комплексах фенолов с 1,7-диметилнафталином смещена примерно на 10 см-1 в сторону меньших волновых чисел по сравнению с полосами в комплексах фенолов со всеми другими ароматическими углеводородами.
