- •Глава 1 введение
- •1.2 Основные сырьевые источники органических соединений
- •1.3 Классификация органических соединений
- •1.4 Номенклатура органических соединений
- •1.4.1 Тривиальная номенклатура
- •1.4.2 Рациональная номенклатура
- •1.4.3 Номенклатура июпак
- •1.4.3.1. Номенклатура июпак для алифатических углеводородов.
- •Глава 2 теоретические представления в органической химии
- •2.1 Типы химических связей
- •2.2 Образование ковалентных связей атомами углерода (σ- и π-ковалентные связи)
- •2.3 Общие представления о механизмах химических реакций
- •2.3.1 Свободнорадикальные реакции
- •2.3.2 Ионные реакции
- •2.4 Пространственное расположение атомов в молекуле. Конформация молекул
- •Глава 3 алифатические углеводороды алканы,алкены, алкины и алкадиены
- •3.1 Алканы: определениек,изомерия и номенклатура
- •3.1.2 Способы получения алканов
- •3.1.3 Химические свойства
- •Радикальное галогенирование
- •Нитрование
- •Сульфирование, сульфоокисление, сульфохлорирование
- •Окисление
- •Крекинг углеводородов при высоких температурах
- •Задачи для самопроверки
- •3.2 Алкены: определение, изомерия, номенклатура
- •3.2.1 Способы получения
- •3.2.2 Химические свойства
- •3.3. Алкадиены: определение, изомерия, номенклатура
- •3.3.1 Способы получения важнейших диенов
- •3.3.2 Химические особенности 1,3-алкадиенов
- •3.4. Алкины: определение, изомерия, номенклатура
- •3.4.1. Способы получения.
- •3.4.2. Химические свойства
- •Глава 4 карбоциклические соединения
- •4.1. Алициклический ряд: определение, изомерия, номенклатура
- •4.1.1 Способы получения
- •4.1.2. Химические свойства
- •4.1.3. Современные представления о строении моноциклоалканов.
- •4.2. Ароматические углеводороды
- •4.2.1. Строение бензола
- •4.2.2. Способы получения
- •4.2.3. Химические свойства
- •4.3.4. Правила ориентации в бензольном кольце
- •4.2.5. Механизм ориентирующего влияния заместителей
- •4.3. Многоядерные ароматические соединения с неконденсированными и конденсированными бензольными ядрами
- •4.3.1. Основные способы получения
- •4.3.2. Химические особенности
- •Функциональные производные углеводородов
- •Глава 5 галогенопроизводные
- •5.1. Галогенопроизводные: определение, изомерия, номенклатура
- •5.2. Способы получения
- •5..3 Химические свойства
- •Глава 6 кислородсодержащие органические соединения
- •6.1. Спирты: определение, изомерия, номенклатура
- •6.1.1. Способы получения
- •6.1.2 Физические свойства спиртов
- •6.1.3. Химические свойства
- •6.1.4 Понятие о непредельных и многоатомных спиртах
- •6.2. Фенолы: определение, изомерия, номенклатура
- •16.2.1. Способы получения
- •6.2.2. Химические свойства
- •6.3. Простые эфиры: определение, изомерия, номенклатура
- •6.3.1. Способы получения
- •6.3.2. Химические свойства
- •6.3.3. Окись этилена (эпоксисоединения)
- •6.4. Оксосоединения (альдегиды и кетоны)
- •6.4.1. Определение, изомерия и номенклатура оксосоединений
- •6.4.2. Способы получения
- •6.4.3. Химические свойства
- •6.4.4. Понятие о непредельных альдегидах и кетонах
- •6.4.5. Особенности получения и химические свойства хинонов
- •Задачи для самопроверки
- •6.5. Одно и многоосновные карбоновые кислоты и их производные: определение, изомерия, номенклатура
- •6.5.1. Способы получения
- •6.5.2. Химические свойства
- •6.5.3. Особенности предельных и непредельных кислот
- •Задачи для самопроверки
- •Глава 7. Серосодержащие соединения
- •7.1. Органические соединения двухвалентной серы (Тиолы, сульфиды, дисульфиды)
- •7.2. Сульфиновые кислоты и их производные
- •7.3. Сульфоновые кислоты и их производные. Сульфоны.
- •Глава 8. Азотсодержащие органические соединения
- •8.1 Нитросоединения: определение, изомерия, номенклатура.
- •8.1.1. Способы получения
- •8.1.2. Химические свойства
- •Задачи для самопроверки
- •8.2 Амины: определение, изомерия, номенклатура
- •8.2.1 Способы получения
- •8.2.2. Химические свойства
- •8.2.3. Понятие о диаминах
- •Задачи для самопроверки
- •8.3. Диазо- и азосоединения: определение, изомерия, номенклатура
- •8.3.1. Способы получения
- •8.3.2 Физические и химические свойства
- •II. Реакции без выделения азота
- •Задачи для самопроверки
- •Глава 9 . Гетерофункциональные соединеия
- •9.1. Гидроксикислоты: определение, изомерия, номенклатура
- •9.1.1. Способы получения
- •9.1.2. Химические свойства
- •9.1.3. Оптическая изомерия гидроксикислот
- •9.1.4. Ароматические гидроксикислоты и их производные
- •Задачи для самопроверки
- •9.2. Альдегидо- и кетокислоты: определение, изомерия, номенклатура
- •9.2.1. Способы получения
- •9.2.2. Химические особенности
- •9.2.3. Применение ацетоуксусного эфира в органическом синтезе
- •Задачи для самопроверки
- •9.3. Аминокислоты: определение, изомерия, номенклатура
- •9.3.1. Способы получения
- •9.3.2. Химические свойства
- •Задачи для самопроверки
- •Глава 10. Гетероциклические соединения
- •10.1. Определение и классификация гетероциклических соединений.
- •10.2. Пятичленные гетероциклические соединения: изомерия, номенклатура, ароматический характер.
- •10.2.1. Способы получения пятичленных гетероциклических соединений.
- •10.2.3. Химические свойства
- •10.3. Понятие о конденсированных гетероциклах (индол)
- •10.4. Шестичленные гетероциклические соединения: изомерия, номенклатура
- •10.4.1. Химические свойства.
- •Глава 11. Липиды
- •11.1.Определение, классификация изомерия, номенклатура
- •11.2. Простые липиды. (Жиры, масла)
- •10.3. Сложные липиды. Понятие о фосфолипидах.
- •10.4. Понятие о циклических липидах
- •Глава 12. Углеводы
- •12.1. Определение, классификация, изомерия, номенклатура.
- •12.2. Моносахариды: строение, оптическая изомерия.
- •12.3.Химические свойства моносахаридов.
- •12.4. Олигосахариды: особенности строения, химические свойства
- •12.5. Несахароподобные полисахариды: крахмал, гликоген, клетчатка.
- •Глава 13. Пептиды и белки
- •13.1. Протеиногенные аминокислоты
- •13.2. Понятие о строении пептидов.
- •13.3. Особенности строения белков
- •Глава 14. Нуклеиновые кислоты
- •14.1. Понятие о составе и строении нуклеиновых кислот
- •14.2. Классификация и биологическая роль нуклеиновых кислот
12.2. Моносахариды: строение, оптическая изомерия.
Все моносахариды являются многоатомными альдегидо- и кето-спиртами, содержащими ассиметрические атомы углерода. В настоящее время изучены как их относительная, так и абсолютная конфигурация. Родоначальником альдоз является глицериновый альдегид:

Принадлежность того или иного моносахарида к D или L ряду определяется конфигураций ассиметрического центра, наиболее удаленного от карбонильной группы.
Изучение свойств моносахаридов (глюкозы, маннозы и др.) показало, они не реагируют с фуксинсернистой кислотой и бисульфитом натрия. Кроме этого, в природе существует в два раза больше стереоизомеров, чем предполагает формула Фишера. Это объясняется тем, что моносахариды могут существовать в двух таутомерных формах, способных переходить друг в друга. Циклическая форма образуется за счет взаимодействия карбонильной группы с гидроксилом, стоящим у четвертого или пятого атома углерода, при этом атом водорода гидроксильной группы присоединяется к кислороду карбонильной группы, образуя полуацетальный или гликозидный гидроксил. Атом кислорода гидроксильной группы после отщепления от него водорода соединяется с атомом углерода альдегидной группы с образованием кислородного мостика и замыканием цикла:

Если полуацетальный гидроксил находится с той же стороны, что и гидроксил, определяющий конфигурацию, то такая циклическая форма называется α-формой, в противном случае β-формой. α и β-Формы одного и того же моносахарида называются аномерами. Моносахариды, отличающиеся строением тетраэдра соседнего с карбонильной группой называются эпимерами.
Полное название любого моносахарида включает в себя указание на положение полуацетального гидроксила, принадлежность к D или L-ряду, название сахара и величину цикла.
Для более удобного и наглядного написания полуацетальных форм моноз Хеуорс предложил рассматривать их как производные тетрагидропирана и тетрагидрофурана (перспективные формулы):

Соответственно моносахариды будут называться пиранозами или фуранозами.
При переходе от проекционных формул к перспективным, атомы и группы, расположенные слева, следует написать сверху, а расположенные справа – снизу кольца. Концевую (последнюю по нумерации) СН2ОН-группу в углеродной цепи располагают над плоскостью кольца, если атом, с которым она связана, имеет D-конфигурацию:

Для сахаров наблюдается явление мутаротации, т.е. изменение угла вращения плоскополяризованного света в свежеприготовленных растворах. Явление мутаротации связано со взаимными превращениями таутомерных форм моносахаридов и установлением равновесия между ними.

12.3.Химические свойства моносахаридов.
Моносахариды проявляют свойства спиртов, карбонильных соединений и полуацеталей, поэтому рассматривая различные реакции сахаров будет приводиться формула той таутомерной формы, которая непосредственно участвует в данной реакции.
1. Окисление моносахаридов дает полиоксикислоты (-оновые и –аровые)

2. Восстановление сахаров дает многоатомные спирты:

3. Удлинение цепи альдоз (оксинитрильный синтез):

Ход синтеза: оксинитрил, оксикарбоновая кислота. Δ-лактон, гептоза в виде двух стереоизомеров.
4. Изомеризация моносахаридов под действием щелочей.
Под действием щелочи снимается протон, связанный с α-углеродным атомом, на котором имеется частичный положительный заряд. При этом, отрицательный заряд в образовавшемся карбанионе делокализуется, перемещаясь к атому кислорода и образуя енолят-анион:
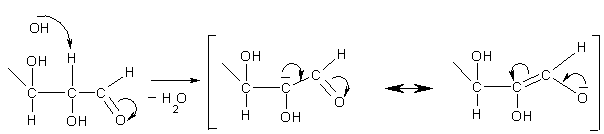 енолят-анион
енолят-анион
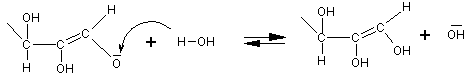
ендиол
При обратном превращении ендиола в карбонильную форму могут образовываться все три изомера, а именно:
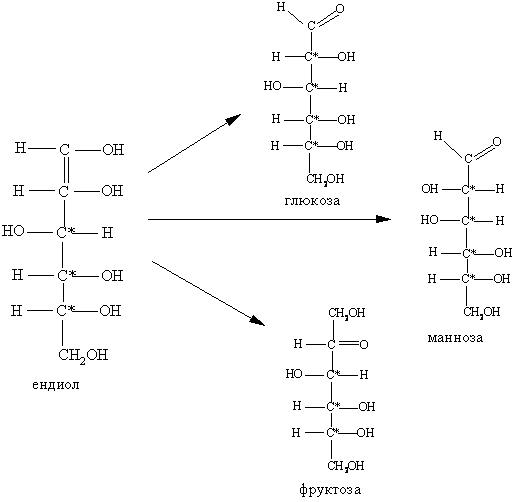
5. Алкилирование. При алкилировании сахара реагируют в полуацетальной (циклической) таутомерной форме

6. Ацилирование. При действии на глюкозу уксусного ангидрида получается пентаацетилглюкоза.

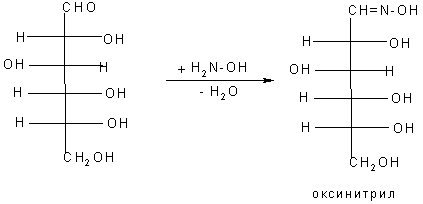
7. Реакция с гидроксиламином – метод установления строения углеводов и перехода от высших сахаров к низшим.