
- •Глава 1 введение
- •1.2 Основные сырьевые источники органических соединений
- •1.3 Классификация органических соединений
- •1.4 Номенклатура органических соединений
- •1.4.1 Тривиальная номенклатура
- •1.4.2 Рациональная номенклатура
- •1.4.3 Номенклатура июпак
- •1.4.3.1. Номенклатура июпак для алифатических углеводородов.
- •Глава 2 теоретические представления в органической химии
- •2.1 Типы химических связей
- •2.2 Образование ковалентных связей атомами углерода (σ- и π-ковалентные связи)
- •2.3 Общие представления о механизмах химических реакций
- •2.3.1 Свободнорадикальные реакции
- •2.3.2 Ионные реакции
- •2.4 Пространственное расположение атомов в молекуле. Конформация молекул
- •Глава 3 алифатические углеводороды алканы,алкены, алкины и алкадиены
- •3.1 Алканы: определениек,изомерия и номенклатура
- •3.1.2 Способы получения алканов
- •3.1.3 Химические свойства
- •Радикальное галогенирование
- •Нитрование
- •Сульфирование, сульфоокисление, сульфохлорирование
- •Окисление
- •Крекинг углеводородов при высоких температурах
- •Задачи для самопроверки
- •3.2 Алкены: определение, изомерия, номенклатура
- •3.2.1 Способы получения
- •3.2.2 Химические свойства
- •3.3. Алкадиены: определение, изомерия, номенклатура
- •3.3.1 Способы получения важнейших диенов
- •3.3.2 Химические особенности 1,3-алкадиенов
- •3.4. Алкины: определение, изомерия, номенклатура
- •3.4.1. Способы получения.
- •3.4.2. Химические свойства
- •Глава 4 карбоциклические соединения
- •4.1. Алициклический ряд: определение, изомерия, номенклатура
- •4.1.1 Способы получения
- •4.1.2. Химические свойства
- •4.1.3. Современные представления о строении моноциклоалканов.
- •4.2. Ароматические углеводороды
- •4.2.1. Строение бензола
- •4.2.2. Способы получения
- •4.2.3. Химические свойства
- •4.3.4. Правила ориентации в бензольном кольце
- •4.2.5. Механизм ориентирующего влияния заместителей
- •4.3. Многоядерные ароматические соединения с неконденсированными и конденсированными бензольными ядрами
- •4.3.1. Основные способы получения
- •4.3.2. Химические особенности
- •Функциональные производные углеводородов
- •Глава 5 галогенопроизводные
- •5.1. Галогенопроизводные: определение, изомерия, номенклатура
- •5.2. Способы получения
- •5..3 Химические свойства
- •Глава 6 кислородсодержащие органические соединения
- •6.1. Спирты: определение, изомерия, номенклатура
- •6.1.1. Способы получения
- •6.1.2 Физические свойства спиртов
- •6.1.3. Химические свойства
- •6.1.4 Понятие о непредельных и многоатомных спиртах
- •6.2. Фенолы: определение, изомерия, номенклатура
- •16.2.1. Способы получения
- •6.2.2. Химические свойства
- •6.3. Простые эфиры: определение, изомерия, номенклатура
- •6.3.1. Способы получения
- •6.3.2. Химические свойства
- •6.3.3. Окись этилена (эпоксисоединения)
- •6.4. Оксосоединения (альдегиды и кетоны)
- •6.4.1. Определение, изомерия и номенклатура оксосоединений
- •6.4.2. Способы получения
- •6.4.3. Химические свойства
- •6.4.4. Понятие о непредельных альдегидах и кетонах
- •6.4.5. Особенности получения и химические свойства хинонов
- •Задачи для самопроверки
- •6.5. Одно и многоосновные карбоновые кислоты и их производные: определение, изомерия, номенклатура
- •6.5.1. Способы получения
- •6.5.2. Химические свойства
- •6.5.3. Особенности предельных и непредельных кислот
- •Задачи для самопроверки
- •Глава 7. Серосодержащие соединения
- •7.1. Органические соединения двухвалентной серы (Тиолы, сульфиды, дисульфиды)
- •7.2. Сульфиновые кислоты и их производные
- •7.3. Сульфоновые кислоты и их производные. Сульфоны.
- •Глава 8. Азотсодержащие органические соединения
- •8.1 Нитросоединения: определение, изомерия, номенклатура.
- •8.1.1. Способы получения
- •8.1.2. Химические свойства
- •Задачи для самопроверки
- •8.2 Амины: определение, изомерия, номенклатура
- •8.2.1 Способы получения
- •8.2.2. Химические свойства
- •8.2.3. Понятие о диаминах
- •Задачи для самопроверки
- •8.3. Диазо- и азосоединения: определение, изомерия, номенклатура
- •8.3.1. Способы получения
- •8.3.2 Физические и химические свойства
- •II. Реакции без выделения азота
- •Задачи для самопроверки
- •Глава 9 . Гетерофункциональные соединеия
- •9.1. Гидроксикислоты: определение, изомерия, номенклатура
- •9.1.1. Способы получения
- •9.1.2. Химические свойства
- •9.1.3. Оптическая изомерия гидроксикислот
- •9.1.4. Ароматические гидроксикислоты и их производные
- •Задачи для самопроверки
- •9.2. Альдегидо- и кетокислоты: определение, изомерия, номенклатура
- •9.2.1. Способы получения
- •9.2.2. Химические особенности
- •9.2.3. Применение ацетоуксусного эфира в органическом синтезе
- •Задачи для самопроверки
- •9.3. Аминокислоты: определение, изомерия, номенклатура
- •9.3.1. Способы получения
- •9.3.2. Химические свойства
- •Задачи для самопроверки
- •Глава 10. Гетероциклические соединения
- •10.1. Определение и классификация гетероциклических соединений.
- •10.2. Пятичленные гетероциклические соединения: изомерия, номенклатура, ароматический характер.
- •10.2.1. Способы получения пятичленных гетероциклических соединений.
- •10.2.3. Химические свойства
- •10.3. Понятие о конденсированных гетероциклах (индол)
- •10.4. Шестичленные гетероциклические соединения: изомерия, номенклатура
- •10.4.1. Химические свойства.
- •Глава 11. Липиды
- •11.1.Определение, классификация изомерия, номенклатура
- •11.2. Простые липиды. (Жиры, масла)
- •10.3. Сложные липиды. Понятие о фосфолипидах.
- •10.4. Понятие о циклических липидах
- •Глава 12. Углеводы
- •12.1. Определение, классификация, изомерия, номенклатура.
- •12.2. Моносахариды: строение, оптическая изомерия.
- •12.3.Химические свойства моносахаридов.
- •12.4. Олигосахариды: особенности строения, химические свойства
- •12.5. Несахароподобные полисахариды: крахмал, гликоген, клетчатка.
- •Глава 13. Пептиды и белки
- •13.1. Протеиногенные аминокислоты
- •13.2. Понятие о строении пептидов.
- •13.3. Особенности строения белков
- •Глава 14. Нуклеиновые кислоты
- •14.1. Понятие о составе и строении нуклеиновых кислот
- •14.2. Классификация и биологическая роль нуклеиновых кислот
4.3. Многоядерные ароматические соединения с неконденсированными и конденсированными бензольными ядрами
Ароматические соединения с неконденсированными ядрами образуют несколько гомологических рядов. Наиболее распространенные из них:
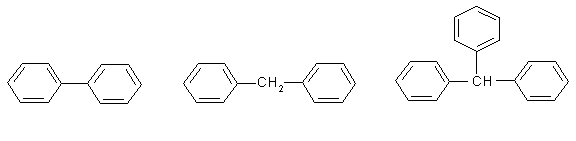
дифенил дифенилметан трифенилметан
4.3.1. Основные способы получения
Для получения соединений этого типа используют реакции, применяемые при синтезе гомологов бензола и специфические реакции:
1. Пиролиз бензола:
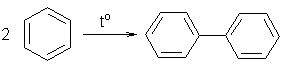
2. Реакция Вюрца-Фиттига
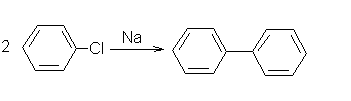
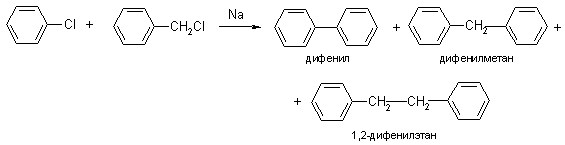
3. Реакция Фриделя –Крафтса

трифенилметан
4.3.2. Химические особенности
Наличие нескольких бензольных колец в молекуле определяет ряд химических особенностей:
1. Второе бензольное кольцо ведет себя как ориентант второго рода:
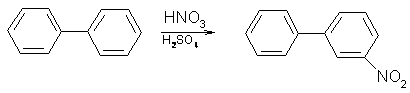
мета-нитродифенил
2. Большое промышленное значение имеет бензидин – производное дифенила, которое получают восстановлением нитробензола до гидразобензола с последующей изомеризацией под действием кислот:
 гидразобензол
бензидин
гидразобензол
бензидин
3. Дифенилметан при окислении образует бензофенон. Аминопроизводное бензофенона – кетон Михлера используется в парфюмерии:
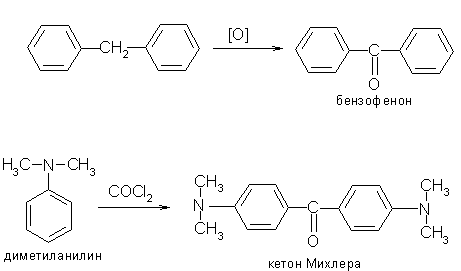
4.Дифенилметан при пропускании через раскаленные трубки образует флуорен:

5. Трифенилметан легко окисляется до трифенилкарбинола, водородный атом в его молекуле легко замещается металлами и галогенами. Причиной подвижности атомов и групп, соединенных с трифенилметановой группировкой, является повышенная устойчивость трифенилметильных радикалов или ионов за счет эффекта сопряжения:

При растворении трифенилкарбинола в концентрированной серной кислоте образуется окрашенный раствор, в котором присутствует карбкатион (С6Н5)3С+ (галохромия).
Взаимные переходы между трифенилметаном, трифенилкарбинолом и хлористым трифенилметилом имеют прямое отношение к химии трифенилметановых красителей. Наиболее простым из красителей этой группы является малахитовый зеленый:
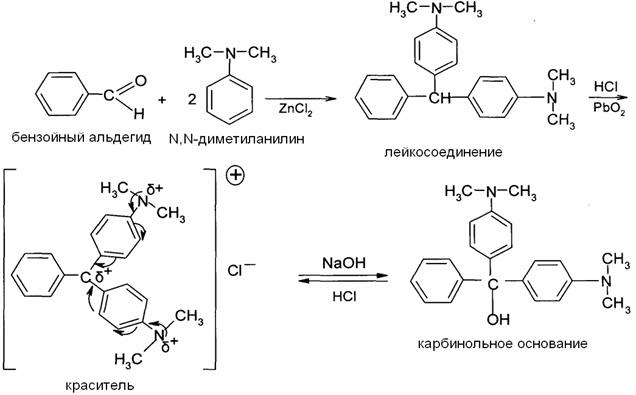
Аминотрифенилметаны – бесцветные вещества, их называют лейкосоединениями. При окислении в кислой среде дают окрашенные соли. В этих солях носителем окраски (хромофором) является сопряженный ион с положительным зарядом, распределенным между атомами углерода и азота. Если вывести аминогруппу из сопряжения образованием соли, то окраска исчезнет.
При подщелачивании раствора красителя происходит медленная нейтрализация и выделяется бесцветный карбинол (карбинольное основание красителя).
6. Хлорпроизводное несимметричного дифенилэтана получают конденсацией хлораля с хлорбензолом:

Это вещество известно под названием ДДТ и применялось как сильный инсектицид. ДДТ помог избавить многие страны от ряда болезней, переносчиками которых являются насекомые. Однако период распада ДДТ в окружающей среде очень велик и он способен накапливаться в живых организмах, нарушая их жизнедеятельность. Поэтому применение ДДТ в большинстве стран запрещено.
Ароматические соединения с конденсированными бензольными ядрами
К ароматическим конденсированным системам относятся нафталин, антрацен, фенантрен:
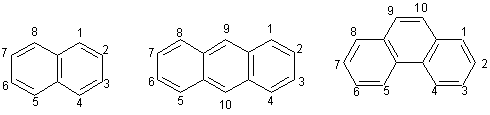
У данных ароматических углеводородов электронная плотность распределена не равномерно, а это приводит к нескольким изомерам при одном заместителе, у нафталина – к двум, у антрацена и фенантрена – к трем.
Для нафталина различают два типа положений (α и β), для антрацена и фенантрена 3 типа положений (α, β и γ).
1,4,5,8 – это α-положения, обладающие избыточной электронной плотностью (для них характерны реакции электрофильного замещения);
2,3,6,7 – β-положения, испытывающие недостаток электронной плотности по сравнению с α-положениями;
9,10 – γ или μ-положения обладают повышенной непредельностью. Для них характерны реакции присоединения и окисления в мягких условиях.
Конденсированные ароматические углеводороды в промышленных условиях получают из каменноугольной смолы или из нефтепродуктов.
Химические способы получения используются в лаборатории для доказательства строения этих соединений.
Для конденсированных систем также характерны реакции электрофильного замещения, как и для бензола. Неравномерность распределения электронной плотности в конденсированных системах определяют направление электрофильного реагента преимущественно в одно из α-положений:

Только процесс сульфирования в зависимости от условий может протекать как в α-, так и в β-положение. Сульфирование нафталина – технически наиболее важная реакция, так как сульфокислоты являются важным материалом для получения красителей:
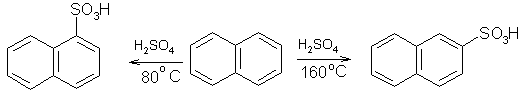
Если в одном из колец нафталина имеется заместитель первого рода, кроме галогенов, то новый заместитель при электрофильном замещении вступает в то же кольцо в свободное α-положение. При наличии заместителя второго рода или галогена в кольце нафталина новый электрофильный реагент направляется в незамещенное кольцо.
Многоядерные углеводороды привлекают к себе все большее внимание, так как они могут стать новым сырьем для анилинокрасочной и других отраслей промышленности. С другой стороны, некоторые из них обладают канцерогенным действием и усиленно изучаются в связи с проблемами возникновения и профилактики рака.
Задачи для самопроверки
1.Назовите следующие соединения:
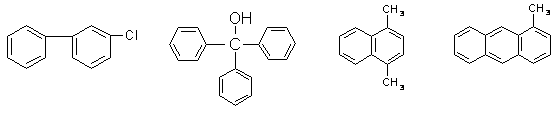
2.Напишите структурные формулы следующих соединений:
а) 2,2′-динитродифенил;
б) 4,4′-дихлордифенилметан
в) о-толил-п-толилметан;
г) 2-нафталинсульфокислота;
д) 9,10-дибромантрацен.
3.Получите из бензола:
а) п-метилдифенил;
б) трифенилметанол;
в) п-толилфенилметан.
4.Используя в качестве исходных веществ фосген и диметиланилин получите 4,4′-тетраметилдиаминодифенилкетон. Напишите для кетона реакцию с аммиаком.
5. Напишите уравнения реакций, соответствующие схеме, назовите все органические вещества:
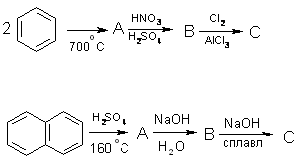
6.Получите из нафталина с наилучшим выходом:
а) 2-нафтол;
б) 1-нафтиламин;
в) 1-бром-5-нитронафталин.
7. Получите из антрацена 2-сульфоантрахинон
