
- •Глава 1 введение
- •1.2 Основные сырьевые источники органических соединений
- •1.3 Классификация органических соединений
- •1.4 Номенклатура органических соединений
- •1.4.1 Тривиальная номенклатура
- •1.4.2 Рациональная номенклатура
- •1.4.3 Номенклатура июпак
- •1.4.3.1. Номенклатура июпак для алифатических углеводородов.
- •Глава 2 теоретические представления в органической химии
- •2.1 Типы химических связей
- •2.2 Образование ковалентных связей атомами углерода (σ- и π-ковалентные связи)
- •2.3 Общие представления о механизмах химических реакций
- •2.3.1 Свободнорадикальные реакции
- •2.3.2 Ионные реакции
- •2.4 Пространственное расположение атомов в молекуле. Конформация молекул
- •Глава 3 алифатические углеводороды алканы,алкены, алкины и алкадиены
- •3.1 Алканы: определениек,изомерия и номенклатура
- •3.1.2 Способы получения алканов
- •3.1.3 Химические свойства
- •Радикальное галогенирование
- •Нитрование
- •Сульфирование, сульфоокисление, сульфохлорирование
- •Окисление
- •Крекинг углеводородов при высоких температурах
- •Задачи для самопроверки
- •3.2 Алкены: определение, изомерия, номенклатура
- •3.2.1 Способы получения
- •3.2.2 Химические свойства
- •3.3. Алкадиены: определение, изомерия, номенклатура
- •3.3.1 Способы получения важнейших диенов
- •3.3.2 Химические особенности 1,3-алкадиенов
- •3.4. Алкины: определение, изомерия, номенклатура
- •3.4.1. Способы получения.
- •3.4.2. Химические свойства
- •Глава 4 карбоциклические соединения
- •4.1. Алициклический ряд: определение, изомерия, номенклатура
- •4.1.1 Способы получения
- •4.1.2. Химические свойства
- •4.1.3. Современные представления о строении моноциклоалканов.
- •4.2. Ароматические углеводороды
- •4.2.1. Строение бензола
- •4.2.2. Способы получения
- •4.2.3. Химические свойства
- •4.3.4. Правила ориентации в бензольном кольце
- •4.2.5. Механизм ориентирующего влияния заместителей
- •4.3. Многоядерные ароматические соединения с неконденсированными и конденсированными бензольными ядрами
- •4.3.1. Основные способы получения
- •4.3.2. Химические особенности
- •Функциональные производные углеводородов
- •Глава 5 галогенопроизводные
- •5.1. Галогенопроизводные: определение, изомерия, номенклатура
- •5.2. Способы получения
- •5..3 Химические свойства
- •Глава 6 кислородсодержащие органические соединения
- •6.1. Спирты: определение, изомерия, номенклатура
- •6.1.1. Способы получения
- •6.1.2 Физические свойства спиртов
- •6.1.3. Химические свойства
- •6.1.4 Понятие о непредельных и многоатомных спиртах
- •6.2. Фенолы: определение, изомерия, номенклатура
- •16.2.1. Способы получения
- •6.2.2. Химические свойства
- •6.3. Простые эфиры: определение, изомерия, номенклатура
- •6.3.1. Способы получения
- •6.3.2. Химические свойства
- •6.3.3. Окись этилена (эпоксисоединения)
- •6.4. Оксосоединения (альдегиды и кетоны)
- •6.4.1. Определение, изомерия и номенклатура оксосоединений
- •6.4.2. Способы получения
- •6.4.3. Химические свойства
- •6.4.4. Понятие о непредельных альдегидах и кетонах
- •6.4.5. Особенности получения и химические свойства хинонов
- •Задачи для самопроверки
- •6.5. Одно и многоосновные карбоновые кислоты и их производные: определение, изомерия, номенклатура
- •6.5.1. Способы получения
- •6.5.2. Химические свойства
- •6.5.3. Особенности предельных и непредельных кислот
- •Задачи для самопроверки
- •Глава 7. Серосодержащие соединения
- •7.1. Органические соединения двухвалентной серы (Тиолы, сульфиды, дисульфиды)
- •7.2. Сульфиновые кислоты и их производные
- •7.3. Сульфоновые кислоты и их производные. Сульфоны.
- •Глава 8. Азотсодержащие органические соединения
- •8.1 Нитросоединения: определение, изомерия, номенклатура.
- •8.1.1. Способы получения
- •8.1.2. Химические свойства
- •Задачи для самопроверки
- •8.2 Амины: определение, изомерия, номенклатура
- •8.2.1 Способы получения
- •8.2.2. Химические свойства
- •8.2.3. Понятие о диаминах
- •Задачи для самопроверки
- •8.3. Диазо- и азосоединения: определение, изомерия, номенклатура
- •8.3.1. Способы получения
- •8.3.2 Физические и химические свойства
- •II. Реакции без выделения азота
- •Задачи для самопроверки
- •Глава 9 . Гетерофункциональные соединеия
- •9.1. Гидроксикислоты: определение, изомерия, номенклатура
- •9.1.1. Способы получения
- •9.1.2. Химические свойства
- •9.1.3. Оптическая изомерия гидроксикислот
- •9.1.4. Ароматические гидроксикислоты и их производные
- •Задачи для самопроверки
- •9.2. Альдегидо- и кетокислоты: определение, изомерия, номенклатура
- •9.2.1. Способы получения
- •9.2.2. Химические особенности
- •9.2.3. Применение ацетоуксусного эфира в органическом синтезе
- •Задачи для самопроверки
- •9.3. Аминокислоты: определение, изомерия, номенклатура
- •9.3.1. Способы получения
- •9.3.2. Химические свойства
- •Задачи для самопроверки
- •Глава 10. Гетероциклические соединения
- •10.1. Определение и классификация гетероциклических соединений.
- •10.2. Пятичленные гетероциклические соединения: изомерия, номенклатура, ароматический характер.
- •10.2.1. Способы получения пятичленных гетероциклических соединений.
- •10.2.3. Химические свойства
- •10.3. Понятие о конденсированных гетероциклах (индол)
- •10.4. Шестичленные гетероциклические соединения: изомерия, номенклатура
- •10.4.1. Химические свойства.
- •Глава 11. Липиды
- •11.1.Определение, классификация изомерия, номенклатура
- •11.2. Простые липиды. (Жиры, масла)
- •10.3. Сложные липиды. Понятие о фосфолипидах.
- •10.4. Понятие о циклических липидах
- •Глава 12. Углеводы
- •12.1. Определение, классификация, изомерия, номенклатура.
- •12.2. Моносахариды: строение, оптическая изомерия.
- •12.3.Химические свойства моносахаридов.
- •12.4. Олигосахариды: особенности строения, химические свойства
- •12.5. Несахароподобные полисахариды: крахмал, гликоген, клетчатка.
- •Глава 13. Пептиды и белки
- •13.1. Протеиногенные аминокислоты
- •13.2. Понятие о строении пептидов.
- •13.3. Особенности строения белков
- •Глава 14. Нуклеиновые кислоты
- •14.1. Понятие о составе и строении нуклеиновых кислот
- •14.2. Классификация и биологическая роль нуклеиновых кислот
3.2 Алкены: определение, изомерия, номенклатура
Углеводороды, в молекулах которых помимо одинарных углерод-углеродных σ-связей имеются углерод-углеродные π-связи, называются непредельными.
Углеводороды, содержащие одну углерод-углеродную π-связь (то есть двойную связь), называются алкенами или олефинами. Общая формула членов гомологического ряда этиленовых углеводородов СnH2n. Родоначальник ряда − этилен СН2=СН2.
Изомерия и номенклатура
В соответствии с правилами ИЮПАК при построении названий алкенов наиболее длинная углеродная цепь, содержащая двойную связь, получает название соответствующего алкана, в котором суффикс «ан» заменен на «ен». Эта цепь нумеруется таким образом, чтобы углеродные атомы, участвующие в образовании двойной связи, получили номера, наименьшие из возможных. Радикалы называются и нумеруются, как и в случае алканов:
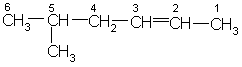 5-метил-2-гексен
5-метил-2-гексен
Углеводородные радикалы, образованные из алкенов, получают суффикс –енил, в общем случае –алкенил. Нумерация в сложных радикалах начинается от углеродного атома, имеющего свободную валентность. Для простейших радикалов используются тривиальные названия:
 этенил
2-пропенил
1-метилэтенил
2-метил-2-бутенил
этенил
2-пропенил
1-метилэтенил
2-метил-2-бутенил
(винил) (аллил) (изоаллил)
Структурная изомерия начинается в этом ряду, как и в ряду предельных углеводородов, с члена ряда С4, однако число изомеров значительно больше. Наряду с изомерией, связанной со строением углеродной цепи, в ряду олефинов наблюдается структурная изомерия, обусловленная положением двойной связи в цепи.
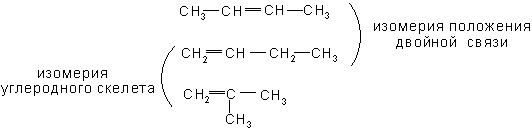
Кроме того, в ряду олефинов имеет место пространственная (геометрическая), так называемая цис-, транс- изомерия (E, Z).
Вращение вокруг связи С─С в молекулах алканов требует малой затраты энергии (8-16 кДж/моль). Для этого достаточно теплового движения молекул.
Вращение же фрагментов С=С относительно друг друга требует разрыва π-связи и затраты 272 кДж/моль. В связи с этим соединения, содержащие у атомов углерода, связанных двойной связью, хотя бы по одному разному заместителю, могут существовать в изомерных формах. Эти изомеры различаются пространственным расположением заместителей относительно друг друга. Если заместители расположены по одну сторону от двойной связи, то такой изомер называется цис-изомером, и транс-изомером, если по разные стороны:

(Z) цис-2-бутен (Е) транс-2-бутен
В сложных молекулах понятие цис- и транс- становятся неопределенными. В этих случаях пользуются общей ZЕ-системой обозначений. Составлена таблица возрастающего старшинства групп. Если старшая группа у одного из углеродных атомов находится по одну сторону со старшей группой у другого атома углерода, то этот изомер называется Z-изомером.
3.2.1 Способы получения
Олефины встречаются в некоторых сортах нефти. В чистом виде из нефти выделены углеводороды от С6Н12 до С13Н26. Алкены, в виде сложных смесей получаются при крекинге нефти.
В технике, кроме того, применяется получение этиленовых углеводородов дегидрированием предельных углеводородов. Катализатором этого процесса служит окись хрома:
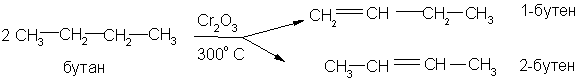 В
лаборатории этиленовые углеводороды
получают следующими способами:
В
лаборатории этиленовые углеводороды
получают следующими способами:
1. При действии спиртовых растворов едких щелочей на галогенопроизводные отщепляется галогеноводород и образуется двойная связь. Порядок отщепления галогеноводорода в большинстве случаев определяется правилом Зайцева: при образовании галогеноводорода и воды наиболее легко отщепляется водород от наименее гидрогенизированного соседнего атома углерода:
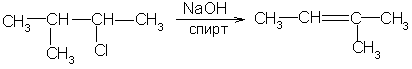
2-метил-3-хлорбутан 2-метил-2-бутен
2. При действии на спирт дегидратирующих средств:
![]()
![]()
этилен
3. При действии Zn или Mg на дигалогенопроизводные с двумя атомами галогена у соседних атомов углерода (вицинальные дигалогенопроизводные):
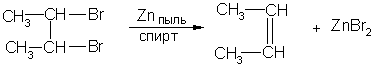
2,3-дибромбутан 2-бутен
4. Гидрированием ацетиленовых или диеновых углеводородов. Алкины гидрируются над катализаторами с пониженной активностью (Fe или платина и Рd, «отравленные» серой, Na в аммиаке):
![]()
пропин пропен
![]()
1,3-бутадиен 2-бутен
Физические свойства
Физические свойства алкенов подобны свойствам соответствующих алканов. Низшие алкены (С2 – С4 ) являются газами, средние алкены (начиная с С5 до С17) жидкостями, не смешивающиеся с водой. Высшие алкены – твердые вещества.
Олефины с нормальной цепью углеродных атомов кипят при более высокой температуре, чем их изомеры с разветвленной цепью. Перемещение двойной связи в центр молекулы вызывает повышение температуры кипения и плавления алкена. Цис-изомеры обычно кипят при более высокой, а плавятся при более низкой температуре, чем транс-изомеры.
Плотность олефинов меньше единицы, но больше, чем плотность соответствующих парафинов. В гомологическом ряду она увеличивается. Для олефинов характерны более высокие показатели преломления света, чем для парафинов.
Следует заметить, что этиленовые углеводороды хорошо растворяются в растворах некоторых солей тяжелых металлов (Сu2Cl2), образуя с ними комплексные соединения.
