- •Глава 1 введение
- •1.2 Основные сырьевые источники органических соединений
- •1.3 Классификация органических соединений
- •1.4 Номенклатура органических соединений
- •1.4.1 Тривиальная номенклатура
- •1.4.2 Рациональная номенклатура
- •1.4.3 Номенклатура июпак
- •1.4.3.1. Номенклатура июпак для алифатических углеводородов.
- •Глава 2 теоретические представления в органической химии
- •2.1 Типы химических связей
- •2.2 Образование ковалентных связей атомами углерода (σ- и π-ковалентные связи)
- •2.3 Общие представления о механизмах химических реакций
- •2.3.1 Свободнорадикальные реакции
- •2.3.2 Ионные реакции
- •2.4 Пространственное расположение атомов в молекуле. Конформация молекул
- •Глава 3 алифатические углеводороды алканы,алкены, алкины и алкадиены
- •3.1 Алканы: определениек,изомерия и номенклатура
- •3.1.2 Способы получения алканов
- •3.1.3 Химические свойства
- •Радикальное галогенирование
- •Нитрование
- •Сульфирование, сульфоокисление, сульфохлорирование
- •Окисление
- •Крекинг углеводородов при высоких температурах
- •Задачи для самопроверки
- •3.2 Алкены: определение, изомерия, номенклатура
- •3.2.1 Способы получения
- •3.2.2 Химические свойства
- •3.3. Алкадиены: определение, изомерия, номенклатура
- •3.3.1 Способы получения важнейших диенов
- •3.3.2 Химические особенности 1,3-алкадиенов
- •3.4. Алкины: определение, изомерия, номенклатура
- •3.4.1. Способы получения.
- •3.4.2. Химические свойства
- •Глава 4 карбоциклические соединения
- •4.1. Алициклический ряд: определение, изомерия, номенклатура
- •4.1.1 Способы получения
- •4.1.2. Химические свойства
- •4.1.3. Современные представления о строении моноциклоалканов.
- •4.2. Ароматические углеводороды
- •4.2.1. Строение бензола
- •4.2.2. Способы получения
- •4.2.3. Химические свойства
- •4.3.4. Правила ориентации в бензольном кольце
- •4.2.5. Механизм ориентирующего влияния заместителей
- •4.3. Многоядерные ароматические соединения с неконденсированными и конденсированными бензольными ядрами
- •4.3.1. Основные способы получения
- •4.3.2. Химические особенности
- •Функциональные производные углеводородов
- •Глава 5 галогенопроизводные
- •5.1. Галогенопроизводные: определение, изомерия, номенклатура
- •5.2. Способы получения
- •5..3 Химические свойства
- •Глава 6 кислородсодержащие органические соединения
- •6.1. Спирты: определение, изомерия, номенклатура
- •6.1.1. Способы получения
- •6.1.2 Физические свойства спиртов
- •6.1.3. Химические свойства
- •6.1.4 Понятие о непредельных и многоатомных спиртах
- •6.2. Фенолы: определение, изомерия, номенклатура
- •16.2.1. Способы получения
- •6.2.2. Химические свойства
- •6.3. Простые эфиры: определение, изомерия, номенклатура
- •6.3.1. Способы получения
- •6.3.2. Химические свойства
- •6.3.3. Окись этилена (эпоксисоединения)
- •6.4. Оксосоединения (альдегиды и кетоны)
- •6.4.1. Определение, изомерия и номенклатура оксосоединений
- •6.4.2. Способы получения
- •6.4.3. Химические свойства
- •6.4.4. Понятие о непредельных альдегидах и кетонах
- •6.4.5. Особенности получения и химические свойства хинонов
- •Задачи для самопроверки
- •6.5. Одно и многоосновные карбоновые кислоты и их производные: определение, изомерия, номенклатура
- •6.5.1. Способы получения
- •6.5.2. Химические свойства
- •6.5.3. Особенности предельных и непредельных кислот
- •Задачи для самопроверки
- •Глава 7. Серосодержащие соединения
- •7.1. Органические соединения двухвалентной серы (Тиолы, сульфиды, дисульфиды)
- •7.2. Сульфиновые кислоты и их производные
- •7.3. Сульфоновые кислоты и их производные. Сульфоны.
- •Глава 8. Азотсодержащие органические соединения
- •8.1 Нитросоединения: определение, изомерия, номенклатура.
- •8.1.1. Способы получения
- •8.1.2. Химические свойства
- •Задачи для самопроверки
- •8.2 Амины: определение, изомерия, номенклатура
- •8.2.1 Способы получения
- •8.2.2. Химические свойства
- •8.2.3. Понятие о диаминах
- •Задачи для самопроверки
- •8.3. Диазо- и азосоединения: определение, изомерия, номенклатура
- •8.3.1. Способы получения
- •8.3.2 Физические и химические свойства
- •II. Реакции без выделения азота
- •Задачи для самопроверки
- •Глава 9 . Гетерофункциональные соединеия
- •9.1. Гидроксикислоты: определение, изомерия, номенклатура
- •9.1.1. Способы получения
- •9.1.2. Химические свойства
- •9.1.3. Оптическая изомерия гидроксикислот
- •9.1.4. Ароматические гидроксикислоты и их производные
- •Задачи для самопроверки
- •9.2. Альдегидо- и кетокислоты: определение, изомерия, номенклатура
- •9.2.1. Способы получения
- •9.2.2. Химические особенности
- •9.2.3. Применение ацетоуксусного эфира в органическом синтезе
- •Задачи для самопроверки
- •9.3. Аминокислоты: определение, изомерия, номенклатура
- •9.3.1. Способы получения
- •9.3.2. Химические свойства
- •Задачи для самопроверки
- •Глава 10. Гетероциклические соединения
- •10.1. Определение и классификация гетероциклических соединений.
- •10.2. Пятичленные гетероциклические соединения: изомерия, номенклатура, ароматический характер.
- •10.2.1. Способы получения пятичленных гетероциклических соединений.
- •10.2.3. Химические свойства
- •10.3. Понятие о конденсированных гетероциклах (индол)
- •10.4. Шестичленные гетероциклические соединения: изомерия, номенклатура
- •10.4.1. Химические свойства.
- •Глава 11. Липиды
- •11.1.Определение, классификация изомерия, номенклатура
- •11.2. Простые липиды. (Жиры, масла)
- •10.3. Сложные липиды. Понятие о фосфолипидах.
- •10.4. Понятие о циклических липидах
- •Глава 12. Углеводы
- •12.1. Определение, классификация, изомерия, номенклатура.
- •12.2. Моносахариды: строение, оптическая изомерия.
- •12.3.Химические свойства моносахаридов.
- •12.4. Олигосахариды: особенности строения, химические свойства
- •12.5. Несахароподобные полисахариды: крахмал, гликоген, клетчатка.
- •Глава 13. Пептиды и белки
- •13.1. Протеиногенные аминокислоты
- •13.2. Понятие о строении пептидов.
- •13.3. Особенности строения белков
- •Глава 14. Нуклеиновые кислоты
- •14.1. Понятие о составе и строении нуклеиновых кислот
- •14.2. Классификация и биологическая роль нуклеиновых кислот
3.2.2 Химические свойства
Главным структурным элементом, определяющим реакционную способность алкенов, является двойная связь, представляющая собой сочетание σ- и π-связей (sp2-гибридизация). При сравнении структурных и энергетических параметров молекул алканов и алкенов видно, что двойная связь значительно короче и прочнее одинарной связи. Однако энергия двойной связи меньше, чем энергия двух ординарных, на 92,1 кДж/моль. Поэтому двойная связь легко переходит в две ординарные σ-связи путем присоединения по месту двойной связи двух атомов или атомных групп.
Таким образом, для олефинов наиболее типичны реакции присоединения. Однако следует иметь в виду, что олефины способны и к реакциям замещения, причем некоторые из них идут значительно легче, чем у парафинов (наиболее легко замещается водород у α-углеродного атома по отношению к двойной связи благодаря σ,π-сопряжению (сверхсопряжению). При разрыве таких СН-связей образуется радикал, стабилизированный сопряжением (см. главу 2).
В реакциях присоединения двойная связь обычно выступает как донор электронов. Поэтому для олефинов характерны реакции электрофильного присоединения (АЕ).
Гидрирование
Присоединение водорода к алкенам происходит только в присутствии катализаторов, как гетерогенных (Pt, Pd, Ni) так и гомогенных. Наиболее часто проводят каталитическое гидрирование на гетерогенных катализаторах:

этилен этан
Галогенирование
Олефины легко присоединяют галогены. Скорость реакции зависит от природы галогена и строения алкена. Фтор реагирует с воспламенением, иод – медленно на солнечном свету:

1,2-дибромэтан
Галогены могут присоединяться к олефинам по радикальному или ионному механизму.
При радикальном присоединении атома галогена, присоединение начинается к наиболее доступному из атомов углерода с образованием наиболее стабильного из возможных радикалов:
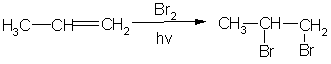
пропен 1,2-дибромпропан
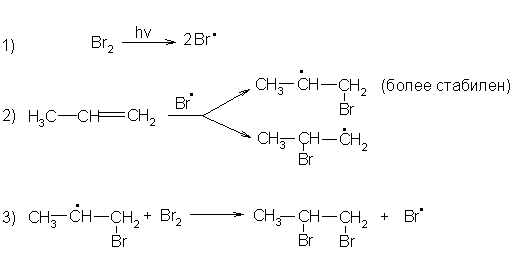
Чаще происходит присоединение по ионному электрофильному механизму. Молекула галогена атакует двойную связь, захватывая электроны и образуя так называемый π-комплекс. Затем отделятся отрицательный ион галогена. К возникшему карбониевому или бромониевому катиону присоединяется отрицательный ион галогена:
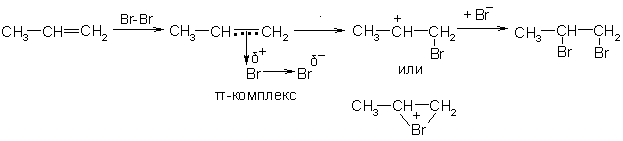
Реакция олефинов с галогенами служит для качественного и количественного определения их в смеси.
Присоединение галогеноводородов
Наиболее легко реагирует йодистый водород. Механизм электрофильного присоединения галогеноводородов двухступенчатый, как и механизм присоединения галогенов, однако π-комплексы в этом случае, вероятно, не образуются: реакция идет через карбониевые ионы. Присоединение галогеноводородов к несимметричным алкенам происходит в соответствии с правилом Марковникова: водород направляется преимущественно к наиболее гидрогенизированному углеродному атому. Такое направление присоединения идет за счет проявления эффекта сверхсопряжения:
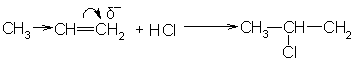
2-хлорпропан
Правило Марковникова соблюдается только при ионном механизме присоединения галогеноводородов. При радикальном механизме присоединение галогеноводорода происходит в обратном порядке – перекисный эффект Караша.
Перекись взаимодействует с галогеноводородом (НBr) и освобождает атом галогена, который и присоединяется по месту двойной связи к крайнему углеродному атому, образуя более стабильный радикал. Возникающий радикал продолжает реакционную цепь:
Н2О2 + 2HBr → 2Br• + 2H2O

пропен 1-бромпропан
Радикальное присоединение HF и HJ никогда не наблюдалось.
Гипогалогенирование
Присоединение к олефинам гипогалогенитных кислот и их эфиров также происходит по правилу Марковникова: более электроотрицательный гидроксил направляется преимущественно к наименее гидрогенизированному атому углерода:
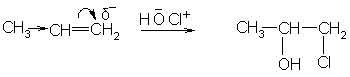
пропен 1-хлор-2-пропанол
Присоединение воды и серной кислоты
В присутствии катализаторов вода присоединяется по двойной связи по правилу Марковникова с образованием спиртов. Реакция идет по карбкатионному механизму:


Для получения спиртов часто используется поглощение олефинов концентрированной серной кислотой. При этом промежуточный карбкатион может реагировать как с содержащейся в кислоте водой с образованием спирта, так и с анионом серной кислоты с образованием алкилсерной кислоты:
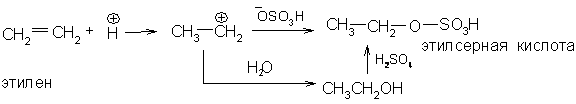
Окисление
Олефины окисляются кислородом воздуха или другими окислителями. Направление окисления зависит от условий реакции и выбора окислителя.
а) Алкены с кислородом воздуха без катализатора образуют гидропероксиды, распадающиеся с образованием спиртов и карбонильных соединений. Воздействию подвергается атом водорода у α-углеродного атома:
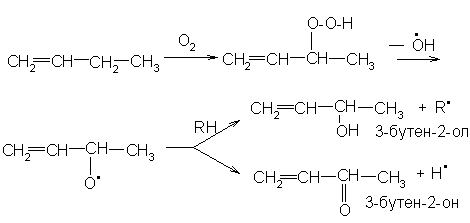
б) Кислородом воздуха в присутствии серебряного катализатора олефины окисляются до органических окисей (эпоксидов):
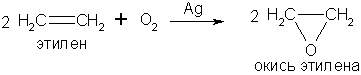
Аналогично действуют гидропероксиды ацилов (реакция Прилежаева)

В) Разбавленный раствор перманганата калия (реакция Вагнера) или пероксид водорода в присутствии катализаторов (Cr2O3, OsO4 и др) с олефинами образуют гликоли:
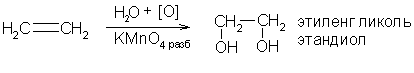
Г) При действии концентрированных растворов окислителей (перманганат калия, хромовая кислота, азотная кислота) молекула олефина разрывается по месту двойной связи образуя кетоны и кислоты:
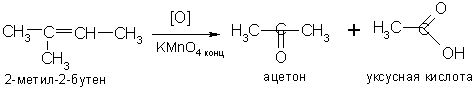
Д) При определении строения этиленовых углеводородов в качестве специфического окислителя используют озон – реакция озонирования Гарриеса (озонолиз). Озон присоединяется по месту двойной связи, образуя нестойкие, взрывчатые озониды, которые при обработке водой распадаются на пероксид водорода и карбонильные соединения:

Полимеризация
Одним из наиболее важных для современной техники превращений олефинов является реакция полимеризации.
Полимеризацией называют процесс образования высокомолекулярного вещества (полимера) путем соединения с помощью главных валентностей молекул исходного низкомолекулярного вещества (мономера).
Полимеризация алкенов может быть вызвана нагреванием, сверхвысоким давлением, облучением, действием свободных радикалов или катализаторов.
В реакцию полимеризации могут вступать как индивидуальные вещества, так и смеси мономеров. В последнем случае говорят о смешанной полимеризации – сополимеризации.
Полимеризация алкенов в зависимости от механизма может быть двух типов: радикальная или ионная.
Радикальная полимеризация вызывается (инициируется) веществами, способными в условиях реакции распадаться на свободные радикалы, а также действием теплоты, света. Растущая частица полимера вплоть до момента стабилизации представляет собой свободный радикал. Радикалы-инициаторы входят в состав молекул полимеров, образуя его концевую группу:
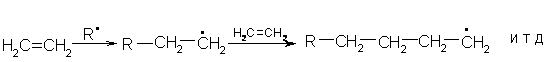
Обрыв цепи происходит при столкновении либо с молекулой регулятора цепи, примеси, стенками сосуда.
Каталитическая или ионная полимеризация может быть катионной или анионной.
Катализаторами катионной полимеризации являются кислоты, хлориды алюминия, бора и т.д. При катионной полимеризации катализатор обычно регенерируется и не входит в состав полимера. Процесс может иметь цепной характер и протекать с очень большой скоростью. Поэтому ионную полимеризацию проводят при низких температурах.
Механизм катионной полимеризации этилена в присутствии AlCl3 и следов НСl можно представить следующим образом:
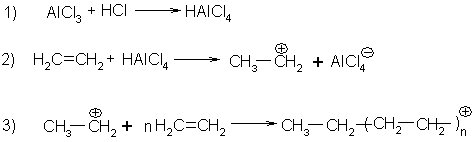
Обрыв цепи может произойти вследствие захвата растущим катионом аниона или потерей протона и образованием концевой двойной связи.
Катализаторами анионной полимеризации служат щелочные металлы, их амиды, металлоорганические соединения и т.д.
Механизм анионной полимеризации под влиянием металлалкилов можно представить следующим образом:

На реакцию полимеризации сильное влияние оказывает присутствие в мономере ничтожных примесей. Некоторые примеси, например многоатомные фенолы, ароматические амины, хиноны, способны задерживать полимеризацию. Такие вещества называются ингибиторами (замедлителями). Ингибиторы используются при хранении и транспортировке мономеров.
Промышленное значение имеет полимеризация этилена и пропилена в присутствии триэтилалюминия.
ЗАДАЧИ ДЛЯ САМОПРОВЕРКИ
1. При взаимодействии 20 г 3-бромпентана со спиртовым раствором гидроксида калия с последующей очисткой было получено 8 г цис-изомера непредельного углеводорода. Написать уравнение реакции и определить выход целевого продукта.
2. При взаимодействии 38 г 2-бром-3-метилбутана со спиртовым раствором гидроксида калия с последующей очисткой было получено 10 г непредельного углеводорода. Написать уравнение реакции и определить выход целевого продукта.
3. При обработке 15 дм3 (при н. у.) газообразной смеси этана и пропилена хлором было получено 25 г 1,2-дихлорпропана. Определить объемную долю (в %) пропилена в смеси.
4. Смесь пропана и пропилена объемом 300 см3 (н. у.) пропустили через раствор йода, получив при этом 3 г 1,2-дийодпропана. Рассчитать объемную долю (%) пропана в смеси.
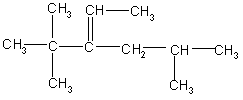
5. Написать структурную формулу 2,5,5,6-тетраметил-3-октена.

6.Назовите углеводород по международной номенклатуре