
- •Глава 1 введение
- •1.2 Основные сырьевые источники органических соединений
- •1.3 Классификация органических соединений
- •1.4 Номенклатура органических соединений
- •1.4.1 Тривиальная номенклатура
- •1.4.2 Рациональная номенклатура
- •1.4.3 Номенклатура июпак
- •1.4.3.1. Номенклатура июпак для алифатических углеводородов.
- •Глава 2 теоретические представления в органической химии
- •2.1 Типы химических связей
- •2.2 Образование ковалентных связей атомами углерода (σ- и π-ковалентные связи)
- •2.3 Общие представления о механизмах химических реакций
- •2.3.1 Свободнорадикальные реакции
- •2.3.2 Ионные реакции
- •2.4 Пространственное расположение атомов в молекуле. Конформация молекул
- •Глава 3 алифатические углеводороды алканы,алкены, алкины и алкадиены
- •3.1 Алканы: определениек,изомерия и номенклатура
- •3.1.2 Способы получения алканов
- •3.1.3 Химические свойства
- •Радикальное галогенирование
- •Нитрование
- •Сульфирование, сульфоокисление, сульфохлорирование
- •Окисление
- •Крекинг углеводородов при высоких температурах
- •Задачи для самопроверки
- •3.2 Алкены: определение, изомерия, номенклатура
- •3.2.1 Способы получения
- •3.2.2 Химические свойства
- •3.3. Алкадиены: определение, изомерия, номенклатура
- •3.3.1 Способы получения важнейших диенов
- •3.3.2 Химические особенности 1,3-алкадиенов
- •3.4. Алкины: определение, изомерия, номенклатура
- •3.4.1. Способы получения.
- •3.4.2. Химические свойства
- •Глава 4 карбоциклические соединения
- •4.1. Алициклический ряд: определение, изомерия, номенклатура
- •4.1.1 Способы получения
- •4.1.2. Химические свойства
- •4.1.3. Современные представления о строении моноциклоалканов.
- •4.2. Ароматические углеводороды
- •4.2.1. Строение бензола
- •4.2.2. Способы получения
- •4.2.3. Химические свойства
- •4.3.4. Правила ориентации в бензольном кольце
- •4.2.5. Механизм ориентирующего влияния заместителей
- •4.3. Многоядерные ароматические соединения с неконденсированными и конденсированными бензольными ядрами
- •4.3.1. Основные способы получения
- •4.3.2. Химические особенности
- •Функциональные производные углеводородов
- •Глава 5 галогенопроизводные
- •5.1. Галогенопроизводные: определение, изомерия, номенклатура
- •5.2. Способы получения
- •5..3 Химические свойства
- •Глава 6 кислородсодержащие органические соединения
- •6.1. Спирты: определение, изомерия, номенклатура
- •6.1.1. Способы получения
- •6.1.2 Физические свойства спиртов
- •6.1.3. Химические свойства
- •6.1.4 Понятие о непредельных и многоатомных спиртах
- •6.2. Фенолы: определение, изомерия, номенклатура
- •16.2.1. Способы получения
- •6.2.2. Химические свойства
- •6.3. Простые эфиры: определение, изомерия, номенклатура
- •6.3.1. Способы получения
- •6.3.2. Химические свойства
- •6.3.3. Окись этилена (эпоксисоединения)
- •6.4. Оксосоединения (альдегиды и кетоны)
- •6.4.1. Определение, изомерия и номенклатура оксосоединений
- •6.4.2. Способы получения
- •6.4.3. Химические свойства
- •6.4.4. Понятие о непредельных альдегидах и кетонах
- •6.4.5. Особенности получения и химические свойства хинонов
- •Задачи для самопроверки
- •6.5. Одно и многоосновные карбоновые кислоты и их производные: определение, изомерия, номенклатура
- •6.5.1. Способы получения
- •6.5.2. Химические свойства
- •6.5.3. Особенности предельных и непредельных кислот
- •Задачи для самопроверки
- •Глава 7. Серосодержащие соединения
- •7.1. Органические соединения двухвалентной серы (Тиолы, сульфиды, дисульфиды)
- •7.2. Сульфиновые кислоты и их производные
- •7.3. Сульфоновые кислоты и их производные. Сульфоны.
- •Глава 8. Азотсодержащие органические соединения
- •8.1 Нитросоединения: определение, изомерия, номенклатура.
- •8.1.1. Способы получения
- •8.1.2. Химические свойства
- •Задачи для самопроверки
- •8.2 Амины: определение, изомерия, номенклатура
- •8.2.1 Способы получения
- •8.2.2. Химические свойства
- •8.2.3. Понятие о диаминах
- •Задачи для самопроверки
- •8.3. Диазо- и азосоединения: определение, изомерия, номенклатура
- •8.3.1. Способы получения
- •8.3.2 Физические и химические свойства
- •II. Реакции без выделения азота
- •Задачи для самопроверки
- •Глава 9 . Гетерофункциональные соединеия
- •9.1. Гидроксикислоты: определение, изомерия, номенклатура
- •9.1.1. Способы получения
- •9.1.2. Химические свойства
- •9.1.3. Оптическая изомерия гидроксикислот
- •9.1.4. Ароматические гидроксикислоты и их производные
- •Задачи для самопроверки
- •9.2. Альдегидо- и кетокислоты: определение, изомерия, номенклатура
- •9.2.1. Способы получения
- •9.2.2. Химические особенности
- •9.2.3. Применение ацетоуксусного эфира в органическом синтезе
- •Задачи для самопроверки
- •9.3. Аминокислоты: определение, изомерия, номенклатура
- •9.3.1. Способы получения
- •9.3.2. Химические свойства
- •Задачи для самопроверки
- •Глава 10. Гетероциклические соединения
- •10.1. Определение и классификация гетероциклических соединений.
- •10.2. Пятичленные гетероциклические соединения: изомерия, номенклатура, ароматический характер.
- •10.2.1. Способы получения пятичленных гетероциклических соединений.
- •10.2.3. Химические свойства
- •10.3. Понятие о конденсированных гетероциклах (индол)
- •10.4. Шестичленные гетероциклические соединения: изомерия, номенклатура
- •10.4.1. Химические свойства.
- •Глава 11. Липиды
- •11.1.Определение, классификация изомерия, номенклатура
- •11.2. Простые липиды. (Жиры, масла)
- •10.3. Сложные липиды. Понятие о фосфолипидах.
- •10.4. Понятие о циклических липидах
- •Глава 12. Углеводы
- •12.1. Определение, классификация, изомерия, номенклатура.
- •12.2. Моносахариды: строение, оптическая изомерия.
- •12.3.Химические свойства моносахаридов.
- •12.4. Олигосахариды: особенности строения, химические свойства
- •12.5. Несахароподобные полисахариды: крахмал, гликоген, клетчатка.
- •Глава 13. Пептиды и белки
- •13.1. Протеиногенные аминокислоты
- •13.2. Понятие о строении пептидов.
- •13.3. Особенности строения белков
- •Глава 14. Нуклеиновые кислоты
- •14.1. Понятие о составе и строении нуклеиновых кислот
- •14.2. Классификация и биологическая роль нуклеиновых кислот
7.2. Сульфиновые кислоты и их производные
Сульфиновые кислоты и сульфоксиды можно рассматривать как производные сернистой кислоты, в которой одна или две гидроксильные группы замещены радикалом:

Способы получения
1. Сульфиновые кислоты получают мягким восстановлением сульфонилхлоридов

Общий метод получения сульфиновых кислот заключается в реакции металлорганических соединений с диоксидом серы:

2. Сульфокисды получают окислением сульфидов разбавленной азотной кислотой или оксидами азота:
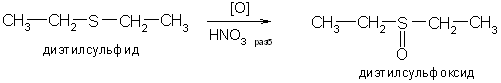
Химические свойства
1. Сульфиновые кислоты – слабые кислоты, способные ионизироваться в водных растворах и образовывать соли
![]()
Сульфиновые кислоты являются нестабильными соединениями. Они легко окисляются до сульфоновых кислот
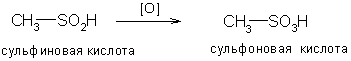
При алкилировании сульфинат-иона образуются два изомерных продукта: эфир сульфиновой кислоты и сульфон, так как сульфинат-ион является амбидентным анионом с двумя реакционными центрами
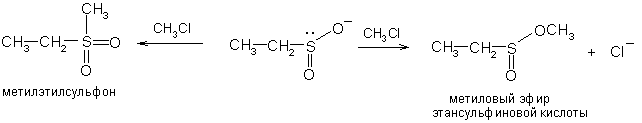 2.
Сульфоксиды обладают как свойствами
слабых оснований так и очень слабых
СН-кислот
2.
Сульфоксиды обладают как свойствами
слабых оснований так и очень слабых
СН-кислот
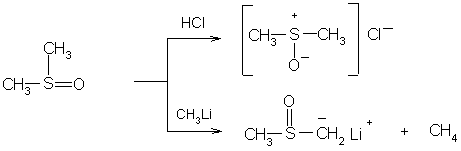
При действии металлорганических соединений образуется стабилизированный карбанион.
7.3. Сульфоновые кислоты и их производные. Сульфоны.
Сульфоновые кислоты и сульфоны можно рассматривать как производные серной кислоты, в молекуле которой одна или обе гидроксильные группы замещены радикалами. Производными сульфоновых кислот являются их эфиры, амиды, хлорангидриды.
Названия этих соединений образуют от названия соответствующих углеводородов и серосодержащей функциональной группы. Номенклатура ИЮПАК рекомендует образовывать названия на основе сульфоновой кислоты. Часто употребляется также название сульфокислоты:
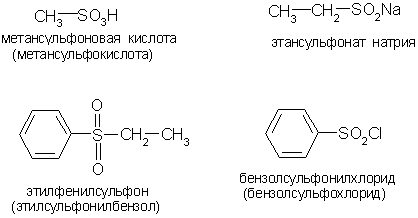
Способы получения
1. В промышленности алифатические и алициклические сульфоновые кислоты получают фотохимическим сульфированием соответствующих углеводородов; ароматические сульфоновые кислоты получают действием концентрированной серной кислоты или олеума на ароматические углеводороды:
![]()
(см. свойства предельных и ароматических углеводородов)
2. Получение сульфонов
2.1) Сульфоны образуются в качестве побочных продуктов в реакциях сульфирования. При повышении температуры реакции и использовании более эффективных сульфирующих реагентов удается получить диарилсульфоны:

2.2) Сульфоны легко образуются в реакции сульфонилирования (аналогично реакции Фриделя-Крафтса)

2.3) Сульфоны конечные продукты окисления сульфидов (см. свойства сульфидов)
Физические и химические свойства
Сульфокислоты – бесцветные кристаллические вещества. Гигроскопичны. Низшие представители легко растворимы в воде. По химическим свойствам они аналогичны серной кислоте. Наиболее сильной является трифторметансульфоновая кислота СF3SO3H.
Из производных сульфоновых кислот наибольший интерес представляют соли, сульфонилхлориды, эфиры и амиды:
1) Соли сульфокислот получают обычной реакцией нейтрализации:

2) Хлорангидриды получают либо реакцией сульфохлорирования алканов, либо действием на сульфоновые кислоты PCl5:

3) Эфиры могут быть получены этерификацией сульфоновых кислот или их галогенангидридов:

4) Сульфониламиды образуются при действии на сульфонилхлориды аммиака:
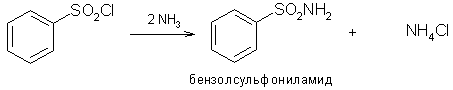
Примечание: Соли высших предельных и непредельных сульфоновых кислот применяются как поверхностно-активные вещества. Сульфохлориды применяются в кожевенной и текстильной промышленности. Сульфоамиды используются в промышленности как эмульгаторы, как поверхностно-активные вещества при обработке металлов, для изготовления отбеливающих средств и т.д.
Эфиры сульфоновых кислот хорошие алкилирующие средства.
5) Ароматические сульфоновые кислоты способны к реакциям замещения сульфогруппы:
5.1) Гидролиз. При действии перегретого пара в кислой среде сульфоновые кислоты дают исходные ароматические углеводороды
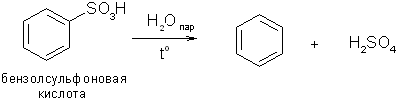
5.2) Реакция щелочного плава. При сплавлении солей сульфоновых кислот с едкими щелочами образуются феноляты.
Это важнейший процесс получения полупродуктов в промышленности красителей:

5.3) При сплавлении солей сульфокислот с цианидами получаются нитрилы
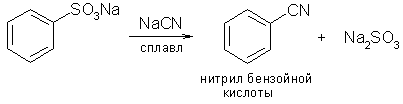
6) Реакции бензольного кольца (см. главу ароматические углеводороды).
Задачи для самопроверки
1. Назовите следующие соединения:
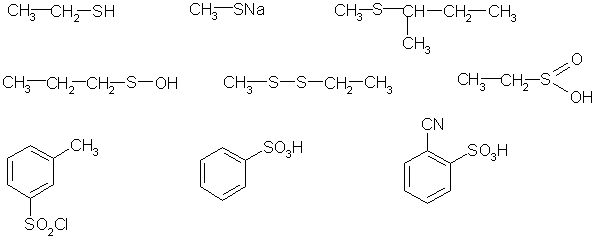
2. Получите из соответствующих галогенопроизводных бутантиол, диметилсульфид, бензолсульфоновую кислоту.
3. Получите этантиол любым способом и напишите для него реакции с едким натром, слабым и сильным окислителем.
4. Напишите уравнения реакций получения иприта (дихлордиэтилсульфида) из окиси этилена. Для иприта напишите реакцию с СаСОСl2.
5. Напишите уравнения реакции сульфохлорирования и сульфоокисления 2-метилгексана. Распишите механизм фотохимического сульфохлорирования.
6. Опишите механизм сульфирования ароматических колец на примере сульфирования нитробензола и толуола. В каком случае реакция протекает в более мягких условиях?
7. Соединение состава С7Н8SO3 при взаимодействии с PCl5 превращается в соединение C7H7SO2Cl, при перегонке с водяным паром (в присутствии H2SO4) – в С7Н8, а при сплавлении с КОН образует n-крезол. Напишите структурную формулу исходного соединения и все перечисленные реакции.
