
- •Глава 1 введение
- •1.2 Основные сырьевые источники органических соединений
- •1.3 Классификация органических соединений
- •1.4 Номенклатура органических соединений
- •1.4.1 Тривиальная номенклатура
- •1.4.2 Рациональная номенклатура
- •1.4.3 Номенклатура июпак
- •1.4.3.1. Номенклатура июпак для алифатических углеводородов.
- •Глава 2 теоретические представления в органической химии
- •2.1 Типы химических связей
- •2.2 Образование ковалентных связей атомами углерода (σ- и π-ковалентные связи)
- •2.3 Общие представления о механизмах химических реакций
- •2.3.1 Свободнорадикальные реакции
- •2.3.2 Ионные реакции
- •2.4 Пространственное расположение атомов в молекуле. Конформация молекул
- •Глава 3 алифатические углеводороды алканы,алкены, алкины и алкадиены
- •3.1 Алканы: определениек,изомерия и номенклатура
- •3.1.2 Способы получения алканов
- •3.1.3 Химические свойства
- •Радикальное галогенирование
- •Нитрование
- •Сульфирование, сульфоокисление, сульфохлорирование
- •Окисление
- •Крекинг углеводородов при высоких температурах
- •Задачи для самопроверки
- •3.2 Алкены: определение, изомерия, номенклатура
- •3.2.1 Способы получения
- •3.2.2 Химические свойства
- •3.3. Алкадиены: определение, изомерия, номенклатура
- •3.3.1 Способы получения важнейших диенов
- •3.3.2 Химические особенности 1,3-алкадиенов
- •3.4. Алкины: определение, изомерия, номенклатура
- •3.4.1. Способы получения.
- •3.4.2. Химические свойства
- •Глава 4 карбоциклические соединения
- •4.1. Алициклический ряд: определение, изомерия, номенклатура
- •4.1.1 Способы получения
- •4.1.2. Химические свойства
- •4.1.3. Современные представления о строении моноциклоалканов.
- •4.2. Ароматические углеводороды
- •4.2.1. Строение бензола
- •4.2.2. Способы получения
- •4.2.3. Химические свойства
- •4.3.4. Правила ориентации в бензольном кольце
- •4.2.5. Механизм ориентирующего влияния заместителей
- •4.3. Многоядерные ароматические соединения с неконденсированными и конденсированными бензольными ядрами
- •4.3.1. Основные способы получения
- •4.3.2. Химические особенности
- •Функциональные производные углеводородов
- •Глава 5 галогенопроизводные
- •5.1. Галогенопроизводные: определение, изомерия, номенклатура
- •5.2. Способы получения
- •5..3 Химические свойства
- •Глава 6 кислородсодержащие органические соединения
- •6.1. Спирты: определение, изомерия, номенклатура
- •6.1.1. Способы получения
- •6.1.2 Физические свойства спиртов
- •6.1.3. Химические свойства
- •6.1.4 Понятие о непредельных и многоатомных спиртах
- •6.2. Фенолы: определение, изомерия, номенклатура
- •16.2.1. Способы получения
- •6.2.2. Химические свойства
- •6.3. Простые эфиры: определение, изомерия, номенклатура
- •6.3.1. Способы получения
- •6.3.2. Химические свойства
- •6.3.3. Окись этилена (эпоксисоединения)
- •6.4. Оксосоединения (альдегиды и кетоны)
- •6.4.1. Определение, изомерия и номенклатура оксосоединений
- •6.4.2. Способы получения
- •6.4.3. Химические свойства
- •6.4.4. Понятие о непредельных альдегидах и кетонах
- •6.4.5. Особенности получения и химические свойства хинонов
- •Задачи для самопроверки
- •6.5. Одно и многоосновные карбоновые кислоты и их производные: определение, изомерия, номенклатура
- •6.5.1. Способы получения
- •6.5.2. Химические свойства
- •6.5.3. Особенности предельных и непредельных кислот
- •Задачи для самопроверки
- •Глава 7. Серосодержащие соединения
- •7.1. Органические соединения двухвалентной серы (Тиолы, сульфиды, дисульфиды)
- •7.2. Сульфиновые кислоты и их производные
- •7.3. Сульфоновые кислоты и их производные. Сульфоны.
- •Глава 8. Азотсодержащие органические соединения
- •8.1 Нитросоединения: определение, изомерия, номенклатура.
- •8.1.1. Способы получения
- •8.1.2. Химические свойства
- •Задачи для самопроверки
- •8.2 Амины: определение, изомерия, номенклатура
- •8.2.1 Способы получения
- •8.2.2. Химические свойства
- •8.2.3. Понятие о диаминах
- •Задачи для самопроверки
- •8.3. Диазо- и азосоединения: определение, изомерия, номенклатура
- •8.3.1. Способы получения
- •8.3.2 Физические и химические свойства
- •II. Реакции без выделения азота
- •Задачи для самопроверки
- •Глава 9 . Гетерофункциональные соединеия
- •9.1. Гидроксикислоты: определение, изомерия, номенклатура
- •9.1.1. Способы получения
- •9.1.2. Химические свойства
- •9.1.3. Оптическая изомерия гидроксикислот
- •9.1.4. Ароматические гидроксикислоты и их производные
- •Задачи для самопроверки
- •9.2. Альдегидо- и кетокислоты: определение, изомерия, номенклатура
- •9.2.1. Способы получения
- •9.2.2. Химические особенности
- •9.2.3. Применение ацетоуксусного эфира в органическом синтезе
- •Задачи для самопроверки
- •9.3. Аминокислоты: определение, изомерия, номенклатура
- •9.3.1. Способы получения
- •9.3.2. Химические свойства
- •Задачи для самопроверки
- •Глава 10. Гетероциклические соединения
- •10.1. Определение и классификация гетероциклических соединений.
- •10.2. Пятичленные гетероциклические соединения: изомерия, номенклатура, ароматический характер.
- •10.2.1. Способы получения пятичленных гетероциклических соединений.
- •10.2.3. Химические свойства
- •10.3. Понятие о конденсированных гетероциклах (индол)
- •10.4. Шестичленные гетероциклические соединения: изомерия, номенклатура
- •10.4.1. Химические свойства.
- •Глава 11. Липиды
- •11.1.Определение, классификация изомерия, номенклатура
- •11.2. Простые липиды. (Жиры, масла)
- •10.3. Сложные липиды. Понятие о фосфолипидах.
- •10.4. Понятие о циклических липидах
- •Глава 12. Углеводы
- •12.1. Определение, классификация, изомерия, номенклатура.
- •12.2. Моносахариды: строение, оптическая изомерия.
- •12.3.Химические свойства моносахаридов.
- •12.4. Олигосахариды: особенности строения, химические свойства
- •12.5. Несахароподобные полисахариды: крахмал, гликоген, клетчатка.
- •Глава 13. Пептиды и белки
- •13.1. Протеиногенные аминокислоты
- •13.2. Понятие о строении пептидов.
- •13.3. Особенности строения белков
- •Глава 14. Нуклеиновые кислоты
- •14.1. Понятие о составе и строении нуклеиновых кислот
- •14.2. Классификация и биологическая роль нуклеиновых кислот
9.1.2. Химические свойства
Гидроксикислоты, являясь гетерофункциональными соединениями, способны реагировать по каждой функциональной группе в отдельности или одновременно, сохраняя типичную реакционную способность.
1. В качестве кислот они дают соли, сложные эфиры, амиды, галогенангидриды и т.д.

2. Как спирты, они образуют алкоголяты, простые и сложные эфиры, замещают гидроксил галогеном

3. Какая из групп реагирует определяется природой реагента и условиями проведения реакции. Например:

4. Вместе с тем в свойствах гидроксикислот сказывается влияние функциональных групп друг на друга. Одна из наиболее характерных реакций такого типа происходит при нагревании гидроксикислот, причем превращение идет по разному, в зависимости от взаимного расположения гидроксила и карбонила:
А) α-гидроксикислоты при нагревании отщепляют воду с образованием лактидов, т.е. циклических сложных эфиров, построенных из двух молекул гидроксикислоты:
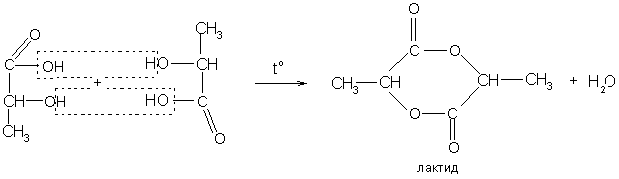
Б) β-гидроксикислоты легко теряют при нагревании воду, переходя в непредельные кислоты:
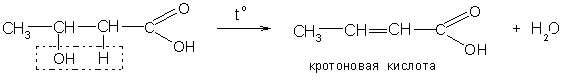
В) При нагревании - и δ-оксикислот отщепляется вода и образуются внутренние сложные эфиры – лактоны:
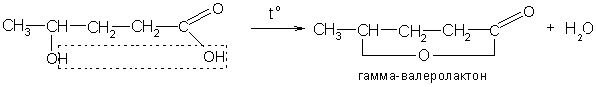
В случае гидроксикислот с более далеким расположением функциональных групп, взаимное влияние их не проявляется.
5. α-Гидроксикислоты легко восстанавливаются в карбоновые кислоты:
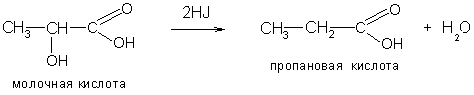
6. При кипячении с разбавленными минеральными кислотами α-гидроксикислоты расщепляются с выделением муравьиной кислоты:
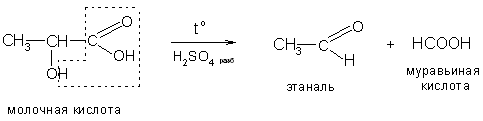
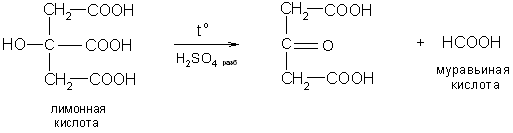
7. При действии серной кислоты, лимонная кислота ведет себя как α-гидроксикислота: отщепляет муравьиную кислоту и дает ацетондикарбоновую кислоту:
9.1.3. Оптическая изомерия гидроксикислот
Одним из видов пространственной изомерии, или стереоизомерии, органических соединений, и в том числе оксикислот, является оптическая изомерия. Ее существование можно понять при рассмотрении тетраэдрической модели. Тетраэдр, в вершинах которого находятся разные заместители, не имеет ни одного элемента симметрии. Атом углерода, связанный с четырьмя разными заместителями называют асимметрическим атомом углерода.
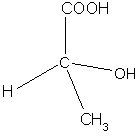
Например:
одно из простейших оптически активных
веществ – молочная кислота
![]() существует
в трех формах: правовращающая –
обозначается знаком (+) перед формулой,
левовращающая – знаком (−) и оптически
неактивная – знаком ()
или (±). Молочная кислота содержит
асимметрический атом углерода и для
нее возможны две формы (два изомера)
молекулы, которые нельзя совместить в
пространстве и которые относятся друг
к другу как предмет к своему изображению
в зеркале и называются стереоизомерами,
а молекулы такого типа называются
хиральными.
существует
в трех формах: правовращающая –
обозначается знаком (+) перед формулой,
левовращающая – знаком (−) и оптически
неактивная – знаком ()
или (±). Молочная кислота содержит
асимметрический атом углерода и для
нее возможны две формы (два изомера)
молекулы, которые нельзя совместить в
пространстве и которые относятся друг
к другу как предмет к своему изображению
в зеркале и называются стереоизомерами,
а молекулы такого типа называются
хиральными.

Такие стереоизомеры одинаковы по физическим и химическим свойствам и отличаются друг от друга только отношением к плоскополяризованному свету: они вращают его плоскость поляризации на одинаковую величину, но в противоположных направлениях. Кроме того, асимметрия молекул двух оптических изомеров часто проявляется в образуемых ими кристаллах, также относящихся друг к другу как предмет и его зеркальное изображение. Это свойство, позволило Луи Пастеру открыть явление оптической изомерии: обнаружив два типа кристаллов соли виноградной кислоты. Он разделил их и получил чистые изомеры.
Пару зеркальных изомеров, отличающихся друг от друга как предмет и его отражение в зеркале, называют оптическими антиподами.
Способность веществ вращать плоскость поляризации света называется оптической активностью. Для ее измерения пользуются прибором – поляриметром.
Молочная кислота, вращающая плоскость поляризации света вправо, содержится в мышцах животных.
Молочная кислота, вращающая плоскость поляризации света влево, образуется при ферментации сахарозы с помощью бактерий Bacillus acidi laevolactici.
Молочная кислота, полученная из кислого молока или синтетически, не вращает плоскость поляризации света. Эта кислота состоит из смеси равных количеств право- и левовращающих форм и называется рацематом.
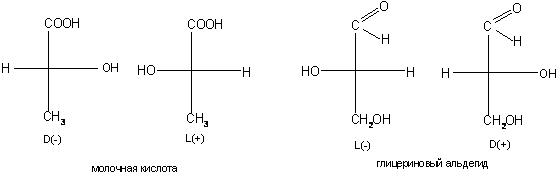
Оптические изомеры изображаются с помощью проекционных формул Фишера. Эти формулы представляют собой проекции тетраэдрических моделей соответствующих молекул на плоскость чертежа. В этих формулах углеродная цепь располагается вертикально, причем группа наиболее отличная от метильной записывается вверху. Асимметрические атомы углерода не обозначаются символами, а только пересечением связей, по концам которых записываются соответствующие заместители.

Обозначения D− и L− в названиях оксикислот указывают условно их конфигурацию, т.е. пространственное расположение заместителей вокруг асимметрического атома углерода Обозначение D- получают те оксикислоты, у которых гидроксильная группа в проекционной формуле Фишера стоит справа; обозначение L – ставится, если гидроксильная группа в проекционной формуле оказывается слева.
Между направлениями вращения и конфигурацией асимметрического центра нет прямой зависимости
В молекуле винной кислоты имеется два одинаковых асимметрических атома углерода.
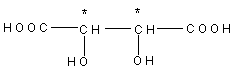
Общая формула расчета количества оптических изомеров N=2n, где n – число асимметрических атомов углерода. Таким образом, для винной кислоты можно ожидать существование четырех оптически деятельных изомеров и двух рацематов. Эти изомеры винной кислоты можно изобразить следующими проекционными формулами:

Если первые два изомера (1); (2) обладают оптической активностью, а их проекции при повороте на 1800 не совпадают, то изомеры 3 и 4 не обладают оптической активностью и их проекции при повороте на 180о совпадают, следовательно вещества (3) и (4) идентичны. Стереоизомер 3 недеятелен вследствие внутренней компенсации вращения. Вращение, вызываемое верхним тетраэдром, уничтожается противоположным по знаку и равным по величине вращением, обусловленным нижним тетраэдром. Следовательно, могут существовать соединения с асимметрическими углеродными атомами, но оптически недеятельные вследствие симметрии молекулы. Таким образом, необходимым и достаточным признаком оптической активности молекулы является ее несимметричное строение.
Первые две винные кислоты называются (+)- и (-)-винными кислотами, изомер (3) называется мезовинной кислотой, рацемат из первых двух изомеров – виноградной кислотой. (+)- и (-)-винные кислоты – оптические антиподы. По отношению к этим кислотам мезовинная кислота является диастереомером (но не их антиподом). Диастереомерами называются стереоизомеры молекул с несколькими асимметрическими атомами углерода имеющие больше различий, чем предмет и его зеркальное отражение, а следовательно и больше различий в физических свойствах.
Методы разделения рацематов на оптические антиподы
Синтетические методы получения органических соединений обычно дают рацемическую смесь. Между тем в ряде случаев требуется выделение какого-либо антипода. Это относится к синтезу лекарственных и биоактивных веществ, так как живые организмы совершенно по-разному реагируют на антиподы. Поэтому большой практический интерес представляют методы разделения рацематов на оптические антиподы. Это разделение представляет и большой теоретический интерес, так как является важным средством установления строения и конфигурации органических соединений.
Существуют три главных классических метода разделения рацематов на оптические изомеры. Все они разработаны Луи Пастером в середине XIX столетия. Широкое применение имеет третий метод. Два первых представляют только исторический интерес.
Механический отбор. При определенных условиях соли рацемической смеси кислот кристаллизуются в виде правой и левой форм отдельно, причем их кристаллы по форме относятся один к другому как предмет к зеркальному отражению.
Биологический отбор. Различные микроорганизмы способны потреблять в процессе жизнедеятельности какую-либо одну из оптически активных форм, обычно ту, которая более распространена в природе. Другая форма остается в чистом виде и может быть выделена из остатка. Микроорганизмы ее используют только после того, как первый изомер будет полностью израсходован.
Кристаллизация диастереомеров. Диастереомеры имеют различия в физических свойствах Например, они обладают различной растворимостью. Метод сводится к тому, что из смеси оптических антиподов получают смесь диастереомеров, которую и раскристаллизовывают. Так, действуя на смесь антиподов какой-либо кислоты оптически активным основанием, получают две соли, представляющие собой диастереомеры. После разделения диастереомерных солей из них выделяют оптические антиподы под действием более сильной кислоты:
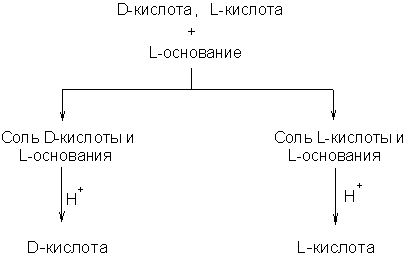
В качестве основания берут сложные гетероциклические соединения: бруцин, цинкохинон, стрихнин.
