
- •В.И. Вершинин, т.В. Антонова, с.В. Усова
- •По аналитической химии
- •Часть 1
- •Издание ОмГу Омск 1998
- •1. Введение для преподавателей
- •2. Правила безопасной работы в лаборатории аналитической химии
- •3. Правила взвешивания на двухчашечных демпферных аналитических весах 2
- •4. Оформление отчетов по лабораторным работам
- •5. Лабораторные работы по химическим методам анализа
- •5.1. Гравиметрическое определение железа Методические указания к лабораторной работе № 1
- •5.2. Аргентометрическое определение галогенидов Методические указания к лабораторной работе № 2
- •А. Стандартизация раствора AgNOз
- •Б. Титрование по методу Мора
- •В. Титрование по методу Фаянса
- •Г. Титрование по методу Фольгарда
- •Д. Выполнение контрольной задачи
- •5.3. Кислотно-основное титрование сильных электролитов Методические указания к лабораторной работе № 3
- •А. Приготовление раствора нCl и его стандартизация методом пипетирования
- •Б. Приготовление раствора NаOh, стандартизация его методом отдельных навесок
- •В. Проверка правильности стандартизации растворов нСl и NaOh
- •5.4. Кислотно - основное титрование слабых электролитов Методические указания к лабораторной работе № 4
- •А. Определение концентрации ледяной уксусной кислоты
- •Б. Определение концентрации водного раствора аммиака
- •В. Определение содержаний карбоната и бикарбоната натрия в их смеси
- •Г. Раздельное определение соляной и борной кислот в смеси. Метод замещения
- •Д. Определение содержания аммонийного азота в солях аммония
- •5.5. Кислотно - основное титрование в неводных средах Методические указания к лабораторной работе № 5
- •Краткие теоретические сведения
- •А. Стандартизация раствора нСlO4в сн3соон
- •Б. Определение концентрации анилина
- •В. Определение состава смеси ацетата и хлорида натрия
- •5.6. Комплексонометрическое титрование Методические указания к лабораторной работе № 6
- •А. Стандартизация рабочего раствора комплексона III по фиксаналу MgSo4
- •Б. Способы установления конечной точки титрования
- •В. Определение общей и кальциевой жесткости воды
- •Г. Способы проведения комплексонометрических титрований
- •Сравнение результатов при титровании разными способами
- •Д. Комплексонометрическое титрование многокомпонентных систем
- •5.7. Перманганатометрическое титрование Методические указания к лабораторной работе № 7
- •А. Стандартизация раствора kMnO4
- •Б. Определение содержания Fe (II) в соли Мора
- •5.8. Хроматометрическое титрование Методические указания к лабораторной работе № 8
- •А. Приготовление рабочего раствора. Прямое титрование восстановителей
- •Б. Определение неустойчивых восстановителей (SnCi2) по методу замещения
- •В. Определение окислителей по методу обратного титрования
- •5.9. Иодометрия Методические указания к лабораторной работе № 9
- •А. Стандартизация рабочего раствора иода
- •Б. Определение концентрации раствора Na2so3методом обратного титрования
- •В. Определение концентрации ионов меди (II) по способу замещения
- •Г. Иодометрическое определение кислот
- •Д. Определение концентрации перекиси водорода по методу замещения
- •6. Материалы для подготовки к практическим занятиям
- •6.1. Правила записи исходных данных и расчет результатов. Использование констант
- •Практическое занятие № 1
- •Оценка погрешности результатов расчета и правила их записи.
- •Примеры решения типовых задач
- •Контрольные вопросы
- •6.2. Расчет гетерогенного равновесия “осадок - раствор” Практическое занятие № 2 Теоретические сведения
- •Расчет возможности осаждения при добавлении реагента-осадителя.
- •Примеры решения типовых задач
- •Контрольные вопросы
- •6.3. Расчеты протолитических равновесий Практическое занятие № 3
- •Теоретические сведения
- •Примеры расчетов
- •Контрольные вопросы
- •6.4. Расчеты равновесий комплексообразования Практическое занятие № 4 Теоретические сведения
- •Расчет концентрации свободных ионов металла в отсутствие избытка лиганда
- •Расчеты закомплексованности и маскирования при введении избытка лиганда
- •Определение степени образования различных комплексов в их смеси
- •Примеры решения типовых задач
- •Контрольные вопросы
- •6.5. Расчет результатов титриметрического анализа Практическое занятие № 5 Теоретические сведения
- •Расчет результатов прямого или заместительного титрования
- •Расчет результатов обратного титрования
- •Другие способы расчета
- •Точность результатов титриметрического анализа
- •Примеры решения типовых задач
- •Контрольные вопросы
- •6.6. Статистическая обработка данных. Вычисление и использование доверительных интервалов Практическое занятие № 6 Теоретические сведения
- •Примеры типовых расчетов
- •Контрольные вопросы
- •7. Задачи для самостоятельного решения
- •7.1. Типовые задачи Запись и оценка точности исходных данных
- •Расчеты, связанные с растворимостью осадков
- •Расчеты, связанные с процессом протолиза
- •Расчеты, связанные с равновесием комплексообразования
- •Расчет результатов в титриметрическом анализе
- •Статистическая обработка результатов
- •7.2. Нетрадиционные задачи
- •8. Методические указания для самостоятельной работы на пэвм с применением расчетных программ
- •Справочные материалы (приложения)
- •Коэффициенты активности ионов [8]
- •Свойства некоторых протолитических растворителей
- •Константы кислотности некоторых кислотно-основных пар (кислотные константы)
- •Мольная доля наиболее депротонированных форм вещества HnR (например, анионов Rn-)
- •Закомплексованность металлов с некоторыми маскирующими реагентами-лигандами при разной концентрации l (без учета рН)
- •Критерии отбраковки грубых промахов а) значения q-теста для разных уровней значимости
- •Б) критические значения максимального относительного отклонения [16]
- •Коэффициенты Стьюдента для некоторых уровней значимости
- •Значения критерия Фишера а) для уровня значимости 0,05:
- •Литература
- •Содержание
- •Часть 1
- •В.И. Вершинин, т.В. Антонова, с.В. Усова
- •По аналитической химии
- •Часть 1
Контрольные вопросы
1. Что такое эквивалент и как рассчитывается его величина в разных случаях?
2. Что такое нормальная концентрация? В каких единицах она выражается? Почему один и тот же раствор может иметь несколько разных нормальных концентраций?
3. Раствор некоторого вещества приготовили в мерной колбе по точной навеске. Как рассчитать его молярную и нормальную концентрацию?
4. Нормальная концентрация раствора KMnO4, рассчитаная для редокститрований в кислой среде, равна 0,100. Чему равна концентрация этого раствора, если титрование проводить в нейтральной среде?
5. Как рассчитать концентрацию металла в растворе по объему комплексона III, затраченному на прямое титрование?
6. Как выбрать число значащих цифр, с которым требуется записать результат анализа, полученный путем прямого титрования ?
7. Чем отличаются понятия «титр раствора» и «титр раствора по определяемому веществу»? Как они связаны математически?
8. Как оценить относительную погрешность результата титрования, если концентрация исследуемого раствора рассчитывается по формуле (27) ?
9. Какую относительную погрешность результатов мы обычно получаем при титровании? Почему гравиметрический анализ, как правило, точнее титриметрического?
6.6. Статистическая обработка данных. Вычисление и использование доверительных интервалов Практическое занятие № 6 Теоретические сведения
Предварительная обработка данных. Для того чтобы оценить воспроизводимость анализа и провести статистическую обработку, необходимо прежде всего получить по одной и той же методикеnрезультатов прямых измерений. Ими могут быть объемы титранта для нескольких одинаковых аликвот, значения аналитического сигнала при его повторных измерениях и т.п. Соответствующие величины (варианты выборки) должны относиться к одному и тому же объекту исследования и быть записаны в порядке их получения. В записи каждой варианты последняя значащая цифра должна соответствовать по разряду абсолютной погрешности измерения, в частности цене деления, а все варианты должны быть равноточными.
Статистическую обработку выборки нельзя вести при наличии грубых промахов,поэтому их надо заранее выявить и исключить. Из нескольких методов их выявления рекомендуется пользоваться наиболее простым - проверкой данных с помощью Q-теста (приложение 8). Если переписать варианты в порядке увеличения измеряемой величины (провести ранжирование), то грубыми промахами могут оказаться крайние варианты, т.е. наибольший или наименьший результаты. Для проверки сомнительного X1 (наименьшего результата) рассчитывают Qэксппо формуле:
Qэксп
=![]() , (32)
, (32)
а при проверке сомнительного Xn (наибольшего результата) пользуются формулой:
Qэксп
=![]() , (32а)
, (32а)
где xn и x1 - крайние варианты в ранжированной выборке,а x2и xn-1 - ближайшие к ним.В любом случае величина Qэксп должна быть положительной. Сомнительная варианта (х1или xn) отбрасывается, если значение Qэкспоказывается больше, чем Qтаблдля выбранного уровня значимости и данного числа вариант (см. пример 1), в противном случае считают, что промах не выявлен, и сомнительный результат оставляют. Вместо Q-теста можно использовать более строгие критерии отбраковки грубых промахов. Так, при одновременном присутствии двух сомнительных результатов рекомендуется пользоваться методом максимальных относительных отклонений (пример 2).
Статистическая обработка не проводится и при наличии дрейфа- особого вида систематической погрешности данных, обычно связанной с изменением состава исследуемой пробы или реагентов во времени. Наличие дрейфа можно предположить, если при достаточно большом количестве вариант (не менее пяти) каждая из них последовательно оказывается больше (или меньше) предыдущей. В этом случае после отбраковки грубых промахов следует провести статистическую проверку значимости дрейфа. В выборке выделяют две группы вариант, взяв их в начале и в конце серии измерений. Затем сравнивают средние значения по обеим группам, пользуясь t-критерием (см. пример 7). Величину tтаблвыбирают с учетом числа вариант в каждой из групп и требуемой достоверности выводов. Если tэксп> tтабл, считают дрейф доказанным. Никакая статистическая обработка полученных данных в этом случае не производится, а исследуются и устраняются причины дрейфа
Проверка характера распределения. Наиболее распространенные способы статистической обработки результатов анализа основаны на предположении, что эти результаты подчиняются нормальному распределению, и вероятность получения любого возможного результата в их генеральной совокупности можно рассчитать по формулам Гаусса. Однако это предположение далеко не всегда истинно; для некоторых объектов и некоторых методик анализа результаты могут соответствовать распределению Пуассона или другим известным распределениям, отличающимся от нормального. Поэтому при достаточном объеме экспериментальных данных следует проверить характер их распределения. Для этого существует ряд способов [19-23], из которых наиболее простым является проверка значимости коэффициентов асимметрии и эксцесса (пример 3). Громоздкие расчеты этих коэффициентов удобно вести с применением специальных компьютерных программ. Если эти коэффициенты не превышают некоторых критических (табличных) значений, считают распределение симметричным и не имеющим достоверного эксцесса, что подтверждает предположение о нормальном (гауссовском) распределении результатов анализа. Возможны и более надежные способы (по критерию Пирсона), но они требуют еще большего объема вычислений.
Расчет выборочных параметров и доверительных интервалов. Если в описании используемой методики измерений (паспорте прибора, ГОСТе) не указываются количественные характеристики воспроизводимости - генеральное стандартное отклонениеили заменяющие его величиныr,x сред и др., то доверительный интервал, в который с заданной надежностью попадает истинное значение измеряемой величины, находят по экспериментальным данным. Для этого после отбраковки грубых промахов рассчитывают следующие параметры:
![]() -
среднее арифметическое из всех n вариант,
-
среднее арифметическое из всех n вариант,
S2- выборочную дисперсию;
S - выборочное стандартное отклонение
S
2 =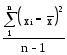 ; S =
; S =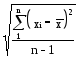 . (33)
. (33)
По выборочным параметрам можно с заданной надежностью оценить - истинное значение измеряемой величины. Однако статистическая обработка не позволяет найти, как и другие параметры генеральной совокупности, абсолютно точно. Мы находим лишь интервал значений, в котором с заданной вероятностью (надежностью) находится. Ширина интервала при прочих равных условиях тем больше, чем больше эта вероятность, которая обозначается символом P. При расчете доверительных интервалов обычно используются значения P = 0,90; 0,95; 0,99.
Способ расчета доверительного интервала зависит от того, какому распределению случайных величин соответствуют полученные нами данные. В случае нормального распределения данных границы доверительного интервала Xminи Xmaxрассчитывают по формулам Стьюдента:
![]()
![]() (34)
(34)
Расчеты по этой формуле дают правильные результаты только в том случае, когда исходные данные (результаты измерений) не содержат значимой систематической погрешности(примеры 4-5). Значения коэффициента Стьюдента (t) приведены в приложении 8. Вероятность того, что в отсутствие дрейфа, грубых промахов, систематических погрешностей и при нормальном распределении данных значениеслучайно окажется вне границ доверительного интервала, равна 1 - P. Эту вероятность обозначают обычно буквойи называют уровнем значимости. В справочниках значения коэффициента Стьюдента обычно приводятся для= 0,10; 0,05 и 0,01.
Величина t зависит и от n (числа параллельно полученных результатов, используемых при расчете интервала). Однако в справочниках значения t приводятся как функция от числа степеней cвободы (df). При расчете доверительных интервалов df = n-1, в других случаях зависимость между n и df может быть иной8.
Формулу (34) можно использовать не только для обработки прямых измерений, но и для обработки результатов анализа, вычисленныхпо прямым измерениям. Так, например, при титровании по методу отдельных навесок прямыми измерениями в каждом опыте являются значения массы и объема титранта, по ним вычисляют содержание компонента, но статистически обрабатывать ни эти объемы, ни массы нельзя. Доверительные интервалы рассчитывают длясодержаний (массовых долей), вычисленных по результатам прямых измерений в параллельных опытах.
Выявление систематических ошибок.Несовпадение среднего результата анализа и истинного содержания компонента в исследуемом материале может быть случайностью, а может быть и следствием систематической погрешности анализа. Для проверки результаты многократного анализа образца с известным содержанием данного компонента выражают в виде доверительного интервала. Если истинное значениев вычисленные границы интервала не попадает, с надёжностью P можно утверждать, что использованный метод анализа имеет значимую систематическую погрешность, т.е. дает неправильные результаты (пример 5).
Сравнение экспериментальных данных по воспроизводимости. При сопоставлении двух методик анализа (двух приборов, двух лаборантов и т.п.) по воспроизводимости полученных данных используют статистический критерий Фишера (пример 6): экспериментальное значение F = S12 / S22сопоставляется с табличным значениями Fтабл. Следует обратить внимание, что первой дисперсией считают ту, которая больше по абсолютной величине, независимо от того, сколько в каждой выборке вариант и какая серия измерений проводилась раньше. Поэтому Fэксп всегда больше 1. Критические значения Fтаблотыскивают в таблицах для подходящих значений n1 и n2 (df1 и df2) и выбранного уровня значимости (см. приложение 10). Дисперсии считают неоднородными, а серии измерений - достоверно отличающимися по воспроизводимости, если Fэксп >Fтабл. В противном случае различие в воспроизводимости методик считают недоказанным.
Сравнение результатов анализа.Различие между средними арифметическими в двух сериях измерений (анализов) может быть статистически достоверным (в этом случае такое различие будет воспроизводиться при повторении измерений) или случайным. Статистическое сравнение средних значений двух выборок позволяет делать обоснованные выводы из проведенных исследований и поэтому особенно важно для специалиста, независимо от того, в какой именно области науки или техники он работает. Обычно сравнение средних проводится по критерию Стьюдента (пример 7). Сопоставление средних значений по Стьюдентув о з м о ж н о, если: а) в обеих выборках отсутствуют грубые промахи; б) измеряемая величина имеет нормальное распределение; в) дисперсии обеих выборок однородны. Поэтому сравнению средних значений должна предшествовать проверка по критерию Фишера. Экспериментальное значение t- критерия находят по формуле:
![]() , (35)
, (35)
где в числителе стоят средние арифметические первой и второй выборок, а в знаменателе - обобщенное стандартное отклонение. Последнюю величину считают по-разному:
Sd
=
![]() при n1=n2=n. (35а)
при n1=n2=n. (35а)
Sd
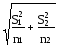 при n1 n2.
(35б)
при n1 n2.
(35б)
При существенном отличии в объеме выборок можно применять и более точные формулы. Величину tэкспсравнивают с табличными значениями для выбранного уровня значимости (см. пример 7), при этом число степеней свободы df = n1+ n2 - 2. Различие средних достоверно, если найденное значение t больше, чем t0,01. Если t меньше, чем t0,05,торазличие средних считается статистически недоказанным, однако и в этом случае не следует утверждать, что результаты анализа, представленные данными двух выборок, достоверно совпадают.
