
- •В.И. Вершинин, т.В. Антонова, с.В. Усова
- •По аналитической химии
- •Часть 1
- •Издание ОмГу Омск 1998
- •1. Введение для преподавателей
- •2. Правила безопасной работы в лаборатории аналитической химии
- •3. Правила взвешивания на двухчашечных демпферных аналитических весах 2
- •4. Оформление отчетов по лабораторным работам
- •5. Лабораторные работы по химическим методам анализа
- •5.1. Гравиметрическое определение железа Методические указания к лабораторной работе № 1
- •5.2. Аргентометрическое определение галогенидов Методические указания к лабораторной работе № 2
- •А. Стандартизация раствора AgNOз
- •Б. Титрование по методу Мора
- •В. Титрование по методу Фаянса
- •Г. Титрование по методу Фольгарда
- •Д. Выполнение контрольной задачи
- •5.3. Кислотно-основное титрование сильных электролитов Методические указания к лабораторной работе № 3
- •А. Приготовление раствора нCl и его стандартизация методом пипетирования
- •Б. Приготовление раствора NаOh, стандартизация его методом отдельных навесок
- •В. Проверка правильности стандартизации растворов нСl и NaOh
- •5.4. Кислотно - основное титрование слабых электролитов Методические указания к лабораторной работе № 4
- •А. Определение концентрации ледяной уксусной кислоты
- •Б. Определение концентрации водного раствора аммиака
- •В. Определение содержаний карбоната и бикарбоната натрия в их смеси
- •Г. Раздельное определение соляной и борной кислот в смеси. Метод замещения
- •Д. Определение содержания аммонийного азота в солях аммония
- •5.5. Кислотно - основное титрование в неводных средах Методические указания к лабораторной работе № 5
- •Краткие теоретические сведения
- •А. Стандартизация раствора нСlO4в сн3соон
- •Б. Определение концентрации анилина
- •В. Определение состава смеси ацетата и хлорида натрия
- •5.6. Комплексонометрическое титрование Методические указания к лабораторной работе № 6
- •А. Стандартизация рабочего раствора комплексона III по фиксаналу MgSo4
- •Б. Способы установления конечной точки титрования
- •В. Определение общей и кальциевой жесткости воды
- •Г. Способы проведения комплексонометрических титрований
- •Сравнение результатов при титровании разными способами
- •Д. Комплексонометрическое титрование многокомпонентных систем
- •5.7. Перманганатометрическое титрование Методические указания к лабораторной работе № 7
- •А. Стандартизация раствора kMnO4
- •Б. Определение содержания Fe (II) в соли Мора
- •5.8. Хроматометрическое титрование Методические указания к лабораторной работе № 8
- •А. Приготовление рабочего раствора. Прямое титрование восстановителей
- •Б. Определение неустойчивых восстановителей (SnCi2) по методу замещения
- •В. Определение окислителей по методу обратного титрования
- •5.9. Иодометрия Методические указания к лабораторной работе № 9
- •А. Стандартизация рабочего раствора иода
- •Б. Определение концентрации раствора Na2so3методом обратного титрования
- •В. Определение концентрации ионов меди (II) по способу замещения
- •Г. Иодометрическое определение кислот
- •Д. Определение концентрации перекиси водорода по методу замещения
- •6. Материалы для подготовки к практическим занятиям
- •6.1. Правила записи исходных данных и расчет результатов. Использование констант
- •Практическое занятие № 1
- •Оценка погрешности результатов расчета и правила их записи.
- •Примеры решения типовых задач
- •Контрольные вопросы
- •6.2. Расчет гетерогенного равновесия “осадок - раствор” Практическое занятие № 2 Теоретические сведения
- •Расчет возможности осаждения при добавлении реагента-осадителя.
- •Примеры решения типовых задач
- •Контрольные вопросы
- •6.3. Расчеты протолитических равновесий Практическое занятие № 3
- •Теоретические сведения
- •Примеры расчетов
- •Контрольные вопросы
- •6.4. Расчеты равновесий комплексообразования Практическое занятие № 4 Теоретические сведения
- •Расчет концентрации свободных ионов металла в отсутствие избытка лиганда
- •Расчеты закомплексованности и маскирования при введении избытка лиганда
- •Определение степени образования различных комплексов в их смеси
- •Примеры решения типовых задач
- •Контрольные вопросы
- •6.5. Расчет результатов титриметрического анализа Практическое занятие № 5 Теоретические сведения
- •Расчет результатов прямого или заместительного титрования
- •Расчет результатов обратного титрования
- •Другие способы расчета
- •Точность результатов титриметрического анализа
- •Примеры решения типовых задач
- •Контрольные вопросы
- •6.6. Статистическая обработка данных. Вычисление и использование доверительных интервалов Практическое занятие № 6 Теоретические сведения
- •Примеры типовых расчетов
- •Контрольные вопросы
- •7. Задачи для самостоятельного решения
- •7.1. Типовые задачи Запись и оценка точности исходных данных
- •Расчеты, связанные с растворимостью осадков
- •Расчеты, связанные с процессом протолиза
- •Расчеты, связанные с равновесием комплексообразования
- •Расчет результатов в титриметрическом анализе
- •Статистическая обработка результатов
- •7.2. Нетрадиционные задачи
- •8. Методические указания для самостоятельной работы на пэвм с применением расчетных программ
- •Справочные материалы (приложения)
- •Коэффициенты активности ионов [8]
- •Свойства некоторых протолитических растворителей
- •Константы кислотности некоторых кислотно-основных пар (кислотные константы)
- •Мольная доля наиболее депротонированных форм вещества HnR (например, анионов Rn-)
- •Закомплексованность металлов с некоторыми маскирующими реагентами-лигандами при разной концентрации l (без учета рН)
- •Критерии отбраковки грубых промахов а) значения q-теста для разных уровней значимости
- •Б) критические значения максимального относительного отклонения [16]
- •Коэффициенты Стьюдента для некоторых уровней значимости
- •Значения критерия Фишера а) для уровня значимости 0,05:
- •Литература
- •Содержание
- •Часть 1
- •В.И. Вершинин, т.В. Антонова, с.В. Усова
- •По аналитической химии
- •Часть 1
Точность результатов титриметрического анализа
Если предположить, что конечная точка прямого титрования идеально совпадает с точкой эквивалентности7, и вычислять массу Х по формуле (26), то относительную погрешность титриметрического анализа следует рассчитывать по формулам сложения случайных погрешностей [ 6, c. 90]:
![]() =
=
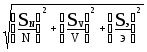 . (31)
. (31)
Погрешности исходных данных (SN, SV, SЭ) следует оценивать с учетом воспроизводимости соответствующих величин, а при отсутствии этой информации в качестве нижнего предела погрешности каждой величины брать единицу последнего разряда (это справедливо только при правильно сделанной записи исходных данных). Например, в качестве Sv можно взять цену деления бюретки, из которой проводилось титрование, хотя правильнее было бы провести несколько параллельных титрований и рассчитать SV, как это принято при статистической обработке данных. Полученная величина, как правило, превышает цену деления бюретки в несколько раз.
При вычислениях по формуле (31) погрешностью в определении молярной массы эквивалента (третьим слагаемым) можно пренебречь (пример 6). Если титруется не вся проба, а аликвота (часть пробы), под корнем в (31) появятся новые слагаемые - относительные погрешности двукратного измерения объемов, и неточность анализа в целом увеличится. Ухудшится точность анализа и в том случае, если проводить анализ по способу обратного титрования, под корнем в этом случае также окажутся дополнительные слагаемые, связанные с погрешностями определения концентрации вспомогательного реагента и измерения его объема.
Примеры решения типовых задач
1.Рассчитать массу карбоната натрия в навеске технической соды, содержащей лишь инертные примеси, если ее титровали фиксанальным 0,1000 н раствором HСl и на титрование затрачено 24,7 мл раствора. В качестве индикатора применяется фенолфталеин.
Решение. Расчет результатов прямого титрования следует вести по формуле (26). Масса Na2CO3(в мг) равна произведению нормальной концентрации титранта, его объема (в мл) и молярной массы одного эквивалента карбоната натрия. Проблема лишь в том, что карбонат натрия может с кислотами реагировать до различных продуктов
Na2CO3 + HCl = NaHCO3 + NaCl
Na2CO3 + 2 HCl = H2CO3 + 2 NaCl
и поэтому величина Эхможет иметь различные значения.
Если карбонат реагирует по первому уравнению, рН раствора гидрокарбоната, присутствующего в точке эквивалентности, практически совпадает с рТ фенолфталеина. Молярная масса эквивалента Na2CO3при его титровании до гидрокарбоната (с фенолфталеином) равна молярной массе этой соли (105,989). При протекании второй реакции, когда на каждую молекулу карбоната натрия расходуется по два протона, молярная масса его эквивалента (далее будем называть ее просто эквивалентом, хотя это не совсем соответствует правилам) равен половине молярной массы (52,9945). Присутствие в точке эквивалентности угольной кислоты фиксируется по окраске соответствующего индикатора, например метилового оранжевого. Таким образом, при титровании карбонатов с разными индикаторами его эквивалент может различаться.
В рассматриваемом примере:
mNa2CO3= 0,1000 · 24,7 · 105,989 = 261,79283262 (мг).
2. Рассчитать массу карбоната натрия в навеске технической соды, содержащей лишь инертные примеси, если ее титровали 0,1000 н. раствором HСl, и на титрование затрачено 49,0 мл раствора. В качестве индикатора применяется метиловый оранжевый.
Решение.Так как переход окраски метилового оранжевого происходит в кислой среде и свидетельствует о переходе карбонатов в угольную кислоту (см. предыдущий пример), эквивалент карбоната натрия в этом титровании равен 52,9945. Масса оттитрованного карбоната натрия равна:
mNa2CO3= 0,1000 · 49,0 · 52,9945 = 259,7260 (мг).
Как и в предыдущем примере ответ округляется до трех значащих цифр, так как с такой точностью измерен объем титранта.
3.Рассчитать процентное содержание СН3СООН в техническом продукте (ледяной уксусной кислоте), если навеску массой 0,1342 г растворили в 10 мл воды и оттитровали 0,0976 н. раствором едкого натра с индикатором фенолфталеином. На титрование затрачено 21,5 мл титранта.
Решение.Прежде всего запишем уравнение реакции:
СН3СООН + NaOH = CH3COONa + H2O.
Поскольку молекула СH3СООH в ходе реакции отдает один протон, ее эквивалент равен молярной массе, т.е. 60,045. Величину молярной массы при расчете эквивалентов либо берут из справочника, либо подсчитывают по формуле через атомные массы, но в любом случае вычислять и записывать эквивалент следует как можно точнее (с 4-5 значащими цифрами).
Проверим, можно ли считать затраченный в ходе титрования объем титранта соответствующим точке эквивалентности, т.е. правильно ли выбран индикатор. В точке эквивалентности рН раствора определяется присутствием продукта (в данном примере - ацетат-ионов). Ацетат-ионы создают слабощелочную среду, и это соответствует рT использованного индикатора (фенолфталеина). Следовательно, индикатор выбран верно и индикаторные ошибки в ходе решения данной задачи учитывать не следует.
Поскольку титрование прямое и рассчитывается процентное содержание компонента, применяем формулу (26а). Массу навески, которая в условии дана в граммах, переводим в миллиграммы.
% CH3COOH = mCH3COOH · 100% / m= NT VT ЭТ · 100% / m=
= 0, 0976 · 21,5 · 60,045 · 100 % / 134,2 = 93,888539 %93,9 %.
Результат округляем до трех значащих цифр, поскольку столько их имеется в наиболее неточном из сомножителей (объеме титранта). Обратите внимание: объем воды, в котором растворили навеску технического продукта перед титрованием, не имеет значения.
4. Для определения содержания серы в нефтепродукте его навеску (0, 8450 г) сожгли в колбе, заполненной кислородом, в присутствии специального катализатора (метод Шенигера), продукты сгорания были поглощены водой. При этом серосодержащие соединения полностью окисляются до серной кислоты. Полученный раствор довели до метки в колбе на 100,0 мл и из него отбирали аликвоты объемом по 10,0 мл. Аликвоты титровали раствором BaCl2 до BaSO4 с помощью микробюретки, точку эквивалентности определяли по изменению электропроводности раствора. На титрование каждой аликвоты было затрачено в среднем 1,47 мл 0,0498 М раствора BaCl2.Рассчитать содержание серы в нефтепродукте.
Решение.Обратите внимание, по условию требуется установить содержание серы, а в реакции титрования участвует серная кислота, анализ идет по методу замещения. Один моль серы дает в результате окисления один моль серной кислоты, на титрование которого расходуется один моль хлорида бария:
H2SO4+ BaCl2= BaSO4+ 2 HСl.
Фактор эквивалентности равен единице, в таких случаях нормальными концентрациями пользоваться нецелесообразно. Для расчета массы серы применяем формулу (25), но, поскольку титровали не всю пробу, а аликвоты, - вводим дополнительно коэффициент аликвирования. При вычислении процентного содержания серы масса навески нефтепродукта предварительно должна быть выражена в тех же единицах, что и масса серы, т.е. в миллиграммах.
mS
= K·CBaCl2 ·VBaCl2·MS
=![]() ·0,0498·1,47·32,066=23,
47423523,5 (мг)
·0,0498·1,47·32,066=23,
47423523,5 (мг)
%S = mS· 100% / m = 23, 5 мг · 100 % / 845,0 мг = 2,78 %.
5.Вычислить, какую процентную концентрацию имеет раствор KBr, если для анализа по методу Фольгарда к 25,0 мл этого раствора добавили 50,0 мл 0,1012 н. раствора AgNO3, а избыток серебра оттитровали 0,1000 н. раствором KSCN, причем на титрование было затрачено 6,2 мл.
Решение.Очевидно, поскольку анализ проводится путем обратного титрования, надо вначале вычислить нормальную (или молярную, в этом случае они равны между собой) концентрацию KBr по формуле (29),
NKBr= (NAg·VAg- NSCN·VSCN) / VKBr = (0,1012·50,0 - 0,1000·6,2) / 25,0 =
= 0,1776 0,178 (моль/л).
Считая, что плотность () раствора KBr равна единице, переводим молярную концентрацию в процентную (см. [8, c.172]):
С% = NKBr· MKBr / 10= 0,178 · 119,002 / 102,12 %.
6.При определении серы по методу Шенигера (см. пример 4) использовали раствор хлорида бария. Чтобы определить его условный титр (титр по сере), взяли навеску (106,4 мг) стандартного дизельного топлива, где содержание серы известно и составляет 1,45%. На титрование продуктов окисления затрачено 12,1 мл титранта. Затем взяли навеску (85,7 мг) другого нефтепродукта - с неизвестным содержанием серы. После окисления его в таких же условиях на титрование полученной серной кислоты пошло 7,6 мл титранта. Рассчитайте процентное содержание серы в исследуемом нефтепродукте.
Решение. Прежде всего рассчитаем титр раствора BaCl2по сере, пользуясь формулой (30). Подставляем в нее данные первого титрования:
T
BaCl2 / S= mS/ VBaCl2 =![]() = 0,128 (мг S на 1 мл титранта).
= 0,128 (мг S на 1 мл титранта).
Теперь по данным второго титрования определим массу серы в навеске исследуемого нефтепродукта и процентное содержание серы в нем.
mS= 0,128 · 7,6 = 0,97 (мг S); %S = 0,97 · 100% / 85,7 = 1,1 %.
7.Рассчитайте относительную случайную погрешность титриметрического определения СH3COOH в техническом продукте. Технические данные возьмите из приведенного выше примера 3.
Решение.Расчет ведут по формуле (31). Для оценки погрешности исходных данных будем считать, что в условии задачи все исходные данные записаны метрологически правильно. Тогда в каждом случае величина абсолютной погрешности будет соответствовать единице последнего разряда в записи соответствующего числа. В частности, будем считать объем титранта (21,5 мл) измеренным с точностью до 0,1 мл и т.п. Тогда относительная погрешность при определении массы СH3COOH равна:
![]() =
=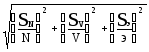 =
=![]() 0,005.
0,005.
Так как взвешивание на аналитических весах - гораздо более точная операция, чем измерение объема, пренебрежем дополнительной погрешностью взвешивания исходной навески и будем считать, что относительная погрешность анализа в целом также будет величиной порядка 0,5%.
