
- •ПРЕДИСЛОВИЕ
- •ЧАСТЬ I. ВАКУУМНАЯ ЭЛЕКТРОНИКА
- •Глава 1. Эмиссионная электроника
- •1.2. Эмиссионная электроника
- •1.2.1. Термоэлектронная эмиссия
- •1.2.2. Термоэлектронная эмиссия с поверхности полупроводников
- •1.2.3. Термокатоды
- •1.2.4. Фотоэлектронная эмиссия
- •1.2.5. Вторичная электронная эмиссия
- •1.2.6. Автоэлектронная эмиссия
- •Контрольные вопросы
- •Глава 2. Движение электронов в вакууме в режиме объемного заряда. Электровакуумные приборы
- •2.1. Диоды
- •2.2. Триоды
- •2.3. Многоэлектродные лампы
- •2.4. Особенности многоэлектродных ламп различного назначения
- •2.5. Генераторные и модуляторные лампы
- •2.6. Электровакуумные приборы диапазона сверхвысоких частот
- •2.6.1. Особенности движения электронов в СВЧ полях
- •2.6.2. Клистроны – приборы с динамическим управлением электронным потоком и резонансными системами
- •2.6.3. Лампы бегущей и обратной волны (ЛБВ и ЛОВ)
- •2.6.4. Лампы со скрещенными полями
- •2.6.5. Усилитель на ЛБВ типа М
- •2.6.6. Генератор на ЛОВ типа М замкнутой конструкции (карсинотрон)
- •2.6.7. Магнетроны
- •2.6.8. Статический режим работы магнетрона
- •2.6.9. Динамический режим работы магнетрона
- •Контрольные вопросы
- •Глава 3. Электронная оптика. Электронно-лучевые приборы
- •3.1. Электронные линзы
- •3.2. Электростатические линзы
- •3.2.1. Диафрагма с круглым отверстием
- •3.2.2. Иммерсионная линза
- •3.2.3. Одиночная линза
- •3.2.4. Иммерсионный объектив
- •3.3. Магнитные линзы
- •3.4. Аберрации электронных линз
- •3.5. Электронно-оптические системы (ЭОС) электронно-лучевых приборов
- •3.6. Отклоняющие системы
- •3.6.1. Электростатическое отклонение электронных пучков
- •3.6.2. Магнитное отклонение электронных пучков
- •3.7. Некоторые особенности электронной оптики интенсивных пучков
- •3.8. Приемные электронно-лучевые трубки
- •3.9. Проекционные ЭЛТ и системы
- •3.10. Запоминающие электронно-лучевые трубки
- •3.11. Передающие электронно-лучевые трубки
- •Контрольные вопросы
- •ЧАСТЬ II. ГАЗОРАЗРЯДНАЯ ЭЛЕКТРОНИКА
- •Глава 4. Элементарные процессы в плазме
- •4.1. Введение
- •4.2. Упругие соударения электронов с атомами и молекулами газа
- •4.3. Неупругие соударения электронов с атомами и молекулами
- •4.3.1. Возбуждение
- •4.3.2. Ионизация
- •4.3.3. Ступенчатые процессы при возбуждении и ионизации молекул электронным ударом
- •4.3.4. Образование и разрушение отрицательных ионов
- •4.3.5. Диссоциация молекул
- •4.3.6. Рекомбинация
- •4.4. Движение электронов и ионов в газе
- •4.4.1. Дрейфовое движение электронов и ионов
- •4.4.2. Диффузия заряженных частиц в условиях разряда
- •Контрольные вопросы
- •Глава 5. Основные виды электрического разряда в газе
- •5.1. Классификация разрядов
- •5.2. Несамостоятельный газовый разряд
- •5.3. Условие развития самостоятельного разряда. Пробой разрядного промежутка
- •5.3.1. Тлеющий разряд
- •5.3.2. Количественная теория катодной области тлеющего разряда
- •5.3.3. Дуговой разряд
- •5.3.4. Искровой разряд
- •5.3.5. Коронный разряд
- •5.3.6. Высокочастотные разряды
- •5.3.7. Разряды на сверхвысоких частотах
- •Контрольные вопросы
- •Глава 6. Газоразрядная плазма
- •6.1. Основные понятия
- •6.2. Диагностика плазмы
- •6.2.1. Метод зондов Лангмюра
- •6.2.2. Оптические методы исследования плазмы
- •6.2.3. Сверхвысокочастотные методы диагностики плазмы
- •6.3. Теории газоразрядной плазмы
- •Контрольные вопросы
- •Глава 7. Газоразрядные приборы
- •7.1. Приборы тлеющего разряда
- •7.1.1. Световые индикаторы
- •7.1.2. Стабилитроны тлеющего разряда
- •7.1.3. Вентили (газотроны) тлеющего разряда
- •7.1.4. Тиратроны тлеющего разряда
- •7.1.5. Переключаемые световые индикаторы
- •7.2.1. Газоразрядные источники света
- •7.3. Ионизационные камеры и счетчики излучений
- •7.3.1. Ионизационные камеры
- •7.3.2. Пропорциональные счетчики
- •7.3.3. Счетчики Гейгера
- •7.4. Разрядники антенных переключателей
- •7.5. Газоразрядные индикаторные панели
- •7.6. Газоразрядные знаковые индикаторы (монодисплеи)
- •7.6.1. ГИП постоянного тока
- •7.6.2. ГИП переменного тока
- •7.6.3. Получение полутоновых изображений на ГИП
- •Контрольные вопросы
- •ЧАСТЬ III. ТВЕРДОТЕЛЬНАЯ ЭЛЕКТРОНИКА
- •8.1. Концентрация носителей заряда в полупроводниках
- •8.2. Электропроводность полупроводников
- •8.3. Диффузионное движение носителей заряда в полупроводниках
- •8.4. Неравновесные носители заряда в полупроводниках
- •8.5. Поверхностные явления в полупроводниках
- •Контрольные вопросы
- •Глава 9. Электрические переходы
- •9.1. Структура и основные параметры n-p перехода
- •9.2. Равновесное состояние n-p перехода
- •9.3. Неравновесное состояние n-p перехода. Явления инжекции и экстракции носителей заряда
- •9.4. ВАХ идеализированного перехода
- •9.5. ВАХ реального n-p перехода
- •9.7. Емкостные свойства n-p перехода
- •9.8. Контакт металл-полупроводник
- •9.9. Гетеропереходы
- •Контрольные вопросы
- •Глава 10. Полупроводниковые диоды
- •10.1. Выпрямительные диоды
- •10.2. Высокочастотные и сверхвысокочастотные диоды
- •10.3. Импульсные диоды
- •10.4. Стабилитроны
- •10.5. Полупроводниковые управляемые емкости (варикапы)
- •10.6. Туннельные и обращенные диоды
- •10.7. Диоды Шотки
- •10.8. Диоды Ганна
- •10.9. Лавинно-пролетные диоды
- •Контрольные вопросы
- •Глава 11. Биполярные транзисторы
- •11.1. Классификация биполярных транзисторов
- •11.2. Физические процессы в транзисторе
- •11.3. Распределение токов в транзисторе
- •11.4. Эффект модуляции ширины базы
- •11.5. Статические вольтамперные характеристики биполярного транзистора
- •11.6. Частотные характеристики биполярного транзистора
- •Контрольные вопросы
- •Глава 12. Тиристоры
- •12.1. Классификация тиристоров
- •12.2. Распределение токов в тиристоре
- •12.3. Особенности работы управляемых тиристоров
- •12.4. Тиристор с симметричной ВАХ
- •Контрольные вопросы
- •Глава 13. Униполярные полупроводниковые приборы
- •13.1. Классификация и основные особенности
- •13.2. Полевые транзисторы с изолированным затвором (МДП-транзисторы)
- •13.4. Дифференциальные параметры МДП-транзистора
- •13.5. Принцип работы полевого транзистора с управляющим n-p переходом
- •13.6. Частотные характеристики МДП-танзисторов
- •13.7. Сравнительная характеристика МДП и биполярного транзистора
- •13.8. Биполярный транзистор с изолированным затвором (IGBT)
- •Контрольные вопросы
- •Глава 14. Светоизлучающие и фотоэлектронные полупроводниковые приборы
- •14.1. Светоизлучающие полупроводниковые приборы
- •14.1.1. Светодиоды
- •14.2. Фотоэлектронные полупроводниковые приборы
- •14.2.1. Поглощение оптического излучения полупроводниками
- •14.2.2. Фоторезистивный эффект и приборы на его основе
- •14.2.3. Фотоэлектрический эффект в n-р переходе
- •14.2.4. Фототранзисторы и фототиристоры
- •14.2.5. Оптоэлектронные пары
- •Контрольные вопросы
- •Глава 15. Полупроводниковые датчики
- •15.1. Датчики температуры
- •15.2. Датчики деформации
- •15.3. Датчики магнитного поля
- •Контрольные вопросы
- •Глава 16. Основы квантовой электроники
- •16.2. Физические основы взаимодействия излучения с веществом
- •16.2.1. Форма и ширина спектральной линии
- •16.3. Устройство и принципы работы лазеров
- •16.3.1. Рабочее вещество
- •16.3.2. Создание инверсии
- •16.3.3. Условия создания инверсной населенности
- •16.3.4. Двухуровневая система
- •16.3.5. Трехуровневые системы
- •16.3.6. Четырехуровневая система
- •16.3.7. Оптические резонаторы
- •16.3.8. Условия самовозбуждения и насыщения усиления
- •16.4. Свойства лазерного излучения
- •16.4.1. Монохроматичность
- •16.4.2. Когерентность
- •16.4.3. Поляризация излучения
- •16.4.4. Направленность и возможность фокусирования излучения
- •16.4.5. Яркость и мощность излучения
- •16.5. Типы лазеров
- •16.5.1. Твердотельные лазеры
- •16.5.2. Рубиновый лазер
- •16.5.3. Неодимовый стеклянный лазер
- •16.5.4. Nd – ИАГ – лазеры
- •16.5.5. Газовые лазеры
- •16.5.6. Атомные лазеры
- •16.5.7. Лазеры на парах металлов
- •16.5.8. Ионные лазеры
- •16.5.9. Молекулярные лазеры
- •16.5.10. Эксимерные лазеры
- •16.5.11. Газовые лазеры в инфракрасной области спектра
- •16.5.12. Химические лазеры
- •16.5.13. Газодинамические лазеры
- •16.5.14. Электроионизационные лазеры
- •16.5.15. Полупроводниковые лазеры
- •16.5.16. Жидкостные лазеры
- •Контрольные вопросы
- •Глава 17. Основы оптоэлектроники
- •17.1. Этапы и перспективы развития оптической электроники
- •17.2. Источники излучения для оптоэлектроники
- •17.3. Фотоэлектронные приемники излучения
- •17.4. Модуляция лазерного излучения
- •17.4.1. Физические основы модуляции лазерного излучения
- •17.4.2. Оптические модуляторы
- •17.4.3. Дефлекторы
- •17.5.1. Элементная база ВОЛС
- •17.5.2. Классификация ВОЛС
- •17.6. Оптические методы запоминания и хранения информации. Оптические (лазерные) диски
- •17.7. Голографические системы хранения и обработки информации
- •17.7.1. Принцип голографии
- •17.7.2. Голографическое запоминающее устройство
- •17.7.3. Голографические схемы записи и считывания информации
- •17.8. Системы отображения информации
- •17.8.1. Особенности зрительного восприятия информации
- •17.8.2. Физические эффекты, используемые для отображения информации
- •17.8.3. Жидкокристаллические индикаторы
- •17.8.4. Жидкокристаллические индикаторные панели
- •17.9. Электролюминесцентные индикаторы
- •17.10. Дисплеи с полевой (автоэлектронной) эмиссией
- •17.11. Отражающие дисплеи (электронная бумага)
- •17.12. Системы отображения информации на основе полупроводниковых светодиодов
- •Контрольные вопросы
- •ЧАСТЬ V. ФУНКЦИОНАЛЬНАЯ, МИКРО И НАНОЭЛЕКТРОНИКА
- •Глава 18. Предмет микроэлектроники
- •18.1. Основные термины и определения
- •18.2. Классификация ИМС
- •18.2.1. Плёночные ИМС
- •18.2.2. Гибридные ИС
- •18.2.3. Полупроводниковые ИМС
- •18.2.4. Совмещенные ИМС
- •18.3. Система обозначений ИМС
- •Контрольные вопросы
- •Глава 19. Биполярные структуры в микроэлектронике
- •19.1. Транзисторы с изоляцией на основе n-p перехода
- •19.2. Транзисторы с диэлектрической изоляцией
- •19.3. Транзисторы с комбинированной изоляцией
- •19.4. Транзисторы типа p–n–p
- •19.5. Многоэмиттерные транзисторы
- •19.6. Многоколлекторные транзисторы
- •19.7. Транзисторы с диодом Шотки
- •19.8. Интегральные диоды и стабилитроны
- •Контрольные вопросы
- •Глава 20. Униполярные структуры в микроэлектронике
- •20.1.1. МДП–транзистор с алюминиевым затвором
- •20.1.3. Конструкция Д–МДП–транзисторов
- •20.1.4. Комплементарные микроэлектронные структуры
- •20.2.1. Пороговое напряжение
- •20.2.2. Вольт-амперные характеристики
- •20.4. Принцип действия МЕП-транзистора
- •20.5. Элементы полупроводниковых постоянных запоминающих устройств (ПЗУ)
- •20.5.1. МНОП-транзистор
- •20.5.3. Двухзатворный МДП–транзистор
- •Контрольные вопросы
- •Глава 21. Микроэлектроника субмикронных СБИС
- •21.2. Методы улучшения характеристик субмикронных МДП-транзисторов
- •21.2.1. Ореол
- •21.2.2. Ретроградное распределение
- •21.2.3. Подзатворный диэлектрик
- •21.2.4. Области стока и истока
- •21.2.5. Напряженный кремний
- •21.3. Субмикронные МДП-транзисторы на диэлектрических подложках
- •21.3.1. Структуры «кремний на изоляторе»
- •21.3.2. Cтруктура «кремний ни на чём»
- •21.4.1. Транзисторы с двойным и с окольцовывающим затвором
- •21.4.2. Транзисторы с вертикальным каналом
- •21.5. Особенности субмикронных транзисторов для аналоговых применений
- •Контрольные вопросы
- •Глава 22. Гетероструктуры в микроэлектронике
- •22.1. Основные свойства гетероперехода
- •22.1.1. Сверхинжекция неравновесных носителей заряда в гетеропереходе
- •22.1.2. Понятие о двухмерном электронном газе
- •22.2. Гетероструктурные полевые транзисторы
- •22.2.1. Транзистор с высокой подвижностью электронов (НЕМТ)
- •22.2.2. Псевдоморфные и метаморфные структуры (р-НЕМТ и m-НЕМТ)
- •22.2.3. НЕМТ на подложках из GaN
- •22.3. Гетеропереходные биполярные транзисторы
- •22.4. Интегральные микросхемы на гетеропереходных полевых транзисторах
- •Контрольные вопросы
- •Глава 23. Пассивные элементы ИМС
- •23.1. Полупроводниковые резисторы
- •23.2. Плёночные резисторы
- •23.3. Конденсаторы и индуктивные элементы
- •23.4. Коммутационные соединения
- •23.4.1. Задержка распространения сигнала
- •23.4.2. Электороимграция
- •Контрольные вопросы
- •Глава 24. Функциональная электроника
- •24.1. Пьезоэлектроника
- •24.2. Оптоэлектроника
- •24.3. Акустоэлектроника
- •24.4. Магнитоэлектроника
- •24.5. Криоэлектроника
- •24.6. Хемотроника
- •24.7. Молекулярная и биоэлектроника
- •24.8. Приборы с зарядовой связью
- •24.9. Диэлектрическя электроника
- •24.10. Приборы на основе аморфных материалов
- •Глава 25. ОСНОВЫ НАНОЭЛЕКТРОНИКИ
- •25.1. Квантовые основы наноэлектроники
- •25.1.1. Квантовое ограничение
- •25.1.2. Интерференционные эффекты
- •25.1.3. Туннелирование
- •25.3. Квантовые транзисторы
- •25.4. Нанотрубки в электронике
- •25.5. Графеновые транзисторы (спинтроника)
- •25.6. Молекулярная электроника
- •25.6.1. Квантовые компьютеры
- •25.7. Заключение
- •Список рекомендуемой литературы
- •CПРАВОЧНЫЙ РАЗДЕЛ
- •Содержание
δ = 2 |
me |
, |
(4.10) |
|
|||
|
M |
|
|
где me – масса электрона; М – масса молекулы газа.
4.3. Неупругие соударения электронов с атомами и молекулами
Если при столкновении электронов с атомами или молекулами происходит изменение внутренней энергии последних, то соударение называется неупругим. При неупругих столкновениях доля энергии, передаваемая при соударении, может быть весьма велика. Существует несколько различных видов неупругих соударений: ионизация, возбуждение, диссоциация и т.д.
Рассмотрим эти процессы отдельно.
4.3.1. Возбуждение
Нормальный атом или молекула находится в состоянии с наименьшей возможной энергией. При возбуждении электронным ударом (или другим путём) валентный электрон атома или молекулы переходит на один из более высоких энергетических уровней, оставаясь связанным с ядром.
Большинство возбуждённых состояний являются неустойчивыми и спустя некоторый промежуток времени возбуждённый атом переходит в состояние с меньшей энергией, излучая при этом фотон. Частота излучения определяется выражением:
hν = Е1 – Е2 , |
(4.12) |
где Е1 и Е2 – потенциальная энергия атома до излучения и после излучения. Спектральные линии, излучаемые из самого низкого возбуждённого
состояния в нормальное невозбуждённое, называются резонансными. Средняя продолжительность жизни возбуждённых атомов t является понятием статистическим. В некотором возбуждённом состоянии величина t
обратно пропорциональна вероятностям перехода из этого состояния на всё
более низкие энергетические состояния путём излучения. |
|
||
t = |
1 |
, |
(4.13) |
å Amn |
|||
n
где Аmn – вероятность перехода из энергетического состояния n в более низкое состояние m путём самопроизвольного (спонтанного) излучения.
Средняя продолжительность жизни атомов, для которых возможны переходы с излучением, составляют 10-7 – 10-8 сек. Атомы и молекулы некоторых веществ имеют уровни возбуждения, с которых излучательный
переход в более низкое энергетическое состояние запрещён правилами отбора. Поэтому продолжительность жизни таких состояний весьма велика и достигает по отношению к излучению до 10-3 сек и более. Такие состояния называются метастабильными. Экспериментально было показано, что время
78
жизни резонансных излучательных уровней, оказывается значительно выше, чем 10-7 – 10-8 сек. Для объяснения этого используются представления о диффузии резонансного излучения. Резонансный квант света при своём
движении в газовой среде может многократно поглощаться и вновь испускаться атомами, что соответствует увеличению экспериментально измеряемого времени жизни соответствующих состояний. Вид функции возбуждения при прямом электронном ударе зависит от того, между какими уровнями осуществляется переход. В силу квантово-механического
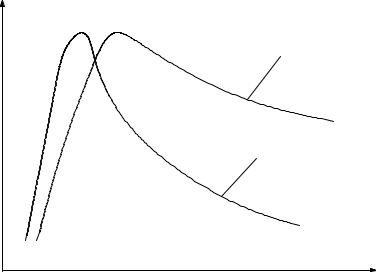
характера неупругого взаимодействия электрона с атомом или молекулой функция возбуждения имеет весьма резкую границу со стороны минимальных значений. Минимальная энергия, необходимая для возбуждения, носит название энергии возбуждения (или потенциала возбуждения). На рис.4.2 приведён схематический вид типичных функций возбуждения атомов электронами.
σ |
в |
2 |
1 |
E |
Рис.4.2. Функции возбуждения при электронном ударе с изменением (1) и без изменения (2) мультиплетности
Функция возбуждения обычно имеет вид кривой с максимумом. Функции возбуждения, связанные с изменением спина электронов при переходе из начального состояния в конечное, имеют более крутой и острый максимум. Если изменения спина не происходит, кривая характеризуется обычно более плавным подъёмом и более медленным спадом. Теоретический расчёт функций возбуждения весьма сложен даже для простых систем, поэтому на практике обычно пользуются экспериментальными данными. Рассмотренные выше вопросы возбуждения применимы как к атомам, так и к молекулам. Необходимо отметить, что при возбуждении электронных состояний молекул при электронном ударе справедлив принцип Франка- Кондона, согласно которому при электронном возбуждении расстояние между ядрами атомов не изменяется. При этом возбуждение может привести
79

к диссоциации молекулы. Подробнее соответствующие эффекты будут рассмотрены ниже.
Кроме возбуждения электронных состояний, в молекулярных газах
электронный удар может приводить к возбуждению колебательных и вращательных состояний молекул. В разрядах наиболее важны колебательно возбуждённые состояния молекул. Возбуждение отдельных колебательных
состояний молекул характеризуются функциями возбуждения резонансного типа с довольно острым максимумом. Наиболее эффективно колебательное
возбуждение |
через |
образование |
промежуточного |
неустойчивого |
отрицательного иона, например: |
|
|
||
|
|
N2 + е → (N2- )* → N2* + e |
(4.14) |
|
4.3.2. Ионизация
Процесс ионизации заключается в отрыве от атома или молекулы одного из валентных электронов. Ионизация в условиях разряда может осуществляться при электронном ударе, термически, под действием квантов излучения и другими способами.
а) Ионизация при электронном ударе
Типичная функция ионизации при электронном ударе возрастает от энергии ионизации до 100 – 150 эВ, а затем медленно спадает (рис 4.3.).
Q, 10–17 см2 |
|
|
|
15 |
|
|
|
10 |
|
|
|
5 |
|
|
|
0 |
50 |
100 |
150 |
|
|||
|
|
|
Е, эВ |
Рис. 4.3. Сечение ионизации молекулы NO |
|||
Спад сечения ионизации при больших энергиях электронов связан с уменьшением времени взаимодействия, в результате чего молекула или атом при столкновении не успевают поляризоваться.
Так же как и в случае возбуждения, на практике обычно используют экспериментальные данные по сечениям ионизации. Поскольку средняя энергия электронов в разрядах невелика (порядка нескольких
80
электроновольт), то в простейшем случае можно применять линейную
аппроксимацию кривой
|
|
s = C (Е – Еi). |
(4.15) |
|
Более широкий интервал энергий охватывает формула, предложенная |
||||
Н.Д. Моргулисом |
|
= C ( E - E )× e-C2 ( E-Ei ) . |
|
|
s |
i |
(4.16) |
||
|
1 |
i |
|
|
Эмпирические постоянные C, C1, C2 зависят от рода газа. Для описания функции ионизации может быть использована и формула Фабриканта.
б) Термическая ионизация
Термическая ионизация заключается в отрыве электрона от атома или молекулы при нагревании газа в условиях термодинамического равновесия.
В качестве количественной характеристики процесса термической ионизации обычно используют степень ионизации a, которая представляет
собой отношение концентрации электронов или ионов к концентрации атомов, включая и ионизованные. При локальном термодинамическом равновесии степень ионизации определяется по формуле Саха:
|
2 |
|
|
|
3 / 2 |
|
eUi |
|
|
a |
|
= |
2gi |
× |
(2pme ) |
× p-1 × kT 5 / 2 × e- |
|
. |
(4.17) |
|
kT |
||||||||
1- a |
|
||||||||
|
g0 |
h3 |
|
|
|
|
|||
В уравнении (4.17) gi и g0 – статистические веса ионов и атомов в нормальном состоянии, eUi- энергия ионизации атома, p – суммарное давление смеси нейтральных и заряженных частиц. Из рассматриваемой формулы следует, что степень ионизации экспоненциально возрастает с ростом температуры и уменьшается с увеличением давления. Для практических расчётов формулу (4.17) можно упростить, пренебрегая a в
знаменателе по сравнению с единицей
|
1/ 2 |
|
|
|
|
|
|
|
|
5800×Ui |
|
|
|
æ |
ö |
|
|
|
|
|
|
|
- |
|
|
|
|
|
-2 |
|
-1/ 2 |
|
5 / 4 |
|
Te |
|
|
||||
ç |
2gi ÷ |
×1,55´10 |
× p |
×T |
× e |
|
|
|
|||||
a = ç |
|
÷ |
|
|
|
|
|
. |
(1.18) |
||||
|
|
|
|
|
|
||||||||
è |
g0 ø |
|
|
|
|
|
|
|
|
|
|
|
|
Термическая ионизация характерна главным образом для дуговых разрядов, а также для магнитогидродинамических генераторов и некоторых других плазменных устройств.
в) Фотоионизация
Фотоионизация заключается в отрыве электрона от атома или молекулы под действием кванта излучения. Основное условие фотоионизации hn®eUi.
Поскольку потенциалы ионизации большинства газов и паров довольно велики, то для фотоионизации необходимы кванты ультрафиолетового или рентгеновского излучения. Функция фотоионизации (зависимость сечения процесса от энергии фотона) обычно представляет собой кривую с острым максимумом. Фотоионизация играет заметную роль в искровых разрядах.
81
