
эээ
.docx
|
1) Технологический процесс получения материалов электронной техники – совокупность способов и процессов переработки сырья в проводники, полупроводники, диэлектрики и магнетики. Способ переработки – это последовательное описание операций, протекающих в соответствующих аппаратах. Такое описание называют технологической схемой. Операция происходит в одном или нескольких аппаратах и представляет собой сочетание различных технологических процессов: тепловых, массообменных, механических и химических. Материалы электронной техники получают в основном с помощью химико-технологических процессов, в которых можно выделить следующие основные стадии: подготовка сырья и подвод реагирующих компонентов в зону реакции.( изменяют только свою внешнюю форму или физические свойства.).химические превращения (реакции) (изменения физических свойств, агрегатного состояния и химического состава вещества). образуются побочные продукты или отходы. отвод из зоны реакции полученных продуктов и выделение целевого продукта. (химических превращений нет). Технологическим режим- совокупность основных факторов, влияющих на скорость процесса, выход и качество продукта. (температура, давление, способ подвода и перемешивание реагентов). Параметры технологического режима определяют принципы конструирования соответствующих реакторов. По характеру протекания во времени технологические процессы подразделяют на периодические, непрерывные и комбинированные. |
2) выделяют отдельные стороны и рассматривают их взаимное влияние. Для количественной характеристики три основных одновременно протекающих стадий: 1) переноса реагирующих веществ к поверхности раздела фаз – зоне реакции; 2) химического взаимодействия в зоне реакции; 3) отвода продуктов реакции из зоны реакции. Характер химико-технологического процесса во многих случаях может значительно усложняться условиями теплопередачи в зоне реакции. так как скорость процесса пропорциональна площади поверхности взаимодействия, то скорость гетерогенного процесса должна зависеть от соотношения между площадями поверхности раздела фаз и объемом. только с учетом всех факторов, влияющих на технологический процесс, можно установить условия, обеспечивающие его высокую скорость, и управлять этим процессом. Общая скорость процесса определяется скоростью самой медленной (лимитирующей) стадии. Если самым медленным звеном процесса является подвод реагирующих веществ к зоне реакции или отвод из нее продуктов реакции, то скорость суммарного процесса будет лимитироваться диффузионным массопереносом (идущие в «диффузионной области»); если химическое взаимодействие, скорость всего процесса определяется скоростью химической реакции (протекает в «кинетической области»). |
3) Активность твердофазных реагентов зависит, от состояния кристаллической решетки, связанного с образованием в ней различных видов дефектов, это обусловлено способом приготовления или обработки реагентов (ионизирующая радиация, лазерное или акустическое излучение, ударные волны и т. д.). Нормальное – это состояние твердых тел, дефектность которых обусловлена собственной разупорядоченностью решетки, являющейся однозначной функцией параметров состояния. Активное – это состояние твердых тел, характеризующееся наличием неравновесных дефектов. Мерой активности твердой фазы является избыток ее свободной энергии по отношению к фазе тождественного состава, находящейся в нормальном состоянии: ΔGизб=Gт*-Gт, где G* и G – свободна энергия фазы в активном и нормальном состоянии. Для каждой группы дефектов природа активности реагента и степень ее проявления в гетерогенных процессах различны. необходимо избегать одновременного введения различных видов дефектов и стремиться, чтобы один вид неравновесных дефектов доминировал над другим. метод активирования реагентов, связанный с термическим и химическим воздействием в процессе их приготовления. Варьирование условиями приготовления реагента позволяет изменять тип его кристаллической структуры . Для активирования твердых фаз используется введение в них микродобавок (легирование). Влияние легирования на активность твердой фазы определяется природой микродобавки, концентрацией и характером ее распределения в матрице. |
|
4) Скорость технологического процесса прямо пропорциональна площади поверхности контакта реагентов и избытку их свободной энергии. Нужно уменьшать размер исходных кусков (позволяет увеличивать реакционную поверхность и избыток свободной энергии твердых реагентов). Процесс уменьшения размеров кусков твердых материалов называется дроблением (измельчением); Процесс измельчения мелких называется размолом. Измельчение бывает сухое и мокрое; Отношение поперечных размеров наиболее крупных кусков до измельчения и после измельчения называется степенью измельчения: n=d1/d2 Степень измельчения за один прием обработки составляет для:- крупных кусков (d1>250 мм) – 2-6;- средних (50-250 мм) – 5-10;- мелких (20-50 мм) – 10-50; - самых мелких (d1<3 мм)- 60 и выше. способы измельчения: раздавливанием , ударом , истиранием и раскалыванием . Способы выбирают с учетом физических свойств измельчаемого материала: твердости, характера излома и др. Материалы с большой твердостью более эффективно измельчать ударом и раздавливанием, вязкие материалы – предпочтительнее истиранием, хрупкие – раскалыванием. Измельчение исходного сырья до необходимого состава осуществляют в машинах грубого, среднего и тонкого измельчения. Для грубого измельчения материала применяют щековые(измельчается периодическим раздавливанием между подвижной и неподвижной массивными щеками) и конусные дробилки (раздавливают в результате непрерывного нажатия внутреннего вертикального усеченного конуса, который вращается в другом, внешнем, конусе). |
5) |
6) Вещество считается достаточно чистым, если содержание примесей в нем меньше того количества, которое мешает использовать это вещество для заданной цели. классификации: «чистый» (марка Ч, содержание примесей от 2·10-5 до 1,0%), «чистый для анализа» (марка ЧДА, содержание примесей от 1·10-5 до 0,4%), «химически чистый» (марка ХЧ, содержание примесей 5·10-6 до 0,5%) и «особо чистый» (марка ОСЧ, содержание примесей не более 0,05%). К высокочистым веществам предлагается относить: 1) неметаллы и химические соединения, если содержание лимитирующих примесей в них не менее чем на порядок ниже по сравнению с соответствующей маркой ХЧ, на два порядка – для марки ЧДА и на три порядка – для марки Ч; 2) металлы и полупроводниковые материалы, если содержание каждой из контролируемых примесей в них не превышает 1·10-4 % (по массе); 3) газы, если содержание каждой из контролируемых примесей в них не превышает 1·10-3 % (объемн.). Высокочистым веществам в зависимости от количества и суммарной концентрации контролируемых примесей присваивают марки ВЭЧ («вещества эталонной чистоты») и ОСЧ («особо чистые вещества»). В ВЭЧ лимитируется общее содержание примесей и содержание некоторых нежелательных примесей. Перед обозначением ВЭЧ пишется число, соответствующее значению общего содержания примесей, а после – два числа через тире: первое показывает количество лимитируемых нежелательных примесей, а второе – отрицательный показатель степени суммы содержания этих примесей.
|
|
7) классификация процессов разделения и очистки, основанная на делении их по физико-химическим свойствам вещества, используемым для разделения компонентов: 1. Процессы, основанные на сорбции. Включают в себя адсорбционные процессы, процессы ионного обмена и хроматографии. 2. Процессы, связанные с экстракцией, в основном жидкостной. 3. Кристаллизационные процессы. 4. Процессы, связанные с перегонкой через газовую фазу. (процессы сублимации, дистилляции, ректификации, а также процессы химического транспорта). 5. Процессы, основанные на электролизе. 6. Процессы, основанные на различии коэффициентов диффузии. 7. Процессы, избирательного осаждения, окисления и восстановления.В общем случае очистку полупроводниковых и диэлектрических материалов и их компонентов обычно ведут в две стадии. На первой стадии компоненты этих материалов переводят в промежуточные химические соединения и производят их очистку, используя практически все процессы, представленные в классификации. На второй стадии производят восстановление компонентов из промежуточных соединений с последующей их очисткой. Применяют способы, основанные на тех же процессах, эффективность которых в отдельных случаях резко возрастает при работе с более чистыми компонентами. Способ выбирается исходя из физико-химических свойств компонента, качества получаемого материала и производительности процесса. |
8) Адсорбция – это поверхностное поглощение. Сорбционные процессы позволяют разделять вещества с очень близкими физико-химическими свойствами. Наибольшее применение в технологии полупроводников и диэлектриков получили процессы разделения и очистки, основанные на поглощении твердыми сорбентами веществ, растворенных в жидких фазах. Это в основном процессы адсорбции, ионного обмена и хроматографии. Адсорбционная система состоит из адсорбента – вещества, на поверхности которого происходит поглощение, и адсорбата – вещества, молекулы которого поглощаются. По природе процессов адсорбцию делят на физическую (молекулы адсорбата не вступают в химическое взаимодействие с адсорбентом. Адсорбция в этом случае обусловлена действием сил Ван-дер-Ваальса) и химическую((хемосорбции) адсорбируемые молекулы вступают в химическую реакцию с адсорбентом с образованием на поверхности химических соединений).Обратный процесс – удаление молекул с поверхности адсорбента – называется десорбцией. Физическая адсорбция в отличие от хемосорбции обратима. Процесс десорбции также может использоваться как метод очистки.Адсорбция является избирательным процессом (на поверхности адсорбента поглощаются только те вещества, которые понижают поверхностное натяжение относительно окружающей среды). |
9) Ионный обмен представляет собой обратимый взаимообмен одноименно заряженных ионов между жидким раствором и твердым нерастворимым веществом, находящимся в контакте с раствором. Твердое вещество, осуществляющее обмен ионов, называют ионитом или ионообменником. Если обмен происходит только положительными ионами (катионами), то ионит называют катионитом, если отрицательными (анионами) – то анионитом. Амфотерные иониты способны одновременно осуществлять катионный и анионный обмен. Ионный обмен представляет собой стехиометрическое замещение: в обмен на каждый эквивалент одного иона, поглощенного из раствора, ионит отдает в раствор один эквивалент другого иона с зарядом того же знака (основное отличие ионного обмена от процесса адсорбции). На практике же ионный обмен всегда сопровождается адсорбцией, а большая часть адсорбентов могут проявлять себя как иониты. Используя иониты, можно осуществлять почти полное извлечение определенного типа ионов из раствора, для этого очищаемый раствор пропускают через ионообменную колонку, заполненную зернами ионита. Рассмотрим схематически строение ионита и механизм ионного обмена. Ионит состоит из каркаса (матрицы), обладающего положительным или отрицательным зарядом (обусловлен расположенными в нем фиксированными ионами). Заряд фиксированных ионов компенсируется зарядом подвижных ионов противоположного знака, расположенных внутри пор каркаса. |
|
1)Выходные параметры конечного продукта Y (характеристики системы, значения которых определяются режимом изучаемого процесса в системе , которая подвергается воздействию входных, управляющих и неконтролируемых факторов).Управляющие параметры Z (параметры процесса, на которые можно оказывать влияние в соответствие с теми или иными требованиями, что позволяет управлять процессом).Неконтролируемые параметры W (Значения их изменяются случайно с течением времени и обычно не могут быть измерены на протяжении процесса). Формализация системы осуществляется с помощью математической модели, выражающей связь между выходными параметрами системы, параметрами состояния и входными управляющими и возмущающими переменными.
|
10)
Графической характеристикой процесса
ионного обмена при постоянной
температуре является линия равновесия
или изотерма ионообмена, которая
выражает зависимость эквивалентной
доли
изотерма
ионообмена показывает, в какой степени
соотношение концентраций конкурирующих
ионов А и В в ионите отклоняется от
этого же соотношения в растворе. Если
рассмотреть ионит не обладающий
никакой избирательностью по отношению
к ионам А сравнительно с ионами В , то
отношение А и В в ионите будет тем же,
что и в растворе. В соответствии с этим
изотерма обмена для такого ионита
будет прямой, расположенной под углом
45º к оси абсцисс.Так как в реальных
системах ионит всегда предпочтительнее
поглощает одни ионы, чем другие, то
селективность ионита по отношению,
например, к иону А будет характеризоваться
кривой с положительной кривизной,
лежащей выше диагонали. Очевидно, что
чем больше кривизна изотермы ионообмена,
тем больше селективность ионита по
отношению к противоионам А.Для оценки
эффективности работы ионита и
характеристики его избирательности
вводят коэффициент
разделения,
который количественно показывает
способность ионита к разделению
противоионов А и В. Коэффициент
разделения
|
10)Поскольку процесс ионного обмена является обратимым, то порцию ионита обычно используют многократно. Как только наступает насыщение ионита ионами В, операцию ионного обмена заканчивают, а ионит регенерируют, промывая его раствором, который удаляет адсорбированные ионы В и обменивает их на ионы А, ранее перешедшие из ионита в очищаемый раствор. Насыщенный ионами А ионит вновь пригоден для использования. При получении чистых полупроводниковых и диэлектрических материалов и их компонентов ионный обмен может быть применен в следующих случаях: для глубокой очистки раствора соли очищаемого элемента от примесей (в этом случае раствор после промывки ионита отбрасывают); для разделения двух элементов, из которых один остается в растворе, а второй адсорбируется ионитом (в этом случае и основной раствор, и раствор после промывки являются ценными); для концентрирования ценного элемента в ионите, извлекаемом из большой массы слабого раствора (в этом случае ценным является раствор после промывки ионита, а исходный раствор отбрасывают); для глубокой очистки воды, широко используемой в технологии полупроводниковых материалов и приборов.
|
|
Если добавка концентрируется на дислокациях и в поверхностном слое, то она изменяет подвижность дислокаций и тем самым влияет на скорость процессов, имеющих дислокационный механизм. легкоплавкие соединения(группа микродобавок), не растворимые в матрице и не образующие с ней химических соединений, но сами заметно растворяющие вещество матрицы. способствуют интенсивной усадке порошкообразных прессовок при нагревании. (увеличивается степень контакта между реагирующими частицами и скорость взаимодействия между ними растет. используются для интенсификации процесса спекания керамики). Механическое воздействие на индивидуальные реагенты и их смеси (для активирования твердых фаз). Механическая энергия, запасенная в твердом теле, подобно теплоте, инициирует многие твердофазные взаимодействия (осуществляют путем измельчения под действием трения и ударов, прессования порошка, действия взрывной волны). Твердые частицы под действием усилий со стороны мелющих тел претерпевают сначала упругую, а затем пластическую деформацию, пока в каком-либо сечении напряжение не превысит предела прочности материала. Затем происходит разделение частиц на более мелкие, которые разлетаются с определенной скоростью. Наибольший вклад в активирование реагентов при их измельчении дают изменения кристаллической структуры и энергетического состояния поверхностных слоев частиц, связанных с накоплением дислокаций, возникновение контактных разностей потенциалов, эмиссия электронов. |
Лимитирующую стадию гетерогенного процесса можно определить опытным путем, изучая влияние различных факторов технологического режима на общую скорость процесса. температурная зависимость скорости диффузии в газах определяется коэффициентом диффузии, зависимость которого от температуры намного меньше аналогичной зависимости константы скорости химической реакции. во многих случаях при повышении температуры гетерогенный процесс может перейти из кинетической области в диффузионную. процессы чаще всего протекают в диффузионной области, однако применение перемешивания потоков и увеличение площади поверхности соприкосновения фаз может привести к переводу процесса из диффузионной области в кинетическую. Это также используется для определения лимитирующей стадии процесса. В общем случае скорость гетерогенного процесса может быть представлена следующим уравнением: u=ksΔF, где k – коэффициент пропорциональности; s – площадь поверхности контакта фаз; ΔF – движущая сила процесса. Это обобщенное кинетическое уравнение для каждого технологического процесса в зависимости от лимитирующей стадии принимает конкретный вид в соответствии с характером движущей силы процесса.
|
Периодический процесс характеризуется единством места протекания отдельных его стадий и неустановившимся состоянием во времени. Непрерывный процесс характеризуется единством времени протекания всех его стадий, установившимся состоянием и непрерывным отбором конечного продукта. Комбинированный процесс представляет собой любой непрерывный процесс, отдельные стадии которого проводятся периодически, либо такой процесс, одна или несколько стадий которого проводятся непрерывно. Непрерывные процессы имеют ряд существенных преимуществ по сравнению с периодическими и комбинированными. «большая технологическая система», включает в себя совокупность происходящих физико-химических и механических процессов, объектов обработки и средств для их реализации. Технологический процесс как большая система схематически представлен на рис X– входы системы или параметры определения исходных продуктов; Y– выходы системы или выходные параметры конечного продукта; Z– контролируемые и управляющие факторы, необходимые для поддержания определенного технологического процесса; W– неконтролируемые факторы, оказывающие случайное возмущающее воздействие на процесс. Входные параметры X (величины, которые могут быть определены экспериментально, но возможность воздействия на них в течение процесса отсутствует. Значения этих параметров не зависят от режима процесса). |
|
В веществах марки ОСЧ на очень низком уровне лимитируется содержание большого числа нежелательных примесей. В обозначении марки после букв ОСЧ приводятся два числа через тире: первое - сколько примесей лимитируется в данном особо чистом веществе, а второе – отрицательный показатель степени суммы содержания этих примесей. В зарубежной литературе принято классифицировать вещества по чистоте числом (n) атомов (молекул) примесей, приходящихся на 1000 атомов (молекул) основного вещества, что обозначается n º/ºº (n promille); на 106 атомов (молекул) основного вещества – n ppm; на 109 атомов (молекул) основного вещества – n ppb. |
|
Для среднего и тонкого измельчения-дробильные валки(с гладкой поверхностью- для измельчения твердых материалов, а зубчатые валки -для дробления пластических материалов), бегуны(состоят из чащи и жерновов, совершающих движение вокруг вертикальной и горизонтальной осей) и ударно-центробежные мельницы. Тонкое измельчение материалов проводят в мельницах, путем истирания материала или одновременного воздействия ударных и истирающих усилий. Бывают шаровые, центробежные и кольцевые мельницы. Для разделения измельченных материалов на фракции с зернами равной величины применяют грохочение(производят при помощи сит или грохотов – аппаратов, главной частью которых являются плоские, цилиндрические или конические сита) или ситовую классификацию. тонкое измельчение объединяют с операцией рассева в схему измельчения, которая осуществляется по открытому или закрытому циклу. Открытый цикл- верхний продукт рассева идет на переработку в шаровую мельницу, откуда все поступает в следующую стадию технологического процесса. закрытый цикл- в дальнейшую стадию переработки поступает материал только заданного гранулометрического состава, все остальное возвращаются в помольный агрегат для дальнейшего измельчения.Для равномерной подачи определенных количеств измельченных материалов в различные технологические реакторы применяют специальные механизмы, называемые питателями или дозаторами (работают по принципу либо весового, либо объемного дозирования). |
|
Эти ионы называются противоионами ( подвижны внутри пор каркаса, они могут быть заменены другими ионами того же знака, поступающими в поры их окружающего ионит раствора). При этом из раствора вместе с противоионами в поры ионита поступают и подвижные ионы того же знака, что и заряд каркаса. Такие ионы называются коионами. В соответствии с этим содержание противоионов в ионите определяется как плотностью заряда каркаса, так и содержанием коионов, согласно условию электронейтральности. Ионный обмен заключается в распределении противоионов между ионитом и раствором. Так как силы электростатического взаимодействия между заряженным каркасом и различными сортами противоионов не одинаковы, и размеры последних могут быть разными, большие противоионы вообще не могут проникать в тонкопористые иониты. Это определяет селективность разных типов ионитов, которая позволяет извлекать из раствора определенные типы ионов, оставляя концентрацию других ионов на неизменном уровне.
|
Используя различную адсорбционную способность веществ, находящихся, например, в растворе, можно осуществить их разделение и очистку, поглотив одно из них адсорбентом и оставив другое в растворе. Количественной характеристикой адсорбционной системы является изотерма адсорбции Второй количественной характеристикой адсорбции, характеризующей температурную зависимость и механизм адсорбционного равновесия, является теплота адсорбции. К наиболее распространенным на практике типам сорбентов можно отнести силикагели, активированные угли, а также различные виды сильно пористых или высокодисперсных алюминосиликатов. Силикагель – гетерополярный сорбент, который хорошо поглощает полярные и значительно менее неполярные вещества и известен прежде всего как эффективный осушитель. Активированные угли имеют кристаллическое строение, у них обнаружена структура графита с характерной слоистой решеткой из шестичленных углеродных колец. Активированные угли состоят из плотных кристаллических агрегатов, формирующих развитую систему пор. Силикагель проявляет высокую адсорбционную активность к веществам различной химической природы, в частности наблюдается эффективная адсорбция полярных примесей из неполярных растворов. Активированные угли, так же как и силикагели, широко применяются на конечной стадии очистки от примесей. |
Часто, особенно при разделении и очистке компонентов с близкими физико-химическими свойствами (например, редкоземельные металлы), использование одного из методов как на первой, так и на второй стадиях оказывается недостаточным и процесс разделения и очистки производят на основе сочетания различных методов. |
|
|
Если
ионит предпочтительнее поглощает
ионы А, то
|
|
|
11) Хроматография - «цветопись». разрешающая способность хроматографического метода разделения сделала возможным появление новой марки чистоты – «хроматографически чистый». Все хроматографические методы основаны на различии в сорбируемости компонентов разделяемой смеси на сорбенте. Это приводит к различной скорости перемещения компонентов разделяемой смеси при движении ее через пористую сорбционную среду.обязательным условием разделения является избирательность и обратимость процесса сорбции компонентов смеси. Скорость передвижения каждого компонента смеси обратно пропорциональна степени сорбции. В результате различной скорости перемещения компонентов смесь делится на ряд полос и зон , образуя хроматогамму. Разделенные компоненты затем механически отделяются друг от друга. При хроматографии разделяемые компоненты распределяются между двумя фазами – неподвижным слоем твердого поглотителя с сильно развитой поверхностью и потоком жидкого раствора или газовой смеси. Виды хроматографического метода(неподвижный слой, подвижный слой): жидкостно- адсорбционная (твердое тело, жидкость), газо- адсорбционная (твердое тело, газовая смесь), жидкостно- распределительная (жидкий поглотитель на твердом носителе, жидкость), газо- жидкостная (жидкий поглотитель на твердом носителе,газовая смесь). Методы разделения смеси, состоящей из двух компонентов А и В, причем вещество В адсорбируется сильнее, чем вещество А: |
12) Сублимация (возгонка) представляет собой процесс непосредственного перехода вещества из твердого состояния в парообразное (возможна для тех веществ, которые будучи нагреты до температуры ниже точки плавления, характеризуются достаточно высокими давлениями паров). При наличии в веществе набора примесей более летучие по сравнению с основным веществом примеси могут быть отогнаны при низкой температуре, а примеси менее летучие – сосредоточены в остатке после возгонки основного компонента.Дистилляция представляет собой процесс разделения жидкого раствора на его составные части, характеризующиеся различием в давлениях паров, путем их испарения и последующей конденсации образовавшихся паров. Эффективность и качество процессов разделения и очистки веществ сублимацией – дистилляцией зависит от целого ряда факторов:1. Примесный состав очищаемого вещества. В зависимости от относительных летучестей основного компонента и примесей примеси более летучие, чем основное вещество, могут быть отогнаны при низкой температуре, а примеси менее летучие – сосредоточены в остатке при отгонке основного компонента при более высоких температурах.2. Величина поверхностей испарения и возгонки.Так как оба процесса происходят с поверхности, то для обеспечения большей скорости необходимо создавать возможно более развитую поверхность у разделяемого вещества. 3. Температура вещества и конденсатора. 4. Давление и состав газов в аппарате для дистилляции или сублимации.
|
13) Представим, что в равновесную систему жидкость А – пар введено некоторое вещество В. При образовании раствора мольная доля растворителя XА становится меньше единицы; равновесие в соответствии с принципом Ле Шателье – Браунасмещается в сторону конденсации вещества А, т.е. в сторону уменьшения давления насыщенного пара РА. Очевидно, что, чем меньше мольная доля компонента А в растворе, тем меньше парциальное давление его насыщенных паров над раствором. Для некоторых растворов выполняется следующая закономерность, называемая первым законом Рауля: Парциальное давление насыщенного пара компонента раствора прямо пропорционально его мольной доле в растворе, причем коэффициент пропорциональности равен давлению насыщенного пара над чистым компонентом. Pi=P0iXi
Поскольку сумма мольных долей всех компонентов раствора равна единице, для бинарного раствора, состоящего из компонентов А и В легко получить следующее соотношение, также являющееся формулировкой первого закона Рауля: (P0A – PA)/P0A=XB Относительное понижение давления пара растворителя над раствором равно мольной доле растворенного вещества и не зависит от природы растворенного вещества. |
|
14) Дистилляция — перегонка, испарение жидкости с последующим охлаждением и конденсацией паров. Простая перегонка — частичное испарение жидкой смеси путём непрерывного отвода и конденсации образовавшихся паров в холодильнике. Полученный конденсат называется дистиллятом, а неиспарившаяся жидкость — кубовым остатком. Фракционная дистилляция (или дробная перегонка) — разделение многокомпонентных жидких смесей на отличающиеся по составу части — фракции путём сбора конденсата частями с различной летучестью, начиная с первой, обогащенной низкокипящим компонентом. Остаток жидкости обогащён высококипящим компонентом. Для улучшения разделения фракций применяют дефлегматор. Ректификация — способ дистилляции, при котором часть жидкого конденсата (флегма) постоянно возвращается в куб, двигаясь навстречу пару в контакте с ним. В результате этого примеси, содержащиеся в паре, частично переходят во флегму и возвращаются в куб, при этом чистота пара (и конденсата) повышается. Действие дистилляции основано на том, что концентрация (С1) некоторого компонента в жидкости отличается от его концентрации (С2) в паре, образующемся из этой жидкости. Отношение С2/С1 является характеристикой процесса и называется коэффициентом разделения (или распределения) при дистилляции. Коэффициент разделения зависит от природы разделяемых компонентов и режима дистилляции. |
|
|
|
|
|
|
|
|
|
|
|
Растворы, для которых выполняется закон Рауля, называют идеальными растворами. Идеальными при любых концентрациях являются растворы, компоненты которых близки по физическим и химическим свойствам (оптические изомеры, гомологи и т.п.) и образование которых не сопровождается объёмными и тепловыми эффектами. В этом случае силы межмолекулярного взаимодействия между однородными и разнородными частицами примерно одинаковы, и образование раствора обусловлено лишь энтропийным фактором. Растворы, компоненты которых существенно различаются по физическим и химическим свойствам, подчиняются закону Рауля лишь в области бесконечно малых концентраций.
|
|
Проявительный - в верхнюю часть колонки с адсорбентом вводят разделяемую смесь А+В, которая тут же адсорбируется. Затем через колонку пропускают жидкость (проявитель Е), адсорбирующуюся слабее обоих компонентов смеси А и В. Проходя через слой, содержащий адсорбированные компоненты, проявитель будет вымывать постепенно из него оба компонента, но преимущественно компонент А, поскольку он адсорбируется слабее. В результате через некоторое время будет наблюдаться разделение компонентов А и В по различным зонам адсорбции. В итоге компоненты А и В выводятся из колонки промывающее жидкостью порциями, разделенными одна от другой чистым проявителем.Вытеснительный- в качестве промывающей применяется жидкость (вытеснитель D), которая адсорбируется сильнее, чем компоненты А и В. Вследствие этого происходит вытеснение жидкостью обоих компонентов, А и В, с адсорбента, причем компонент А вытесняется быстрее. Это приводит к разделению компонентов ,причем наряду с зонами, содержащими А и В в отдельности, будет существовать и промежуточная зона, где они содержатся оба. При дальнейшем проведении процесса вытеснения некоторую часть компонентов на выходе из колонки можно получить в чистом виде, но некоторая часть так и останется в смеси.Фронтальный- заключается в пропускании через колонку только разделяемой смеси. Вследствие меньшей адсорбции компонента А в колонке достигается распределение компонентов. Такой метод дает возможность получить в чистом виде некоторое количество только слабо адсорбируемого компонента А. |
|
|
|
Режимы дистилляции характеризуются температурой испарения и степенью отклонения от фазового равновесия жидкость-пар. С понижением температуры значение коэффициента разделения обычно удаляется от единицы, т. е. эффективность разделения при этом увеличивается. Дистилляция реальных веществ в сильной степени зависит от интенсивности перемешивания жидкости, а также от взаимодействия примесей с основным компонентом и с другими примесными компонентами.Эффективный коэффициент разделения реальной системы основа-примесь может на несколько порядков отличаться от идеального коэффициента разделения - в сторону единицы. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|


 противоиона
А в ионите от его эквивалентной доли
γА
в растворе. Или другими словами для
реакции А+ТВ
+ В+
= В+ТВ
+ А+
противоиона
А в ионите от его эквивалентной доли
γА
в растворе. Или другими словами для
реакции А+ТВ
+ В+
= В+ТВ
+ А+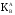 определяется следующим выражением:
определяется следующим выражением: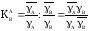
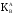 >1,
если же предпочтительнее поглощаются
ионы В, то
>1,
если же предпочтительнее поглощаются
ионы В, то
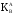 <1.
Чем дальше
<1.
Чем дальше
 отстоит от 1, тем выше селективность.Между
коэффициентом разделения ионита и
изотермой ионообмена существует
простая связь. Согласно выражению для
отстоит от 1, тем выше селективность.Между
коэффициентом разделения ионита и
изотермой ионообмена существует
простая связь. Согласно выражению для
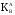 и характеру изотермы, коэффициент
разделения при данном составе раствора
и ионита определяется отношением
площадей двух прямоугольных площадок
,которые сопрягаются с изотермой в
точке N,
отвечающей заданному составу.Важнейшей
физико-химической характеристикой
сорбента является его емкость, под
которой понимают количественную меру
способности сорбента поглощать
извлекаемый компонент из раствора.
От емкости зависит количество сорбента,
необходимого для очистки данного
объема раствора. Емкость сорбентов
часто выражают в миллиэквивалентах
на килограмм сухого сорбента (мэкв/кг)
или в килограммах адсорбированного
вещества на 1 м3
или 1 кг сорбента. Свойства ионитов
обнаруживают многие природные и
синтетические вещества, важнейшие из
которых иониты на основе синтетических
смол и углей, а также некоторые
минеральные иониты (различные
алюмосиликаты, оксиды и др.).
и характеру изотермы, коэффициент
разделения при данном составе раствора
и ионита определяется отношением
площадей двух прямоугольных площадок
,которые сопрягаются с изотермой в
точке N,
отвечающей заданному составу.Важнейшей
физико-химической характеристикой
сорбента является его емкость, под
которой понимают количественную меру
способности сорбента поглощать
извлекаемый компонент из раствора.
От емкости зависит количество сорбента,
необходимого для очистки данного
объема раствора. Емкость сорбентов
часто выражают в миллиэквивалентах
на килограмм сухого сорбента (мэкв/кг)
или в килограммах адсорбированного
вещества на 1 м3
или 1 кг сорбента. Свойства ионитов
обнаруживают многие природные и
синтетические вещества, важнейшие из
которых иониты на основе синтетических
смол и углей, а также некоторые
минеральные иониты (различные
алюмосиликаты, оксиды и др.).