
- •П.А. Киселев, с.Б. Бокуть курс лекций по физической химии
- •Введение
- •Лекция 1. Газовые законы
- •1.1. Температура и нулевой закон термодинамики
- •1.2. Законы поведения идеальных газов: уравнение состояния идеального газа
- •1.3. Кинетическое уравнение газов
- •1.4. Уравнение состояния реальных (неидеальных) газов. Уравнение Ван-дер-Ваальса
- •1.5. Закон парциальных давлений Дальтона
- •Лекция 2. Первое начало термодинамики и термохимия
- •2.1. Вводная часть
- •2.2. Некоторые понятия, используемые в термодинамике
- •2.3. Формулировка первого начала термодинамики
- •2.4. Применение первого начала термодинамики к различным процессам
- •2.5. Теплота химической реакции (общие положения)
- •2.6. Закон Гесса
- •2.7. Следствие из закона Гесса
- •Лекция 3. Второе начало термодинамики и его применение
- •3.1. Основной смысл и значение второго закона термодинамики
- •3.2. Обратимые и необратимые процессы
- •3.3. Формулировка и математическое выражение второго начала термодинамики
- •3.4. Изменение энтропии изолированной системы
- •3.5. Статистическая природа второго начала термодинамики
- •Лекция 4. Третье начало термодинамики. Расчеты изменения энтропии при различных процессах
- •4.1. Формулировка третьего начала термодинамики
- •4.2. Абсолютные и стандартные значения энтропии
- •4.3. Расчеты изменения энтропии в различных процессах
- •1. Расчеты изменения энтропии при изотермических процессах
- •2. Расчет изменения энтропии в неизотермических процессах
- •3. Расчет изменения энтропии сложного процесса
- •4.4. Расчет изменения энтропии при протекании химического процесса
- •4.5. Критерии направления протекания процессов и достижения равновесных состояний в открытых и закрытых системах. Понятие об энергии Гиббса
- •Лекция 5. Химические реакции как открытые в термодинамическом смысле системы. Направление протекания химических реакций. Равновесные химические реакции
- •5.1. Понятие о химическом потенциале
- •5.2. Экзергонические и эндергонические реакции
- •5.3. Взаимосвязь энтальпийного и энтропийного факторов в качестве критерия самопроизвольного протекания химической реакции
- •5.4. Понятие о равновесии химической реакции. Обратимые и необратимые реакции
- •5.5. Уравнение изотермы химической реакции и вывод закона действующих масс
- •5.6. Зависимость константы химического равновесия от температуры
- •Лекция 6. Химическое равновесие в гетерогенных и гомогенных системах
- •6.1. Взаимосвязь химического потенциала с другими термодинамическими функциями
- •6.2. Летучесть
- •6.3. Идеальный раствор
- •6.4. Фазовая диаграмма содержит зоны, линии и тройную точку
- •6.5. Уравнение Клаузиуса-Клапейрона
- •6.6. Коллигативные свойства растворов
- •6.7. Понижение точки замерзания и повышение точки кипения растворов
- •6.8. Осмотическое давление
- •6.9. Растворы электролитов
- •Лекция 7. Растворы электролитов
- •7.1. Общие сведения о теории электролитической диссоциации
- •7.2. Сильные и слабые электролиты
- •7.3. Закон разведения
- •7.4. Сильные электролиты
- •7.5. Ионная сила
- •7.6. Произведение растворимости
- •7.7. Электролитическая диссоциация воды
- •7.8. Концентрация водородных ионов
- •7.9. Буферные растворы
- •7.10. Механизм действия буферных растворов
- •7.11. Буферная емкость
- •Лекция 8. Основные понятия химической кинетики
- •8.1. Химическая реакция
- •8.2. Механизм химической реакции
- •8.3. Исходные, конечные и промежуточные вещества
- •8.4. Глубина превращения реакции
- •8.5. Гомогенные и гетерогенные реакции
- •8.6. Скорость химической реакции
- •8.7. Измерение скорости реакции
- •8.8. Порядок реакции и константа скорости реакции
- •8.9. Молекулярность реакции
- •8.10. Количественные соотношения между скоростью реакции и концентрацией реагента
- •8.11. Реакция второго порядка
- •8.12. Уравнение скорости реакции третьего порядка
- •8.13. Уравнение скорости реакции нулевого порядка
- •8.14. Определение порядка реакции
- •8.15. Теоретические основы химической кинетики
- •8.15.1. Теория активных соударений
- •8.15.2. Теория активированного (переходного) комплекса (переходного состояния)
- •8.15.3. Вывод основного уравнения теории переходного состояния
- •8.15.4. Термодинамическая форма основного уравнения теории переходного состояния
- •8.15.5. Сравнение термодинамической формы основного уравнения теории переходного состояния с уравнением Аррениуса
- •Лекция 9. Основы кинетики и механизма ферментативных реакций. Гомогенный и гетерогенный катализ
- •9.1. Понятие катализа
- •9.2. Основы теории гомогенного катализа
- •9.3. Основы теории гетерогенного катализа
- •9.4. Ферменты как биологические катализаторы
- •9.5. Кинетика реакций, катализируемых ферментами
- •9.6. Физический смысл величин Km и Vmax
- •9.7. Уравнение Михаэлиса-Ментен и ферментативные механизмы
- •9.8. Общее уравнение скорости
- •Лекция 10. Электрохимия
- •10.1. Введение в электрохимию
- •10.2. Термодинамика электрохимических систем
- •10.3. Электродный потенциал
- •10.4. Двойной электрический слой на границе между металлом и раствором электролита
- •10.5. Зависимость плотности заряда от концентрации электролита
- •Лекция 11.Электродные и безэлектродные электрохимические системы
- •11.1. Правила записи эдс и электродных потенциалов электрохимических систем
- •11.2. Типы электродов
- •11.3. Диффузионный и межжидкостный потенциалы
- •На электродах протекают реакции
- •11.5. Концентрационные цепи
- •Лекция 12. Поверхностные явления и адсорбция
- •12.1. Общая характеристика поверхностных явлений
- •12.2. Поверхностные явления в дисперсных системах
- •12.3. Поверхностное натяжение и природа вещества
- •12.4. Термодинамика поверхностных явлений в однокомпонентных системах
- •12.5. Равновесие фаз при искривленной поверхности раздела. Капиллярность
- •12.6. Уравнение Томсона
- •12.7. Капиллярные явления
- •Лекция 13. Адсорбция
- •13.1. Уравнение адсорбции Гиббса
- •13.2. Обзор сорбционных явлений
- •13.3. Природа адсорбционного взаимодействия
- •13.4. Термическое уравнение адсорбции. Изотерма адсорбции
- •13.5. Мономолекулярная адсорбция и изотерма Ленгмюра
- •Литература
- •Содержание
На электродах протекают реакции
Sn2+ + 2e- Sn
Cl2 + 2e- 2Cl- .
Sn2++ 2Cl-Sn+Cl2
Потенциал правого электрода равен
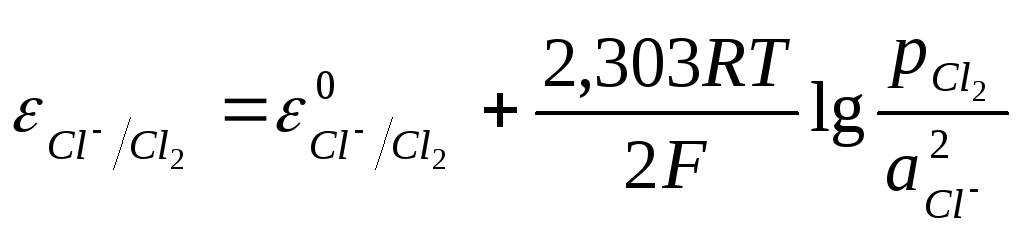 . (11.25)
. (11.25)
Потенциал левого электрода равен
![]() . (11.26)
. (11.26)
ЭДС цепи составляет
 , (11.27)
, (11.27)
Так как
![]() представляет собой среднюю ионную
активность электролита, то
представляет собой среднюю ионную
активность электролита, то
![]() ,
,
т.е. ЭДС простой химической цепи зависит от природы электродов и от средней ионной активности электролита. К сложным электрохимическим системам относятся системы, в которых одинаковые или различные металлические электроды погружены в различные по составу электролиты:
(-) Zn|ZnSO4||CuSO4|Cu(+).
На электродах протекают следующие реакции:
Zn Zn2+ + 2e-;
Cu2+ + 2e- Cu.
Eцепи равна
![]() . (11.28)
. (11.28)
ЭДС сложных химических цепей определяются разностью стандартных потенциалов электродов и активностью потенциал-определяющих ионов (т.е. ионов, обратимых по отношению к электродам).
11.5. Концентрационные цепи
Различают два типа концентрационных элементов – с переносом и без переноса ионов. Концентрационный элемент с переносом ионов состоит из двух одинаковых металлических пластинок, погруженных в раствор с различными концентрациями ионов данного металла. Растворы либо разделены пористой перегородкой, проницаемой для ионов, либо при нахождении в разных сосудах, соединенных электролитическим ключом. Например, левый медный электрод погружен в более концентрированный раствор С1 С2и приобретает более положительный потенциал, чем правый:
CuCu2++ 2e-
Cu2+ + 2e- Cu
Cu+Cu2+Cu2++Cu.
Движущей силой в этом элементе является разность концентраций. При его работе медный электрод растворяется в менее концентрированном растворе, а в более концентрированном ионы меди разряжаются и внедряются в металл. Это приводит к выравниванию концентраций, за счет чего и возникает электрическая энергия. Работа процесса, связанная с выравниванием концентраций, равна
![]() . (11.29)
. (11.29)
Эта работа полностью
превращается в электрическую энергию
![]() .
Отсюда
.
Отсюда
![]() . (11.30)
. (11.30)
Концентрационные элементы без переноса ионов состоят из двух электродов – твердых сплавов или амальгам, отличающихся по содержанию активного вещества. Оба электрода погружены в один и тот же раствор, содержащий ион активного вещества. В этих элементах существует граница между жидкими фазами и нет диффузионного потенциала, искажающего результаты измерения ЭДС.
Примером такого элемента может служить кадмиевый амальгамный элемент.
В этом
случае происходит перенос кадмия от
более концентрированной амальгамы к
менее концентрированной. ЭДС такого
элемента (при
![]() )
равна
)
равна
![]() . (11.31)
. (11.31)
Эта формула справедлива, если металлы, входящие в состав сплава (или амальгамы), не образуют химических соединений.
Лекция 12. Поверхностные явления и адсорбция
12.1. Общая характеристика поверхностных явлений
К поверхностным явлениям относится совокупность явлений, связанных с особенностями свойств пограничных слоев между двумя соприкасающимися фазами, обусловленных наличием избыточной энергии у поверхности раздела. Эти явления могут быть разделены на две основные группы. К первой группе следует отнести явления, связанные с изменением формы поверхностей раздела (капиллярные явления, смачивание, прилипание и др.). Ко второй группе относятся адсорбированные явления, в основе которых лежит изменение состава поверхностного слоя.
Молекулы вещества, расположенного внутри фазы, отличаются по энергетическому состоянию от молекул, находящихся на границе раздела фаз.
Во внутренних слоях фазы силы взаимодействия для каждой молекулы в среднем по времени одинаковы по всем направлениям, полностью скомпенсированы и их равнодействующая равна нулю. Поэтому произвольное перемещение молекулы жидкости или газа внутри фазы в любом направлении не связано с выделением или поглощением энергии. Иначе обстоит дело с молекулами, находящимися на границе раздела фаз. Они испытывают неодинаковое влияние сил межмолекулярного взаимодействия со стороны каждой из соседних фаз, поскольку их физические свойства (плотность, поляризуемость и т.д.) различны.
Поверхностная молекула на границе жидкость/пар испытывает одностороннее притяжение со стороны жидкости, втягивающее ее внутрь жидкости.
В общем случае равнодействующая сил межмолекулярного взаимодействия поверхностных молекул перпендикулярна поверхности раздела и направлена в сторону фазы с более интенсивным межмолекулярным взаимодействием. Эта сила, отнесенная к единице площади поверхности раздела, носит название внутреннего давления. Как правило, внутреннее давление тем больше, чем выше полярность вещества. Втягивая поверхностные молекулы внутрь фазы, внутреннее давление стремится уменьшить поверхность до минимума, возможного в данных условиях.
Увеличение площади поверхности раздела фаз связано с выделением молекул из глубины фазы на поверхность, т.е. с совершением работы против сил внутреннего давления. Эта работа Wв обратимых изотермических условиях пропорциональна площади образующейся новой поверхностиS:
-dW=dS. (12.1)
Максимальная работа W, взятая со знаком минус, в зависимости от условий (р=соnst, илиV=const) равна увеличению энергии Гиббса или энергии Гельмгольца.
Подобным же образом к увеличению поверхностной энергии Гельмгольца приводит и работа разрыва связей при дроблении твердых тел (V=const), сопровождающаяся увеличением площади поверхности раздела фаз.
Коэффициент пропорциональности равен работе увеличения поверхности при постоянных температуре, объеме и составе, отнесенной к единице поверхности. Он численно равен удельной поверхностной энергии Гельмгольца иназывается поверхностным натяжением. В случае двух конденсированных фаз чаще используется понятие «межфазное натяжение». Сложилось так из-за того, что это понятие было введено раньше, чем была развита термодинамика поверхностных явлений. Величинурассматривали как силу, направленную тангенциально к поверхности и стягивающую ее, однако использование такого понятия может привести к неправильному выводу о том, что существует особая, отличная от межмолекулярных сила (поверхностная) и увеличение поверхности есть результат ее растяжения, т.е. увеличения расстояния между молекулами в поверхностном слое. Размерность величины– энергия на единицу поверхности (джоуль на квадратный метр), или, что то же, сила на единицу длины (ньютон на метр).
