
- •2. Значение медицинской генетики для общей патологии человека. Классификация болезней человека (генетические аспекты)
- •3. Феноменология проявления генов. (Принципы клинической генетики).
- •4. Полиморфизм нб
- •5. Гетерогенность нб
- •6. Врожденные ошибки метаболизма. Классификации и общие клинические признаки.
- •7. Лизосомные болезни
- •8. Митохондриальные болезни.
- •9. Механизмы прогрессии опухоли. Онкогены, протоонкогены и гены супрессии опухоли.
- •10. Наследственные формы рака. Феномен потери гетерозиготности.
- •11. Ретинобластома и ген rb1. Синдром Ли-Фраумени и ген tp53.
- •12. Колоректальный рак и гены репарации ошибок спаривания.
- •14. Фенотипическое разложение дисперсии.
- •15. Коэффициент наследуемости
- •18. Генетика количественных признаков как теоретическая основа изучения генетической подверженности в мфз. Понятие генетической предрасположенности.
- •23. Подходы к изучению генетики мфз
- •24 Мультфакториальная модель наследования с пороговым эффектом:
- •25. Модель наследования с эффектами главного гена
- •26. Закон харди-вайнберга
- •28. Мутации и миграции.
- •29. Дрейф генов,
- •30. Естественный отбор(типы) –
- •31. Естественный отбор (компоненты)
- •32. Понятие генетического груза
- •33. Инбридинг
- •34. Современная концепция экогенетики. Основные составляющие экогенетики как науки.
- •35. Экогенетика(факторы окр.Среды)
- •36. Экогенетика(ксенобиотики)
- •37. Фармакогенетика. Генетический контроль метаболизма лекарственных препаратов. Фармакогенетические особенности при наследственных болезнях.
- •40. Картирование и секвенирование.
- •41. Карты генетического сцепления
- •42. Физическое картирование
- •43. Клонирование гена (векторы, космида,плазмида).
- •44. СеквеннрованиеДнк
- •46.Структура гена
- •47. Вариабельность генома человека.
- •48. Транскрипция и трансляция
- •54. Детекция точечных мутаций.
- •55. Методы анализа конформационного полиморфизма одноцеп.Днк и гетеродуплексного анализаэ
- •56. Картирование функц, кандидат, позицион.
- •57. Генетика мфз. Полигены, среда.
- •58.Проблемы генетич.Картирования мфз
- •60.Рутинная и дифференциальная окр. Хромосом.
- •62. Классификация хромосомных болезней
- •64.Хромосомные болезни
- •65. Типы структурных хромосомных мутаций
- •66. Микроделеционные и микродупликационные хзр. Синдромы.
- •67. Метод флюоресцентной гибридизации in situ (fish).
- •69.Нетрадиционное наследование. Мозаицизм, драйв и др.
- •70. Болезни геномного импринтинга, связанные с однородительскими дисомиями
- •71. Экспансия числа тринуклетидных повторов днк.
- •73. Пренатальная диагностика-
- •74. Наслед болезни обмена
- •75. Принципы диагностики нбо
- •77. Селективный скрининг на нбо
- •78. Методы подтверждающей диагностики нбо
- •85. Моногенные болезни. Типы наследования признаков или заболеваний, обусловленных мутацией одного гена.
- •89. Медико-генетическое консультирование.
- •91. Расчет риска при аутос-доминантном типе наследования.
- •96. Понятие о популяционной географии наследственных болезней. Подходы к изучению географии наследственных болезней.
- •99. Методы профилактики наследственных болезней.
23. Подходы к изучению генетики мфз
В основе генетических моделей МФЗ лежат простые закономерности распределения генетических факторов в популяции и в семьях, известных из классической генетики и положенных в основу генетики количественных признаков, являющихся фундаментом генетической эпидемиологии МФЗ.
• Модель мультифакториального наследования с пороговым эффектом (Фолкнер, 1965).
• Модель наследования с эффектами главного гена.
• Модели комплексного сегрегационного анализа (генетическая гетерогенность МФЗ).
• Поиск ассоциаций генетических маркеров с МФЗ.
• Генетическое картирование.
Модель мультифакториального наследования с пороговым эффектом
Фолкнер (1965г.): модель, предназначенную для изучения количественных признаков, можно использовать и в отношении МФЗ, Т.е. когда имеет место качественное проявление - есть или нет заболевание.
Термин «подверженность» (<<предрасположенность», «склонность», «восприимчивость») возник в связи, с попыткой генетического анализа количественных признаков, определяемых множеством генетических и средовых факторов. При этом в отличие от монофакторных признаков, когда всех индивидов можно разделить по фенотипу на два генетических класса («болен»-«здоров»), для признаков, определяемых многими факторами, теоретически может иметь место непрерывный ряд фенотипических классов, объединяющих разные генотипы. При этом всех индивидов можно упорядочить, например, по числу специфических аллелей или по числу средовых эффектов, отрицательно (положительно) влияющих на здоровье. Количественная мера, с помощью которой можно хотя бы теоретически распределить индивидов в непрерывном ряду по их статусу в отношении данного заболевания, и получила название «подверженности».
В пределах этой меры не существует генетических классов «болен» - «здоров». Здесь возможно лишь ввести подразделение по фенотипу, относя всех лиц со значениями подверженности выше некоторого (порогового ) уровня К больным, а лиц, не достигших порога - к здоровым. На практике, однако, поступают наоборот: сначала по клиническим или эпидемиологическим критериям разделяют популяцию на больных и здоровых, а затем определяют пороговые значения подверженности, по которому и была разделена популяция.
Основные положения модели:
Предрасположенность к заболеванию зависит от большого числа генов с аддитивным эффектом и внешнесредовых факторов.
Наиболее часто предрасположенность к заболеванию изучают, анализируя количественные признаки, распределение которых является нормальным. Предполагается, что существует непрерывный ряд значений таких признаков, которые можно измерить у больных и здоровых людей. В этом случае термином «порог» обозначают определенную границу в градуированном континууме подверженности заболеванию, за которой располагаются больные индивиды (рис. 1).
Положение порога определяется частотой заболевания в популяции. Величина порога подверженности к тому или иному заболеванию может быть различна для лиц разного пола, возрасста, национальности и расы. Возрастание восприимчивости к заболеванию, приводящее к превышению этого «порога», возникает в том случае, когда совокупность наследственных и средовых факторов приводит к нарушению гомеостаза и возникновению заболевания.
Кривая распределения у родственников больных также имеет нормальное распределение, но сдвинута вправо по сравнению с распределением в популяции, так как предрасположенность к заболеванию у родственников больного выше, чем в среднем в популяции.
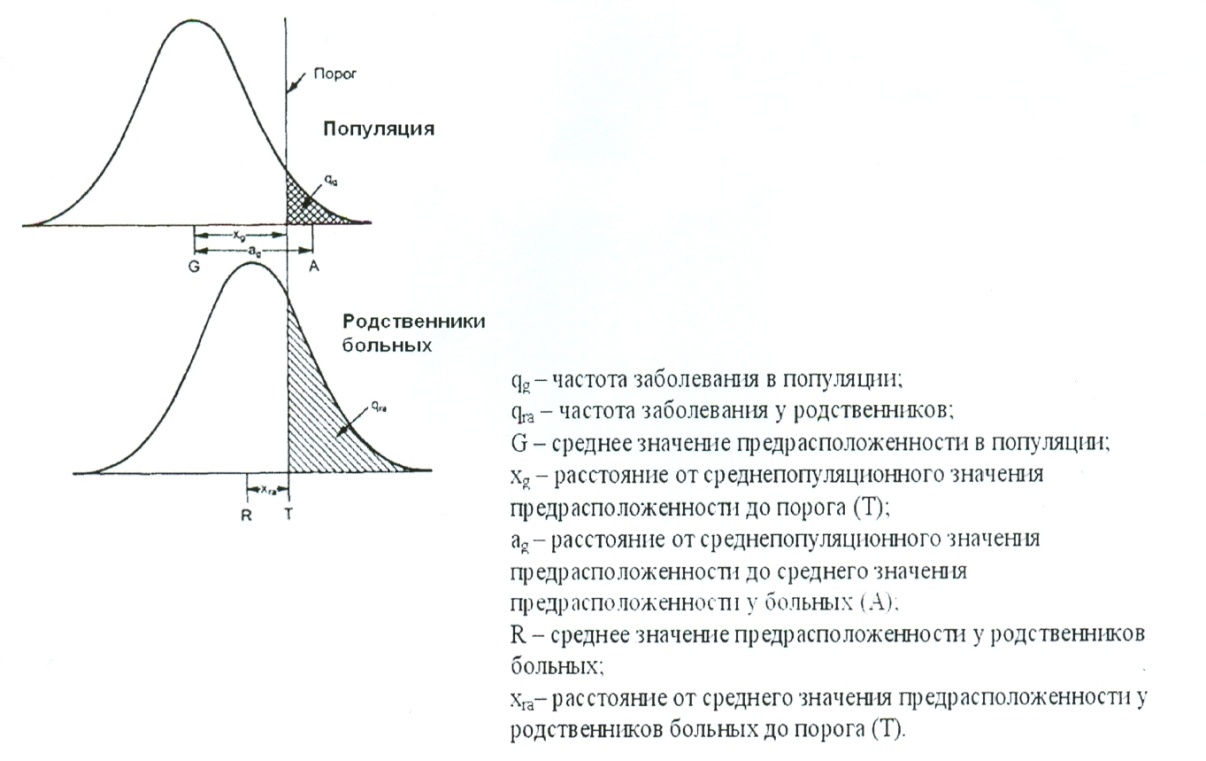
Рис. 1. Гипотетические кривые предрасположенности к МФЗ в популяции и у родственников больных.
Среднюю предрасположенность родственников больного можно определить по частоте заболевания родственников с помощью статистик нормального распределения.
Обычно исследователь располагает:
- данными о частоте заболевания в популяции (g);
- данными о частоте заболевания среди родственников больных (ra).
Эти данные позволяют рассчитать:
- показатели отклонения порога (х) и среднего значения предрасположенности для родственников больного (а) от среднепопуляционного значения предрасположенности.
Из таблиц нормального распределения можно определить:
- показатели отклонения «х» и «а> в единицах стандартного отклонения (xg и ag);
- значение частоты заболевания среди родственников в единицах стандартного отклонения (хга).
Тогда коэффициент корреляции между пробандами и родственниками составит: r=(Xg - xra)/ag
Корреляции нужны для оценки наследуемости соответствующего заболевания.
Для оценки вклада генетических факторов в предрасположенность к МФЗ необходимо использовать коэффициент наследуемости в узком смысле слова (h2).
h2=VА / VР
Однако в большинстве случаев вычисление коэффициента наследуемости осуществляется через коэффициент корреляции (r) между родственниками различной степени родства. Например, h2=2r для родственников первой степени родства и дизиготных близнецов и h2=4r для родственников второй степени родства (дедушки, бабушки; дяди, тети).
Наследуемость - доля предрасположенности к заболеванию, обусловленная действием аддитивных генетических Факторов.
Существуют графы корреляции по предрасположенности между родственниками и пробандами. С их помощью можно определить коэффициента наследуемости для МФЗ.
Коэффициенты наследуемости для МФЗ варьируют в широких пределах:
• инсулинозависимый сахарный диабет - 30%
• биполярные психозы - 90%
• системная красная волчанка - 90%
Если наследуемость приближается к 100%, возможно наличие главного гена.
На основе концепции подверженности с пороговым эффектом можно сформулировать некоторые теоретические закономерности распределения МФЗ в популяции и в семьях, которые отличаются от моногенных (менделирующих) форм.
- Чем реже встречается болезнь в популяции, тем выше риск для родственников больного;
- Частота заболевания среди родственников больного 1 степени родства равна квадратному корню из частоты болезни в популяции;
- Снижение частоты заболевания у родственников больного II степени родства по сравнению с родственниками 1 степени родства, и III степени родства по сравнению с родственниками II степени родства будет более резким, чем при доминантном наследовании с неполной пенетрантностью.
При мультифакториальном наследовании риск развития заболевания зависит от:
• степени родства с больным в родословной. Чем выше степень родства с больным, тем выше риск заболевания для его родственников.
• числа больных родственников. Чем больше в семье больных родственников, тем выше риск заболевания.
• тяжести клинических проявлений. Чем тяжелее протекает заболевание, тем выше риск для родственников больного.
• различий в частоте заболевания у разных полов. Чем чаще заболевание проявляется у одного пола, тем выше риск для родственников больного редко поражаемого пола.
• Чем выше наследуемость заболевания, тем выше его риск.
Таким образом, при МФЗ, в отличие от моногенных болезней, риск не является постоянной величиной.
Для оценки риска развития МФЗ используют значения эмпирического риска. Величины эмпирического риска устанавливают при эпидемиологических обследованиях населения. Результатом таких исследований являются таблицы, которые используют при оценке риска для разных типов семей.
