
- •2.1. Предмет термодинаміки і термодинамічний метод.
- •2.2. Основні поняття та визначення.
- •3.1. Термодинамічна система:
- •3.2. Термодинамічні процеси та стани: рівноважні й нерівноважні.
- •4.1. Зміст термодинамічного процесу: теплота і робота
- •5.1. Теплота процесу: поняття теплоємності тіла.
- •5.2. Масова, об'ємна й мольна теплоємності
- •5.3. Закон збереження і перетворення енергії
- •5.4. Внутрішня енергія
- •5.5. Перше начало термодинаміки
- •5.6. Ентальпія.
- •6.1. Термічне рівняння стану
- •6.2. Фізичний зміст теплоємностей.
- •7.1. Ентропія
- •7.2. Теплові діаграми.
- •8.1. Внутрішня енергія, ентальпія й ентропія ідеального газу.
- •8.3. Основні властивості газових сумішей
- •8.5 Парціальні тиски
- •9.1. Термодинамічний метод дослідження процесів
- •Ізохорний процес
- •9.3. Ізобарний процес
- •9.4. Ізотермічний процес
- •9.5. Адіабатний процес
- •9.6. Політропні процеси
- •9.7. Політропний процес
- •. Другий закон термодинаміки: його значення й сфера застосування
- •10.2. Формулювання другого начала термодинаміки
- •11.1. Умови роботи теплових машин
- •11.2. Кругові термодинамічні процеси, або цикли
- •11.3. Термодинамічний аналіз кругових процесів: баланс теплоти й роботи в теплових машинах
- •11.4. Термічний к. К. Д. І холодильний коефіцієнт циклів
- •12.1. Прямий оборотний цикл Карно та його термічний ккд
- •12.2. Зворотний оборотний цикл Карно та його холодильний коефіцієнт
- •12.3. Перша теорема Карно
- •12.4. Середньоінтегральна температура підведення (відводу) тепла й еквівалентний цикл Карно.
- •12.5. Узагальнений (регенеративний) цикл Карно
- •12.6. Абсолютна термодинамічна температура
- •13.1. Властивості оборотних і необоротних циклів та математичне вираження другого закону термодинаміки
- •13.2. Зміни ентропії в оборотних і необоротних процесах
- •13.3. Принцип зростання ентропії та фізичний зміст другого закону термодинаміки
- •13.4. Ентропія та статистичний характер другого закону термодинаміки
- •13.5. Третій закон термодинаміки (теорема Нернста)
- •14.1. Максимальна робота й функції стану.
- •14.2. Термодинамічні потенціали.
- •Графічне представлення співвідношень характеристичних функцій
- •Канонічі рівняння стану
- •14.4. Рівняння Гіббса-Гельмгольца
- •14.5. Хімічний потенціал і нерівність Гіббса
- •14.6. Загальні умови рівноваги термодинамічної системи
- •15.1. Властивості реальних газів
- •15.2. Рівняння стану Ван-дер-Ваальса
- •15.3. Аналіз рівняння Ван-дер-Ваальса - закон відповідних станів
- •Фазові переходи й фазові діаграми речовин; рівняння Клапейрона - Клаузіуса
- •16.2. Рівняння Клапейрона - Клаузіуса
- •Одержання пари та її характерні стани
- •Основні параметри станів водяної пари.
13.2. Зміни ентропії в оборотних і необоротних процесах
Величина dQ/T під знаком інтеграла в (8-8), як ми знаємо, являє собою повний диференціал ентропії S
dS = dQ/T. ( 8-9)
Проінтегрував рівняння (8-9) по якому-небудь шляху 1-2, одержуємо
 (
8-10)
(
8-10)
При оборотному адіабатному процесі, коли dQ = 0, dS = 0 і S2 = S1 = const,
тобто в адіабатному оборотному процесі ентропія не змінюється.
Розглянемо зміну ентропії при необоротних процесах. Для цього проведемо між станами 1 і 2 оборотний процес 2-4-1 і умовно пунктиром необоротний 1-3-2 (мал. 8-7). Отриманий у результаті цих процесів цикл буде необоротним. Відповідно до рівняння ( 8-7) одержуємо
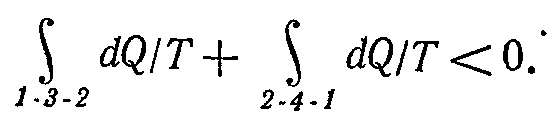
|
|
Рис. 8-7
Оскільки процес 2-4-1 оборотний, то другий інтеграл дорівнює різниці S1 – S 2, тому

або
![]() ( 8-11)
( 8-11)
Знак нерівності в рівнянні ( 8-11) указує на те, що у випадку необоротного процесу інтеграл у правій частині його вже не виражає собою різниці ентропії, а менше її. Поєднуючи рівняння ( 8-10) і ( 8-11), знаходимо
 (
8-12)
(
8-12)
Ентропія є функція стану, тому зміна ентропії як для оборотного, так і необоротного процесів буде такою самою.
Рівняння (8-12)
показує, що для оборотного процесу
![]() дорівнює
зміні ентропії S2
— S1,
а
для необоротного він менше, ніж S2
– S1.
дорівнює
зміні ентропії S2
— S1,
а
для необоротного він менше, ніж S2
– S1.
Оскільки рівняння ( 8-8) виражає собою другий закон термодинаміки, то й рівняння (8-12) виражає той же закон, але для більш загального випадку. Вираження (8-8) застосовне тільки до циклів, тоді як вираження (8-12) застосовне до будь-яких процесів, у яких початковий і кінцевий стани 1 і 2 різняться між собою. Вираження (8-8) виходить із (8-12) як окремий випадок.
Для елементарного необоротного процесу
ds > dQ /T. ( 8-13)
Поєднуючи рівняння ( 8-9) і ( 8-13), можна записати, що для всякого процесу зміна ентропії задовольняє співвідношенню
ds ≥ dQ /T, ( 8-14)
де dQ — кількість теплоти, отримана тілом від джерела теплоти; Т — абсолютна температура джерела теплоти; знак рівності відноситься до оборотних, а знак «більше» — до необоротних процесів.
В оборотних процесах зміна ентропії характеризує напрямок теплообміну. Якщо dq > 0, тобто теплота до робочого тіла підводиться, то його ентропія у відповідності c нерівністю (8-13) зростає (ds > 0). При відводі теплоти (dq < 0) ентропія тіла зменшується (ds < 0). Нерівність (8-14) можна представити у вигляді
Tds ≥ dq ,
або з урахуванням першого закону термодинаміки
![]() (
8-20)
(
8-20)
Ці співвідношення називаються об'єднаними рівняннями першого й другого законів термодинаміки.



