
- •Учебно-методические разработки для самостоятельной работы студентов по курсу «Теоретические основы защиты окружающей среды»
- •Часть II
- •Специальные методы очистки сточных вод и основные методы сепарации твердых отходов
- •Введение
- •Глава 1. Химические методы очистки сточных вод
- •1.1 Нейтрализация
- •1.1.1. Нейтрализация смешиванием
- •1.1.2. Нейтрализация добавлением реагентов
- •1.1.3. Нейтрализация фильтрованием кислых вод через нейтрализующие материалы
- •1.2. Нейтрализация кислыми газами
- •1.2.1. Окисление и восстановление
- •1.2.2. Окисление пероксидом водорода
- •1.2.3. Окисление кислородом воздуха
- •1.2.4. Озонирование
- •Контрольные вопросы
- •Глава 2. Явление осмоса и его использование при очистке сточных вод
- •2.1. Осмотическое давление
- •2.2. Биологическая роль осмотического давления
- •2.3. Законы осмотического давления
- •2.4. Термодинамика осмотического давления
- •Контрольные вопросы
- •Глава 3. Физические основы электродных процессов при очистке сточных вод от примеси
- •3.1. Явления электролиза, поляризации и перенапряжения
- •3.1.1 Электролиз
- •3.1.2. Кривая напряжения
- •3.1.3. Электродвижущие силы разложения
- •3.1.4. Потенциал разложения
- •3.1.5. Концентрационная поляризация
- •3.1.6. Деполяризация
- •3.1.7. Перенапряжение
- •3.2. Электрокапиллярные явления
- •3.2.1. Зависимость поверхностного напряжения от заряда
- •3.2.2. Влияние адсорбции на электрокапиллярную кривую
- •3.2.3. Проблема абсолютных потенциалов
- •3.3. Электрокинетические явления
- •3.3.1. Диффузионный двойной слой и электрокинетический потенциал
- •3.3.2. Емкость двойного слоя
- •3.3.3. Электроосмос
- •3.3.4. Потенциал течения
- •3.3.5. Электрофорез
- •3.3.6. Потенциалы осаждения
- •3.4. Электрохимические методы очистки сточных вод
- •3.4.1. Анодное окисление и катодное восстановление
- •3.4.2. Электрокоагуляция
- •3.4.3. Электрофлотация
- •3.4.4. Электродиализ
- •Контрольные вопросы
- •Глава 4. Физические основы процессов переработки твердых бытовых отходов
- •4.1. Процессы измельчения и дробления
- •4.1.1. Назначение операций дробления и измельчения
- •4.1.2. Степень дробления и измельчения
- •4.1.3. Стадиональность и схемы дробления и измельчения
- •4.1.4. Удельная поверхность диспергированного материала
- •4.1.5. Современные представления о разрушении твердого материала
- •4.1.6. Механические свойства твердых тел при простых видах деформации
- •4.1.7. Законы дробления
- •4.1.8. Способы дробления, классификация машин для дробления и измельчения
- •4.2. Процесс грохочения
- •4.2.1. Основные понятия и назначение грохочения
- •4.2.2. Просеивающая поверхность
- •4.2.3. Способы определения гранулометрического состава
- •4.2.4. Ситовый анализ
- •4.2.5. Характеристики крупности
- •4.2.6. Аналитическое представление характеристик крупности
- •4.2.7. Дифференциальные функции распределения по крупности
- •4.2.8. Вычисление поверхности и числа частиц по уравнениям суммарной характеристики крупности
- •4.2.9. Эффективность процесса грохочения
- •4.2.10. «Легкие», «трудные» и «затрудняющие» частицы
- •4.2.11. Вероятность прохождения частиц через отверстия сита
- •4.2.12. Факторы, влияющие на процесс грохочения
- •4.3. Электромагнитная сепарация. Физические основы процесса
- •4.4. Электростатическая сепарация. Физические основы процесса
- •4.5. Электродинамическая сепарация
- •4.6. Сепарация твердых материалов по коэффициенту трения
- •4.7. Сепарация на основе явления смачиваемости
- •4.8. Аэросепарация
- •4.9. Составление балансной схемы переработанного твердого сырья
- •4.9.1. Баланс материалов при переработке твердых отходов
- •4.9.2. Технологические и технико-экономические показатели переработки твердых отходов
- •Контрольные вопросы
- •Варианты домашнего задания по курсу «Теоретические основы защиты окружающей среды»
- •1. Отстаивание, сгущение, осветление.
- •2. Флотация
- •3. Экстракция
- •4. Дробление и грохочение
- •5. Измельчение и классификация
- •6. Магнитное и электрическое разделение
- •Примеры выполнения домашних заданий
- •Темы заданий для курсовых работ по курсу «Теоретические основы защиты окружающей среды»
- •Пример выполнения курсовой работы
- •Литература
- •Оглавление
- •Глава 1. Химические методы очистки сточных вод 6
- •Глава 2. Явление осмоса и его использование при очистке сточных вод 20
- •Глава 3. Физические основы электродных процессов при очистке сточных вод от примеси 31
- •Глава 4. Физические основы процессов переработки твердых бытовых отходов 73
4.9. Составление балансной схемы переработанного твердого сырья
4.9.1. Баланс материалов при переработке твердых отходов
Организация работы на обогатительных фабриках имеет свои особенности: каждую смену подводятся итоги количественных и качественных показателей. Например, если фабрика выдает один концентрат и за смену переработано Q т руды, то обозначаем по данным анализов средних проб, содержание металла в исходной руде %, в концентрате β %, в отработанной породе υ % и весовой выход полученного концентрата К. Тогда количественно потери составят (Q − K). Баланс металла будет иметь вид:
![]() .
.
Степенью концентрации по весу r называется отношение веса обогащенной руды к весу полученных концентратов:
![]() .
.
Процент извлечения металла представляет отношение количества металла, извлеченного в концентрат, к количеству металла, содержащемуся в исходной руде:
![]() . (4.50)
. (4.50)
Количество выработанных концентратов:
![]() . (4.51)
. (4.51)
Из вышеприведенных формул видим, что для учета качественных и количественных показателей работы фабрики необходимо знать количество переработанной руды за смену по сухому весу Q т, а также α, β и υ - по анализам средних проб.
Аналогично на фабриках, вырабатывающих два концентрата, легко вывести закономерности, если обозначить: Qт - количество переработанной руды, KPb - первого концентрата (например, свинцового) и KZn - цинкового концентрата.
Тогда количество «хвостов» составит:
Q − (KPb + KZn).
Принимая Q за 100% и обозначая через х процент выхода свинцового концентрата, через y - процент выхода цинкового концентрата и через z - процент выхода «хвостов», получим
100 = х + y + z, или z = 100 (x + y).
При установившемся режиме производственного процесса для его надлежащего контроля необходимо за весь период восьмичасовой смены отбирать пробы: 1) исходной руды; 2) свинцовых концентратов; 3) цинковых концентратов; 4) потерь.
Каждая из этих проб подвергается химическому анализу, и в ней определяют процентное содержание свинца βPb и цинка β′Zn, в цинковом концентрате цинка βZn и свинца β′Pb и в «хвостах» свинца υPb и цинка υZn.
При этих обозначениях распределение металлов свинца и цинка по продуктам обогащения может быть определено следующими двумя уравнениями:
100 αPb − x βPb − y β′Pb − [100 − (x+y)] υPb = 0; (4.52)
100 αZn − x βZn − y β′Zn − [100 − (x + y)] υZn = 0. (4.52,a)
Подставляя данные химических анализов, решаем эти два уравнения с двумя неизвестными и находим значение весовых выходов концентратов γPb[%] = х[%] свинцового и γZn[%] = y[%] цинкового, а выход «хвостов» γх z[%] = 100 − (x + y).
Количественные весовые выходы продуктов обогащения в тоннах при обработке Qт руды за смену или за любой другой отрезок времени, в течение которого производится отбор проб, выразятся следующим образом:
![]() и
и
![]() .
.
Тогда баланс металлов и извлечение в процентах по продуктам определяется следующими формулами.
Распределение свинца и цинка по продуктам обогащения:
Свинца в руде
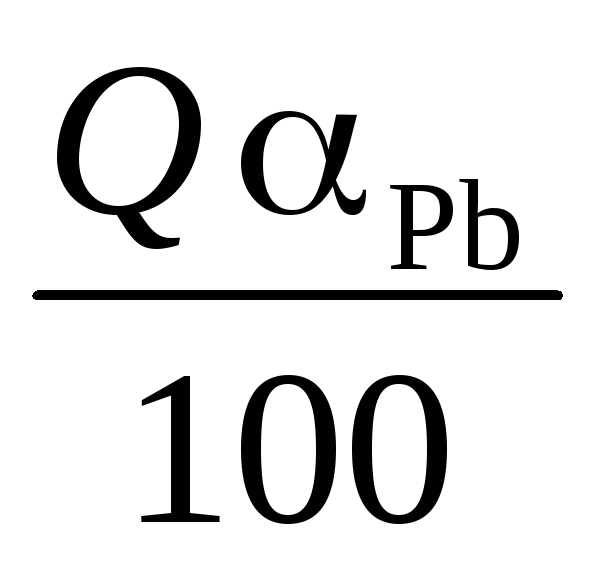 [т], а извлечение свинца равно 100 %.
[т], а извлечение свинца равно 100 %.Свинца в свинцовом концентрате
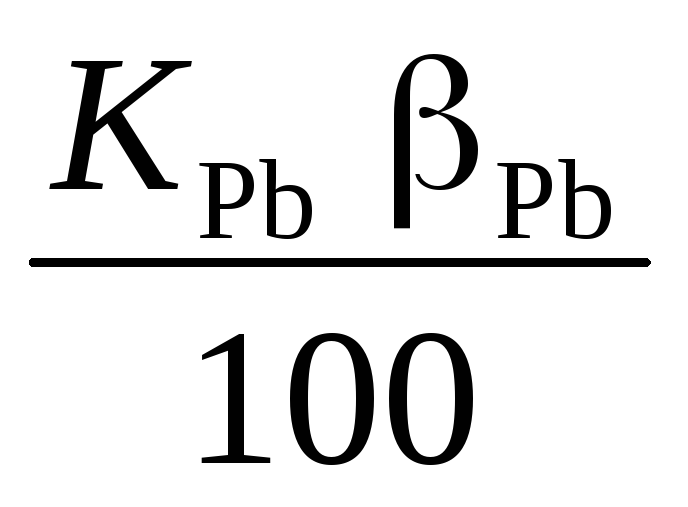 [т], а извлечение свинца в концентрате,
равное:
[т], а извлечение свинца в концентрате,
равное:
![]() .
.
Свинца в цинковом концентрате
 [т], а извлечение свинца в цинковом
концентрате:
[т], а извлечение свинца в цинковом
концентрате:
![]() ;
;
Свинца в хвостах
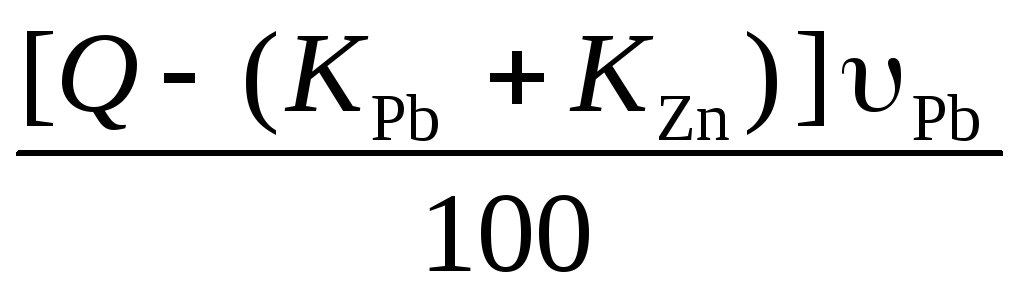 [т], а извлечение, т.е. процент потерь,
равно:
[т], а извлечение, т.е. процент потерь,
равно:
![]() .
.
Цинка в руде
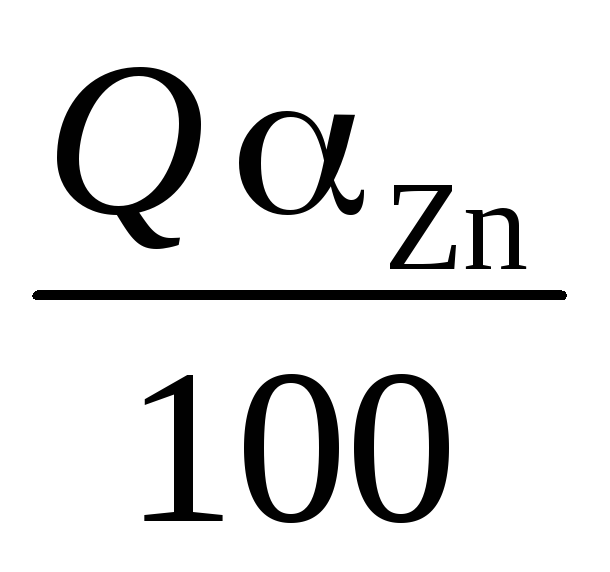 [т], а извлечение цинка равно 100 %.
[т], а извлечение цинка равно 100 %.Цинка в цинковом концентрате
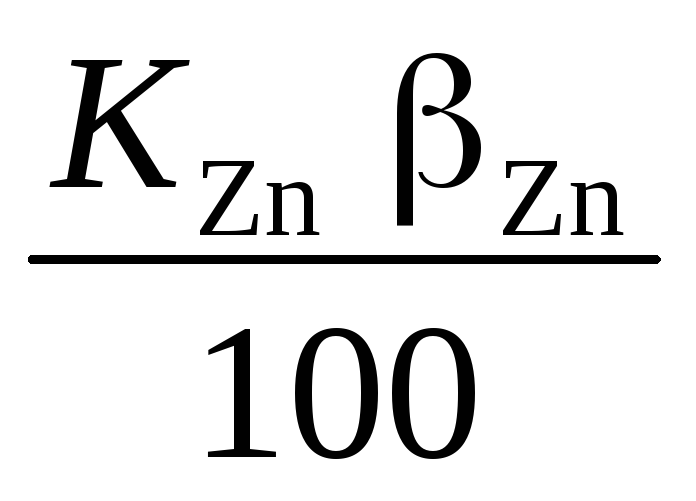 [т], а извлечение цинка в цинковый
концентрат:
[т], а извлечение цинка в цинковый
концентрат:
![]() .
.
Цинка в свинцовом концентрате
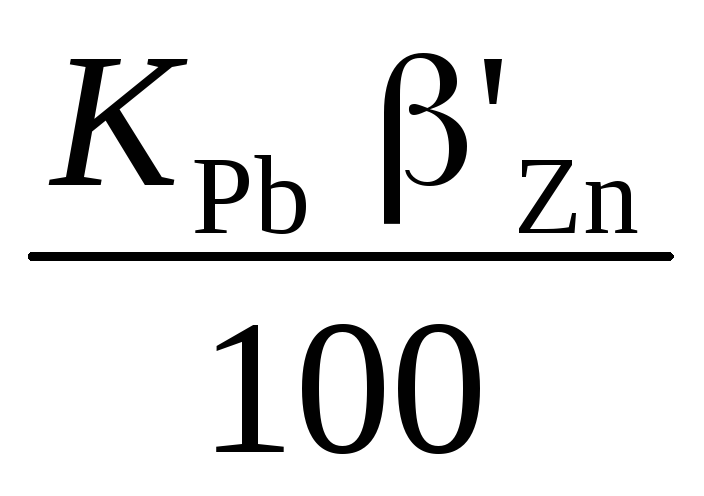 [т], а извлечение цинка в свинцовом
концентрате составит:
[т], а извлечение цинка в свинцовом
концентрате составит:
![]() .
.
Цинка в хвостах
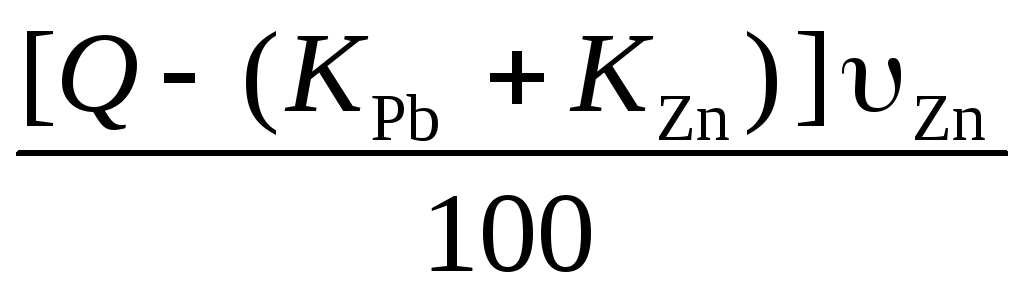 [т], а процент потерь цинка:
[т], а процент потерь цинка:
![]() .
.
