
- •Учебно-методические разработки для самостоятельной работы студентов по курсу «Теоретические основы защиты окружающей среды»
- •Часть II
- •Специальные методы очистки сточных вод и основные методы сепарации твердых отходов
- •Введение
- •Глава 1. Химические методы очистки сточных вод
- •1.1 Нейтрализация
- •1.1.1. Нейтрализация смешиванием
- •1.1.2. Нейтрализация добавлением реагентов
- •1.1.3. Нейтрализация фильтрованием кислых вод через нейтрализующие материалы
- •1.2. Нейтрализация кислыми газами
- •1.2.1. Окисление и восстановление
- •1.2.2. Окисление пероксидом водорода
- •1.2.3. Окисление кислородом воздуха
- •1.2.4. Озонирование
- •Контрольные вопросы
- •Глава 2. Явление осмоса и его использование при очистке сточных вод
- •2.1. Осмотическое давление
- •2.2. Биологическая роль осмотического давления
- •2.3. Законы осмотического давления
- •2.4. Термодинамика осмотического давления
- •Контрольные вопросы
- •Глава 3. Физические основы электродных процессов при очистке сточных вод от примеси
- •3.1. Явления электролиза, поляризации и перенапряжения
- •3.1.1 Электролиз
- •3.1.2. Кривая напряжения
- •3.1.3. Электродвижущие силы разложения
- •3.1.4. Потенциал разложения
- •3.1.5. Концентрационная поляризация
- •3.1.6. Деполяризация
- •3.1.7. Перенапряжение
- •3.2. Электрокапиллярные явления
- •3.2.1. Зависимость поверхностного напряжения от заряда
- •3.2.2. Влияние адсорбции на электрокапиллярную кривую
- •3.2.3. Проблема абсолютных потенциалов
- •3.3. Электрокинетические явления
- •3.3.1. Диффузионный двойной слой и электрокинетический потенциал
- •3.3.2. Емкость двойного слоя
- •3.3.3. Электроосмос
- •3.3.4. Потенциал течения
- •3.3.5. Электрофорез
- •3.3.6. Потенциалы осаждения
- •3.4. Электрохимические методы очистки сточных вод
- •3.4.1. Анодное окисление и катодное восстановление
- •3.4.2. Электрокоагуляция
- •3.4.3. Электрофлотация
- •3.4.4. Электродиализ
- •Контрольные вопросы
- •Глава 4. Физические основы процессов переработки твердых бытовых отходов
- •4.1. Процессы измельчения и дробления
- •4.1.1. Назначение операций дробления и измельчения
- •4.1.2. Степень дробления и измельчения
- •4.1.3. Стадиональность и схемы дробления и измельчения
- •4.1.4. Удельная поверхность диспергированного материала
- •4.1.5. Современные представления о разрушении твердого материала
- •4.1.6. Механические свойства твердых тел при простых видах деформации
- •4.1.7. Законы дробления
- •4.1.8. Способы дробления, классификация машин для дробления и измельчения
- •4.2. Процесс грохочения
- •4.2.1. Основные понятия и назначение грохочения
- •4.2.2. Просеивающая поверхность
- •4.2.3. Способы определения гранулометрического состава
- •4.2.4. Ситовый анализ
- •4.2.5. Характеристики крупности
- •4.2.6. Аналитическое представление характеристик крупности
- •4.2.7. Дифференциальные функции распределения по крупности
- •4.2.8. Вычисление поверхности и числа частиц по уравнениям суммарной характеристики крупности
- •4.2.9. Эффективность процесса грохочения
- •4.2.10. «Легкие», «трудные» и «затрудняющие» частицы
- •4.2.11. Вероятность прохождения частиц через отверстия сита
- •4.2.12. Факторы, влияющие на процесс грохочения
- •4.3. Электромагнитная сепарация. Физические основы процесса
- •4.4. Электростатическая сепарация. Физические основы процесса
- •4.5. Электродинамическая сепарация
- •4.6. Сепарация твердых материалов по коэффициенту трения
- •4.7. Сепарация на основе явления смачиваемости
- •4.8. Аэросепарация
- •4.9. Составление балансной схемы переработанного твердого сырья
- •4.9.1. Баланс материалов при переработке твердых отходов
- •4.9.2. Технологические и технико-экономические показатели переработки твердых отходов
- •Контрольные вопросы
- •Варианты домашнего задания по курсу «Теоретические основы защиты окружающей среды»
- •1. Отстаивание, сгущение, осветление.
- •2. Флотация
- •3. Экстракция
- •4. Дробление и грохочение
- •5. Измельчение и классификация
- •6. Магнитное и электрическое разделение
- •Примеры выполнения домашних заданий
- •Темы заданий для курсовых работ по курсу «Теоретические основы защиты окружающей среды»
- •Пример выполнения курсовой работы
- •Литература
- •Оглавление
- •Глава 1. Химические методы очистки сточных вод 6
- •Глава 2. Явление осмоса и его использование при очистке сточных вод 20
- •Глава 3. Физические основы электродных процессов при очистке сточных вод от примеси 31
- •Глава 4. Физические основы процессов переработки твердых бытовых отходов 73
3.1.2. Кривая напряжения
Соединим с внешним источником тока два платиновых электрода, опущенных в раствор серной кислоты, включив в цепь гальванометр. Приложим сначала небольшую электродвижущую силу, например 1 В. После короткого выброса стрелка гальванометра вернется почти к нулю, т.е. через цепь почти не будет проходить тока, и не будет наблюдаться электролиза. То же будет происходить при последовательном увеличении приложенной электродвижущей силы E до тех пор, пока она не превзойдет некоторую величину Ep (в данном примере 1,7 В), называемую электродвижущей силой разложения. При этой электродвижущей силе начинается разложение воды с выделением водорода на катоде и кислорода на аноде и появляется длительный ток, сила которого растет с увеличением приложенной электродвижущей силы E.
Кривая силы тока в функции от электродвижущей силы называется кривой напряжения. В простых случаях, не осложненных побочными факторами, она имеет вид, показанный на рис. 3.1.
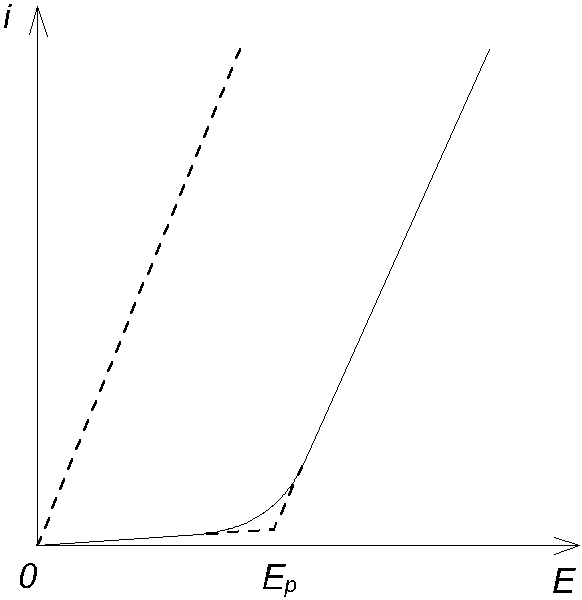
Рис.3.1 Кривая напряжения
Электродвижущую силу разложения можно найти как из положения точки изгиба этой кривой, так и по началу электролиза (появление пузырьков газов на электродах). Однако оба способа не очень точны.
Эти явления объясняются так. После включения внешней электродвижущей силы на электродах начинается выделение водорода и кислорода, что превращает катод в водородный электрод, а анод - в кислородный. При этом ячейка превращается в водородно-кислородный гальванический элемент, дающий собственную обратную электродвижущую силу, растущую по мере насыщения электродов газами до тех пор, пока она не станет равной приложенной электродвижущей силе E, после чего ток прекратится. Если увеличить E, то снова через короткое время наступит стационарное состояние с более высокой степенью насыщения электродов газами. Последнее не может однако расти безгранично. Когда достигнуто равновесие с внешним давлением, газы начинают покидать электроды в виде пузырьков, и дальнейший рост приложенной электродвижущей силы не будет сопровождаться ростом обратной электродвижущей силы, которая достигла наибольшей возможной величины Ep. Дальнейшее увеличение E сверх Ep будет давать длительный ток, растущий согласно (3.1), т.е. линейно, как это показано на рис.3.1. Наклон прямой определяется величиной сопротивления w ячейки.
Из рисунка видно, что при E<Ep также имеется небольшой длительно сохраняющийся остаточный ток, вызванный утечкой некоторых количеств водорода и кислорода из электродов путем диффузии, так что обратная электродвижущая сила всегда несколько отстает от приложенной. Ускорение диффузии путем нагревания или размешивания электролита увеличивает остаточный ток.
Рассмотрим теперь более простой случай, когда электролиз не изменяет природы электролитов, например ячейку из двух серебряных электродов в растворе AgNO3. Если пренебрегать концентрационными изменениями у электродов, сопровождающими электролиз, то обратная электродвижущая сила равна нулю и (3.1) превращается в
E = iw.
Тогда кривая напряжения имеет форму прямой, выходящей из начала координатных осей, как изображено пунктиром на рис.3.1.
Если электролиз сопровождается необратимыми процессами, из которых наиболее часто встречаются рассматриваемые ниже перенапряжение и концентрационная поляризация, то кривая напряжения имеет более сложный вид.
Изменения, происходящие в гальванической цепи при прохождении через нее тока, называют поляризацией (не смешивать с диэлектрической поляризацией молекул в электрическом поле.), а вызываемую ими обратную электродвижущую силу называют электродвижущей силой поляризации. Эти изменения, большей частью термодинамически необратимые, могут быть как химическими, так и концентрационными.
