
- •Учебно-методические разработки для самостоятельной работы студентов по курсу «Теоретические основы защиты окружающей среды»
- •Часть II
- •Специальные методы очистки сточных вод и основные методы сепарации твердых отходов
- •Введение
- •Глава 1. Химические методы очистки сточных вод
- •1.1 Нейтрализация
- •1.1.1. Нейтрализация смешиванием
- •1.1.2. Нейтрализация добавлением реагентов
- •1.1.3. Нейтрализация фильтрованием кислых вод через нейтрализующие материалы
- •1.2. Нейтрализация кислыми газами
- •1.2.1. Окисление и восстановление
- •1.2.2. Окисление пероксидом водорода
- •1.2.3. Окисление кислородом воздуха
- •1.2.4. Озонирование
- •Контрольные вопросы
- •Глава 2. Явление осмоса и его использование при очистке сточных вод
- •2.1. Осмотическое давление
- •2.2. Биологическая роль осмотического давления
- •2.3. Законы осмотического давления
- •2.4. Термодинамика осмотического давления
- •Контрольные вопросы
- •Глава 3. Физические основы электродных процессов при очистке сточных вод от примеси
- •3.1. Явления электролиза, поляризации и перенапряжения
- •3.1.1 Электролиз
- •3.1.2. Кривая напряжения
- •3.1.3. Электродвижущие силы разложения
- •3.1.4. Потенциал разложения
- •3.1.5. Концентрационная поляризация
- •3.1.6. Деполяризация
- •3.1.7. Перенапряжение
- •3.2. Электрокапиллярные явления
- •3.2.1. Зависимость поверхностного напряжения от заряда
- •3.2.2. Влияние адсорбции на электрокапиллярную кривую
- •3.2.3. Проблема абсолютных потенциалов
- •3.3. Электрокинетические явления
- •3.3.1. Диффузионный двойной слой и электрокинетический потенциал
- •3.3.2. Емкость двойного слоя
- •3.3.3. Электроосмос
- •3.3.4. Потенциал течения
- •3.3.5. Электрофорез
- •3.3.6. Потенциалы осаждения
- •3.4. Электрохимические методы очистки сточных вод
- •3.4.1. Анодное окисление и катодное восстановление
- •3.4.2. Электрокоагуляция
- •3.4.3. Электрофлотация
- •3.4.4. Электродиализ
- •Контрольные вопросы
- •Глава 4. Физические основы процессов переработки твердых бытовых отходов
- •4.1. Процессы измельчения и дробления
- •4.1.1. Назначение операций дробления и измельчения
- •4.1.2. Степень дробления и измельчения
- •4.1.3. Стадиональность и схемы дробления и измельчения
- •4.1.4. Удельная поверхность диспергированного материала
- •4.1.5. Современные представления о разрушении твердого материала
- •4.1.6. Механические свойства твердых тел при простых видах деформации
- •4.1.7. Законы дробления
- •4.1.8. Способы дробления, классификация машин для дробления и измельчения
- •4.2. Процесс грохочения
- •4.2.1. Основные понятия и назначение грохочения
- •4.2.2. Просеивающая поверхность
- •4.2.3. Способы определения гранулометрического состава
- •4.2.4. Ситовый анализ
- •4.2.5. Характеристики крупности
- •4.2.6. Аналитическое представление характеристик крупности
- •4.2.7. Дифференциальные функции распределения по крупности
- •4.2.8. Вычисление поверхности и числа частиц по уравнениям суммарной характеристики крупности
- •4.2.9. Эффективность процесса грохочения
- •4.2.10. «Легкие», «трудные» и «затрудняющие» частицы
- •4.2.11. Вероятность прохождения частиц через отверстия сита
- •4.2.12. Факторы, влияющие на процесс грохочения
- •4.3. Электромагнитная сепарация. Физические основы процесса
- •4.4. Электростатическая сепарация. Физические основы процесса
- •4.5. Электродинамическая сепарация
- •4.6. Сепарация твердых материалов по коэффициенту трения
- •4.7. Сепарация на основе явления смачиваемости
- •4.8. Аэросепарация
- •4.9. Составление балансной схемы переработанного твердого сырья
- •4.9.1. Баланс материалов при переработке твердых отходов
- •4.9.2. Технологические и технико-экономические показатели переработки твердых отходов
- •Контрольные вопросы
- •Варианты домашнего задания по курсу «Теоретические основы защиты окружающей среды»
- •1. Отстаивание, сгущение, осветление.
- •2. Флотация
- •3. Экстракция
- •4. Дробление и грохочение
- •5. Измельчение и классификация
- •6. Магнитное и электрическое разделение
- •Примеры выполнения домашних заданий
- •Темы заданий для курсовых работ по курсу «Теоретические основы защиты окружающей среды»
- •Пример выполнения курсовой работы
- •Литература
- •Оглавление
- •Глава 1. Химические методы очистки сточных вод 6
- •Глава 2. Явление осмоса и его использование при очистке сточных вод 20
- •Глава 3. Физические основы электродных процессов при очистке сточных вод от примеси 31
- •Глава 4. Физические основы процессов переработки твердых бытовых отходов 73
3.3.2. Емкость двойного слоя
Подобно конденсатору двойной слой имеет электрическую емкость, зависящую от его строения. Ее можно в принципе, измерять так же, как и обыкновенный конденсатор: по количеству электричества, необходимому для увеличения потенциала на единицу. Другой способ основан на получении электрокапиллярной кривой, из кривизны которой может быть найдена емкость С
![]() С.
С.
Изучение емкости двойных слоев, особенно в комбинации с адсорбционными измерениями, дает детальные сведения об их строении. При уменьшении степени диффузности емкость растет, так как заряды сближаются. В согласии с этим А.Н. Фрумкин, М.Н. Проскурин и М.И. Ворсина (1939) установили, что повышение концентрации раствора KCl и других электролитов (вызывающее, как было указано, уменьшение диффузии) увеличивает емкость двойного слоя ртути. При данной концентрации кривая зависимости емкости от поляризующего потенциала имеет минимум точно при том потенциале, который отвечает максимуму электрокапиллярной кривой. В этой точке поверхность ртути не заряжена и поэтому двойной слой наиболее диффузен, а емкость наименьшая. Минимум исчезает в 0,1н. и более концентрированных растворах KCl, где двойной слой становится плоским. Эти исследования позволили получить экспериментальные доказательства диффузного строения двойных слоев. Из измеренных емкостей были вычислены ξ-потенциалы в удовлетворительном согласии с тем, что предлагает теория. Другой, не зависящий от часто противоречивых электрокинетических измерений способ вычисления ξ-потенциала основан на измерении перенапряжения η в функции от концентрации электролитов. При постоянной плотности тока и постоянной концентрации теория дает η = const - ξ. Величины ξ, вычисленные из измеренных η, хорошо согласуются с результатами предыдущего метода и с теорией. Величину const можно найти из предельного η при больших добавках электролитов, когда ξ→0.
3.3.3. Электроосмос
В электрическом поле возникает движение жидкости относительно твердой поверхности. Это явление называется электроосмосом (рис. 3.9).

Рис. 3.9. Схема измерения электроосмоса
Капилляр К соединяет два сосуда, наполненные жидкостью, с введенными в них электродами Е, соединенными с источниками тока. Скорость течения жидкости через капилляр может быть измерена по перемещению ее мениска в трубке М. Капилляр может быть заменен пористой перегородкой. Направление течения зависит от материала твердой поверхности и от состава жидкости. Например, вода в стеклянном капилляре заряжается относительно его стенок положительно, потому и течет в направлении к отрицательному электроду.
Электроосмос, так же как и рассматриваемый ниже электрофорез, был открыт в России Ф.Ф. Рейсом (1809). Его теория была разработана Гельмгольцом (1879) и дополнена Смолуховским (1903), Перреном (1904) и др. Это явление обусловлено образованием двойного электрического слоя на границе твердого тела с жидкостью. В случае диэлектрика он возникает из-за неодинаковой адсорбции ионов обоих знаков. Благодаря этому двойному слою твердая поверхность и прилегающая к ней тонкая пленка жидкости с плоской частью двойного слоя заряжаются одним знаком, а остальной объем жидкости, содержащий диффузную часть двойного слоя, - другим знаком, что вызывает его движение в электрическом поле. Таки образом, это явление существенно зависит от знака и величины электрокинетического потенциала ξ. Обозначив приложенную электродвижущую силу Е, сечение капилляра (или сумму сечений пор) q, расстояние между электродами l, диэлектрическую постоянную жидкости D и ее вязкость равна η, можно согласно теории записать скорость течения жидкости:
![]() . (3.3)
. (3.3)
Уравнение (3.3) получается из условия равенства силы трения и приложенной электродвижущей силы. Оно не совсем точно из-за изменения электропроводности жидкости в капилляре вследствие адсорбции ионов его стенкам и переноса их движущейся жидкостью.
Так как в (3.3) все величины, кроме ξ, известны или могут быть изменены, то из наблюдений электроосмоса можно найти величину электрокинетического потенциала большей частью в удовлетворительном согласии с величиной, получаемой из других рассматриваемых ниже электрокинетических явлений. Она обычно не превышает 0,05÷0,1 В. Поэтому для получения заметных скоростей электроосмоса приложенное поле Е должно иметь большое напряжение порядка десятков и сотен В. Например, при градиенте потенциала в 1 В/см и ξ=0,05 В скорость u равна лишь 1·10-3 см/сек при q=0,01 см2.
Элктроосмос имеет ряд технических применений. Например, помещая водные гали (глину, силикагель, клей и др.) между сетчатыми электродами, можно их обезвоживать. Дубление кожи сильно ускоряется электроосмотическим прониканием дубящего раствора в ее поры, если ее поместить в этом растворе между двумя электродами. Электроосмосом воды через ряд пористых диафрагм можно ее очистить от большинства взвешенных и растворенных примесей; этот способ очистки мало уступает дистилляции.
Большинство твердых поверхностей (стекло, глина, асбест, благородные металлы, шерсть и др.) заряжается отрицательно относительно воды. Неблагородные металлы, ряд окислов, сульфидов и других неорганических соединений, наоборот, заряжаются положительно.
Прибавление электролитов, особенно поливалентных, сильно влияет на величину ξ-потенциала, вплоть до перемены его знака, что сопровождается переменой направления электроосмоса. Пример довольно сложных соотношений между ξ-потенциалом, концентрацией и валентностью ионов показан на рис.3.10, относящийся к границе воды со стеклом.
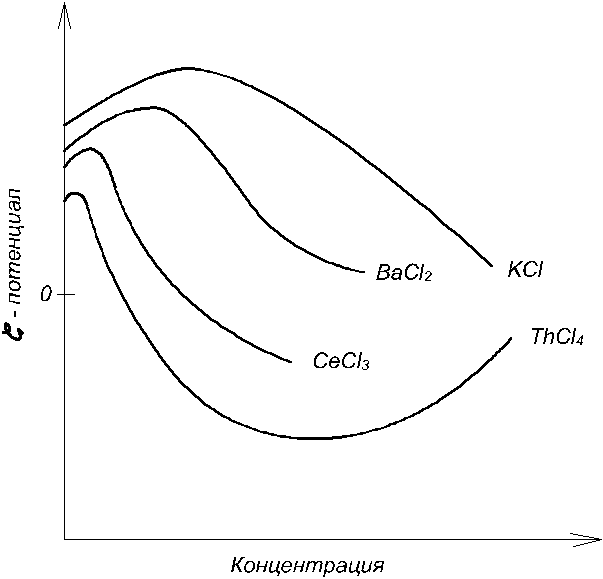
Рис.3.10. Зависимость ξ -потенциала то концентрации электролита
Прибавление 0,2 мг/л изменяет его направление потенциала на обратное. Как уже указывалось, в более концентрированных растворах ξ-потенциал приближается к нулю, и электроосмос прекращается.
Еще большее влияние, чем электролиты, оказывают сильно поверхностно-активные вещества, хорошо адсорбируемые стенкой Часто незначительные их количества оказывают огромное влияние на величину ξ-потенциала и на скорость элетроосмоса, а также на другие электрокинетические явления.
