- •Российский университет дружбы народов
- •К практическим занятиям по биохимии
- •Авторский коллектив:
- •Предисловие как пользоваться этим учебным пособием?
- •Список сокращений и условных обозначений
- •Техника безопасности при работе в биохимической лаборатории
- •1. Общие требования безопасности
- •Классификация химических реактивов в биохимической лаборатории
- •2. Требования безопасности перед началом работ
- •3. Требования безопасности во время работы
- •4. Требование безопасности в аварийных ситуациях
- •5.Требование безопасности по окончании работы
- •Раздел 1: Аминокислоты и простые белки Введение
- •1.1 Проверка знаний по органической химии
- •1.2. Цветные реакции на белки и аминокислоты. Реакции осаждения и денатурации белков а. Цветные реакции на белки и аминокислоты
- •Б. Реакции осаждения и денатурации белков
- •1.3. Количественное определение белка биуретовым методом. Построение калибровочных кривых
- •1 .4. Диализ белков. Бумажная хроматография аминокислот
- •А. Диализ
- •1.5. Коллоквиум I по теме «Аминокислоты и простые белки»
- •Раздел 2: Сложные белки, нуклеиновые кислоты и ферменты Введение
- •2.1 Действие амилазы на крахмал. Влияние температуры на активность амилазы а. Действие амилазы на крахмал
- •Б. Изучение влияния температуры на скорость ферментативной реакции
- •2.2. Количественное определение активности щелочной фосфатазы в сыворотке крови с п-нитрофенилфосфатом
- •2.3. Коллоквиум II по теме: «Сложные белки, нуклеиновые кислоты и ферменты» Вопросы, для самостоятельной подготовки
- •Варианты письменной части коллоквиума
- •Варианты заданий на компьютерном тестировании
- •Правильные ответы
- •Раздел 3: Витамины, липиды, гормоны Введение
- •3.1. Количественное определение витаминов с и р.
- •3.3. Влияние гормонов на содержание глюкозы в крови
- •3.4. Коллоквиум III по теме «Витамины, липиды, гормоны»
- •Раздел 4: Метаболизм. Биоэнергетика клеток. Химия и обмен углеводов Введение
- •4.1. Специфичность действия ферментов распада углеводов: амилазы и сахаразы
- •4.2. Количественное определение глюкозы. Построение «сахарных кривых»
- •4.3. Определение активности сукцинатдегидрогеназы в мышцах. Количественное определение пирувата в моче
- •4.4 Коллоквиум IV по теме: «Метаболизм. Биоэнергетика клеток. Химия и обмен углеводов»
- •Правильные ответы
- •Раздел 5: Обмен липидов и его регуляция Введение
- •5.1. Кинетика действия липазы.
- •5.2. Количественное определение фосфатидилхолинов (лецитинов) по фосфору
- •I. Приготовление рабочего раствора сыворотки.
- •II. Определение концентрации фосфатидолхолинов по содержанию фосфора.
- •5.3. Количественное определение холестерина в сыворотке крови
- •5.4. Количественное определение малонового диальдегида
- •5.5. Коллоквиум по теме «Обмен липидов»
- •Раздел 6: Переваривание белков и обмен аминокислот
- •6.1. Количественный анализ желудочного сока. Определение свободной, связанной, общей соляной кислоты и общей кислотности желудочного сока.
- •6.2. Количественное определение аспартатаминотрансферазы и аланинаминотрансферазы в сыворотке крови
- •6.3. Доказательство проявления активности аланин-аминотрансферазы (АлАт) методом бумажной хроматографии
- •6.4. Экспресс-метод определения повышенного содержания фенилаланина в плазме крови
- •6.5. Количественное определение мочевины в моче ферментативным уреазным/фенол-гипохлоритным методом
- •6.6. Количественное определение креатинина в моче
- •6.7. Коллоквиум по теме: «Обмен простых белков» Вопросы, для самостоятельной подготовки
- •Варианты письменной части коллоквиума
- •Правильные ответы
- •Раздел 7: Обмен хромопротеинов и нуклеопротеинов. Биохимия крови и мочи. Биосинтез нуклеиновых кислот и белков. Введение
- •7.1. Определение общего билирубина в сыворотке крови
- •7.2. Количественное определение мочевой кислоты в моче
- •7.3. А. Определение активности -амилазы в моче
- •7.3. Б. Составные части мочи в норме и при патологии
- •7.4. Определение активности холинэстеразы в сыворотке крови
- •7.5. Определение активности лактатдегидрогеназы в сыворотке крови
- •7.6. Коллоквиум по теме: «Обмен хромопротеинов и нуклеопротеинов. Биохимия крови и мочи. Биосинтез нуклеиновых кислот и белка». Вопросы, для самостоятельной подготовки
- •Варианты письменной части коллоквиума
- •Правильные ответы
- •Раздел 8: Подготовка к экзамену
- •8.1. Основные вопросы, выносимые на обсуждение
- •8.2. Пример экзаменационного тестового задания по курсу биохимии
- •59. Найти соответствие между процессом и его графическим изображением
- •60. Цикл мочевинообразования установил
- •Ответы к экзаменационному тесту
- •Раздел 9: Приложения
- •9.1. Термины, различающиеся по смыслу, но сходные по написанию и звучанию
- •9.2. Стандартные биохимические наборы и реактивы, используемые в практикуме
- •9.3. Рекомендуемая литература
- •Содержание
- •Раздел 7: Обмен хромопротеинов и нуклеопротеинов. Биохимия крови и мочи. Биосинтез нуклеиновых кислот и белков. 126
- •Раздел 8: Подготовка к экзамену 148
- •Раздел 9: Приложения 161
1.1 Проверка знаний по органической химии
1) Ответить на каждый вопрос однозначно: «да» или «нет»
Кислород входит в состав углеводородов.
Фенол обладает кислыми свойствами.
Аминокислоты могут иметь гетероциклическую структуру.
Между молекулами органических кислот возможно образование сложноэфирной связи.
Глицерин относится к классу спиртов.
Кислые свойства дикарбоновых аминокислот обусловлены наличием карбоксильных групп.
Обладают ли белки свойствами амфотерных электролитов?
Одинакова ли структура белков и структура нуклеиновых кислот?
Может ли в состав белков входить сера?
Образуют ли белки при растворении в воде истинные растворы?
Возможен ли синтез белка в лабораторных условиях?
Все ли белки состоят из аминокислот?
2) Выбрать только один правильный ответ
Положительным зарядом может обладать:
|
К циклическим соединениям не относятся:
|
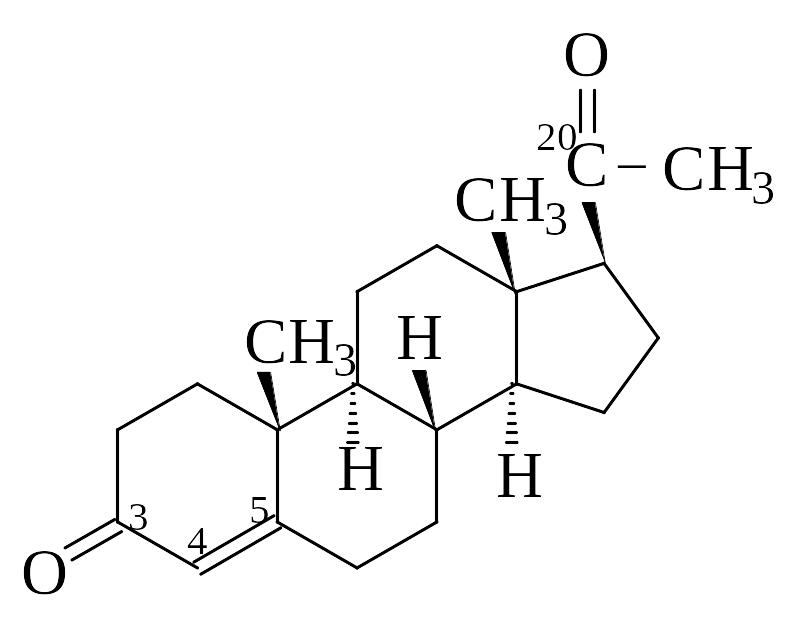
3) Найти соответствие между формулой и принадлежностью к классу соединений
Химическая формула |
Класс соединений |
|
1. |
|
А. стероиды |
2. |
|
Б. углеводы |
3. |
|
В. аминокислоты |
4. |
|
Г. витамины |
5. |
|
Д. терпены |
1.2. Цветные реакции на белки и аминокислоты. Реакции осаждения и денатурации белков а. Цветные реакции на белки и аминокислоты
Белки — полимерные соединения, построенные из аминокислот, которые соединены между собой пептидными связями. Аминокислоты – производные карбоновых кислот, у которых три валентности -углеродного атома всегда образованы одним атомом водорода (—H), аминогруппой (—NH2) и карбоксильной группой (—COOH). Четвертая валентность может быть образована одним атомом водорода (—Н у глицина) или группировкой атомов, называемой радикалом аминокислот (—R). В составе радикалов многие аминокислоты имеют реакционно-способные (функциональные) группы. Например:
1. Сульфгидрильная группа (—SH) у цистеина.
2. Тиометильная группа (—S–CH3) у метионина.
3. Гидроксильная группа (-ОН) у серина, треонина и тирозина.
Цель работы
Провести цветные реакции с двумя растворами (I и II)1, один из которых содержит овальбумин (яичный белок), а другой – желатину (овальбумин содержит все 20 аминокислот, а желатина только 17), и определить, в каком растворе содержится овальбумин, а в каком – желатина.
Принцип метода
Ряд химических реактивов специфически взаимодействуют (реагируют) с функциональными группами аминокислот (как свободных, так и в составе пептидов или белков) в результате чего развивается специфическое окрашивание. Такие реакции называют цветными реакциями. Интенсивность окраски в цветных реакциях пропорциональна количеству реагирующих функциональных групп. Поэтому цветные реакции могут быть использованы для качественного и количественного определения белков, для определения присутствующих в них аминокислот или для анализа состава белков.
Так, например:
биуретовой реакцией определяют наличие пептидных групп в олигопептидах и в белках (универсальная для любых белков).
нингидриновой реакцией определяют наличие -аминогрупп в свободных аминокислотах, а также в аминокислотах олигопептидов и белков (универсальная для любых белков).
ксантопротеиновой реакцией определяют наличие в белках ароматических аминокислот.
реакцией Фоля определяют наличие в составе белков серосодержащей аминокислоты – цистеина.
Выполнение работы
Реакция |
№ пробирок |
Ход определения |
Окраска |
Чем обусловлена реакция |
Биуретовая |
1 |
Раствор I - 5 капель, 10% NaOH - 5 капель, 1 % CuSO4 - 1 капля |
|
|
2 |
Раствор II - 5 капель, 10% NaOH - 5 капель, 1 % CuSO4 - 1 капля |
|
|
|
Нингидри- новая |
1 |
Раствор I - 5 капель, 1% раствор нингидрина в ацетоне - 2 капли, нагревают |
|
|
2 |
Раствор II - 5 капель, 1% раствор нингидрина в ацетоне - 2 капли, нагревают |
|
|
|
Ксанто-протеиновая |
1 |
Раствор I - 5 капель, конц. HNO3 - 3 капли, осторожно нагревают |
|
|
2 |
Раствор II - 5 капель, конц. HNO3 - 3 капли, осторожно нагревают |
|
|
|
Фоля |
1 |
Раствор I - 5 капель, 30 % NaOH - 5 капель, 5 % (CH3COO)2Pb - 1 капля, нагревают до кипения |
|
|
2 |
Раствор II - 5 капель, 30 % NaOH - 5 капель, 5 % (CH3COO)2Pb - 1 капля, нагревают до кипения |
|
|
Студенты могут проводить указанные цветные реакции на 4-х предметных стеклах1:
На один край каждого стекла наносят 1 каплю раствора I, на другой – раствора II.
Биуретовая реакция. К белкам на первом стекле последовательно добавляют 1 каплю 10% NаOH и 1 каплю 1% CuSO4, аккуратно перемешивая стеклянной палочкой.
Нингидриновая реакция. К белкам на втором стекле добавляют 1 каплю раствора нингидрина. Перемешивают. Осторожно нагревают до кипения.
Ксантопротеиновая реакция. К белкам на третьем стекле добавляют 1 каплю концентрированной HNO3. Перемешивают. Осторожно нагревают.
Реакция Фоля. К белкам на четвертом стекле добавляют 1 каплю 30% NaOH и 1 каплю (CH3OO)2Pb. Нагревают до кипения.
Выводы
Заполнить таблицу, сравнить полученные окраски, определить, в каком растворе овальбумин, а в каком – желатина и обосновать этот выбор.