
- •Сборник методических указаний к лабораторным работам
- •«Аналитическая химия и физико-химические методы анализа»
- •Содержание
- •Часть I. Химические методы анализа
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов (в присутствии вольфрама)
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Выполнение реакций обнаружения анионов
- •Обнаружение карбонатов.
- •Обнаружение нитратов
- •Обнаружение ортофосфатов
- •Обнаружение силикатов
- •Обнаружение сульфидов
- •Обнаружение сульфатов
- •Обнаружение хлоридов
- •Вопросы для самоподготовки
- •Гравиметрия (весовой анализ)
- •Цель и задачи работы
- •Программа работы Приборы и реактивы.
- •Определение сульфатов
- •Ход работы.
- •Определение железа
- •Ход работы.
- •Определение никеля
- •Ход работы.
- •Вопросы для самоподготовки
- •Протолитометрический анализ
- •Ход работы
- •Контрольная задача. Определение уксусной кислоты.
- •Вопросы для самоподготовки.
- •Перманганатометрия.
- •Приготовление первичного стандарта щавелевой кислоты
- •Ход работы:
- •Контрольная задача. Определение железа (II)
- •Ход работы:
- •Вопросы для самоподготовки.
- •Иодометрия
- •Стандартизация рабочего раствора тиосульфата натрия (вторичного стандарта).
- •Ход работы:
- •Контрольная задача: Определение меди (II).
- •Ход определения:
- •Вопросы для самоподготовки.
- •Комплексонометрия.
- •Цель и задачи работы.
- •Оборудование и реактивы:
- •Программа работы
- •Определение кальция
- •Ход работы:
- •Определение железа
- •Ход работы
- •Вопросы для самоподготовки
- •Часть II. Инструментальные методы анализа
- •Определение калия по методу градуировочного графика
- •Ход работы:
- •Приготовление стандартных растворов:
- •Подготовка прибора к работе:
- •Построение градуировочного графика
- •Контрольная задача. Определение содержания калия в анализируемом растворе
- •Фотометрический анализ
- •Выбор светофильтра
- •Построение градуировочного графика
- •Контрольная задача. Определение содержания меди (II) в анализируемом растворе
- •Определение железа (III) методом градуировочного графика
- •Фототурбидиметрия.
- •Ход работы:
- •Приготовление стандартных растворов и раствора сравнения:
- •Построение градуировочного графика:
- •Контрольная задача. Определение содержания в растворе.
- •Вопросы для самоконтроля
- •Рефрактометрия
- •Цель и задачи работы
- •Программа работы
- •Рефрактометрическое определение сахара в молоке.
- •Приборы и реактивы:
- •Ход работы:
- •Подготовка пробы к анализу:
- •Порядок работы на рефрактометре:
- •Контрольная задача Определение содержания сахара в анализируемом образце:
- •Определение содержания хлорида натрия в водном растворе. Приборы и реактивы.
- •Ход работы:
- •Приготовление стандартных растворов:
- •Построение градуировочного графика.
- •Контрольная задача. Определение содержания хлорида натрия в анализируемом растворе
- •Вопросы для самоподготовки
- •Потенциометрия
- •Цель и задачи работы
- •Программа работы
- •Определение хлородородной и уксусной кислот в растворе при их совместном присутствии методом потенциометрического титрования.
- •Приборы и реактивы
- •Ход работы
- •Установление титра рабочего раствора
- •Подготовка анализируемого образца к титрованию
- •Подготовка иономера к работе в режиме определения рН
- •Контрольная задача. Определение содержания хлороводородной и уксусной кислот в анализируемом образце
- •Вопросы для самоподготовки.
- •Кондуктометрия.
- •Цель и задачи работы.
- •Программа работы.
- •Определение слабой кислоты и соли слабого основания в их смеси.
- •Приборы и реактивы:
- •Ход работы:
- •12.2.1.1. Установление титра рабочего раствора :
- •12.2.1.2. Подготовка анализируемого образца к титрованию:
- •12.2.1.3. Контрольная задача. Определение содержания борной кислоты и солянокислого гидроксиламина в испытуемой смеси:
- •Определение ионовив их смеси.
- •Приборы и реактивы:
- •Подготовка анализируемого образца к титрованию:проводят по пункту 12.2.1.2.
- •Контрольная задача. Определение содержания солей никеля (II) и кальция в испытуемой смеси
- •Вопросы для самоконтроля.
- •13. Газохроматографический метод определения содержания токсичных микропримесей
- •13.1. Цель работы:
- •13.2. Объекты и средства исследования.
- •13.3. Программа работы
- •13.3.1. Приготовление градуировочных смесей
- •Условия хроматографирования с капиллярными колонками:
- •Литература:
Определение железа (III) методом градуировочного графика
Метод основан на
образовании окрашенного красного
комплекса ионов железа с сульфосалициловой
кислотой состава 1:2, имеющего максимальный
выход при
![]() = 4.
= 4.
Приборы и реактивы:
Фотоэлектроколориметр КФК-2;
Рабочий раствор
 ,
, = 0,1 мг/см3 (навеску 0,8663 г
= 0,1 мг/см3 (навеску 0,8663 г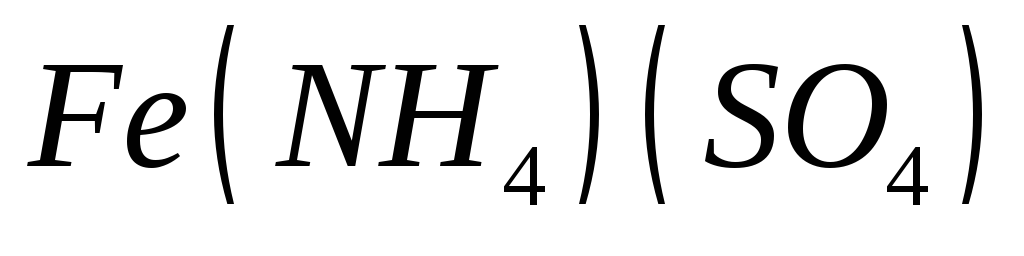
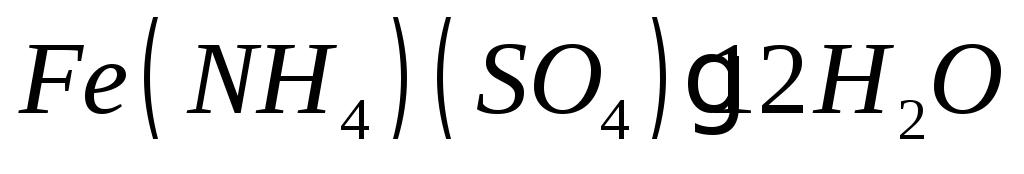 квалификации х.ч., растворяют в 25 см3
раствора
квалификации х.ч., растворяют в 25 см3
раствора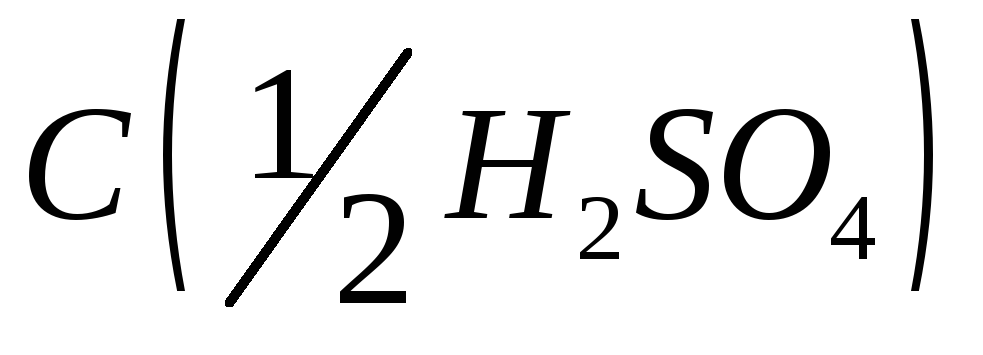 = 2 М и доводят объём раствора до 1 дм3дистиллированной водой);
= 2 М и доводят объём раствора до 1 дм3дистиллированной водой);Сульфосалициловая кислота х.ч., водный раствор
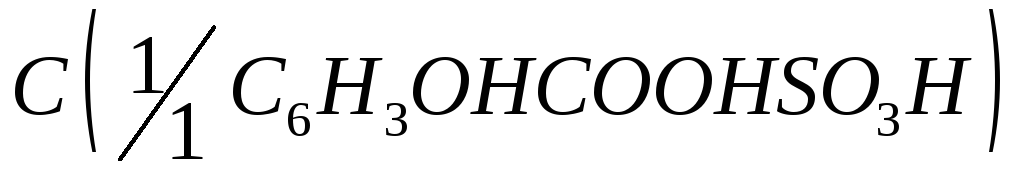 = 0,01 моль/дм3;
= 0,01 моль/дм3;Ацетатный буферный раствор,
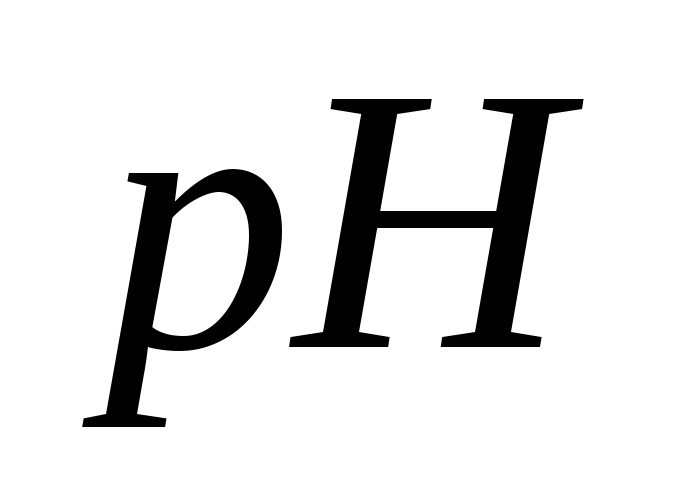 = 4,0;
= 4,0;Мерные колбы вместимостью 50 см3, 7штук;
Градуированные пипетки вместимостью 1 см3и 5 см3по 1 шт.
Мерный цилиндр вместимостью 30 см3,1 шт.
Ход работы:
Приготовление стандартных растворов:
Готовят пять стандартных растворов, содержащих 0,1; 0,2; 0,3; 0,4; 0,5; и 0,6 мг железа (III) в 50 см3по методике, описанной в пункте 8.2.1.1, используя в качестве реагентов 30 см3раствора сульфосалициловой кислоты и 5 см3буферного раствора.
Выбор светофильтра осуществляется по пyнкту 8.2.1.2
Построение градуировочного графика:
Стандартные растворы фотометрируют относительно раствора сравнения, содержащего все, предусмотренные методикой компоненты за исключением определяемого иона.
Результаты измерений заносят в таблицу 8.2.
Контрольная задача. Определение содержания железа (III) в анализируемом растворе:
К анализируемому раствору приливают 30 см3раствора сульфосалициловой кислоты и 5 см3буферного раствора, доводят объём до 50 см3дистиллированной водой.
Фотометрирование проводят через 10 минут относительно раствора сравнения. Измерения проводят пять раз и по среднему результату графически находят содержание железа (III) в пробе, данные вносят в таблицу 8.2.
.
Вопросы для самоконтроля
Какова природа возникновения спектров поглощения?
Спектры каких переходов используются в фотометрии?
Основной закон светопоглощения и его параметры?
Какие факторы влияют на оптическую плотность раствора и молярный коэффициент светопоглощения?
Физический смысл молярного коэффициента светопоглощения?
Причины отклонения от закона Бугера-Ламберта-Бера?
Классификация фотометрических методов анализа?
Принципиальная схема приборов для абсорбционной фотометрии и их работа?
Назначение основных узлов фотометрических приборов?
Спектральные характеристики растворов?
Принципы выбора аналитических длин волн?
Оптимальные условия фотометрических измерений?
Фотометрические реагенты и требования, предъявляемые к ним?
Приёмы, применяемые для фотометрических измерений?
Качественный и количественный анализ в фотометрии?
Определение смеси светопоглощающих веществ?
Принципы фотометрического титрования?
Область фактического применения фотометрических методов анализа?
Метрологические характеристики фотометрических методов анализа?
Какие из соединений можно определять в УФ-области спектра
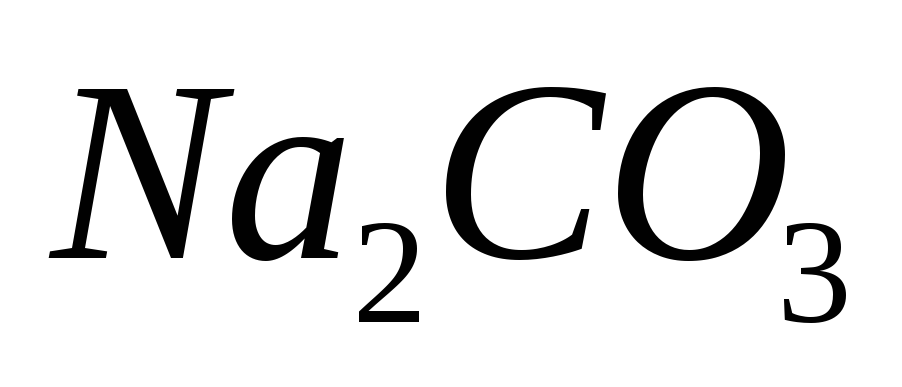 ,
,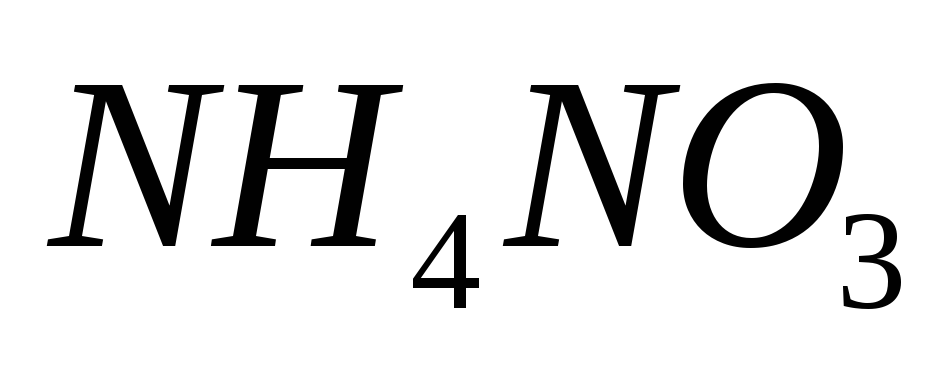 ,
,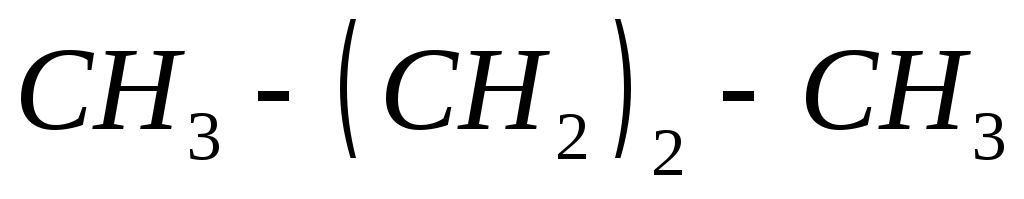 ,
, ?
?Какие из соединений можно определять в видимой области
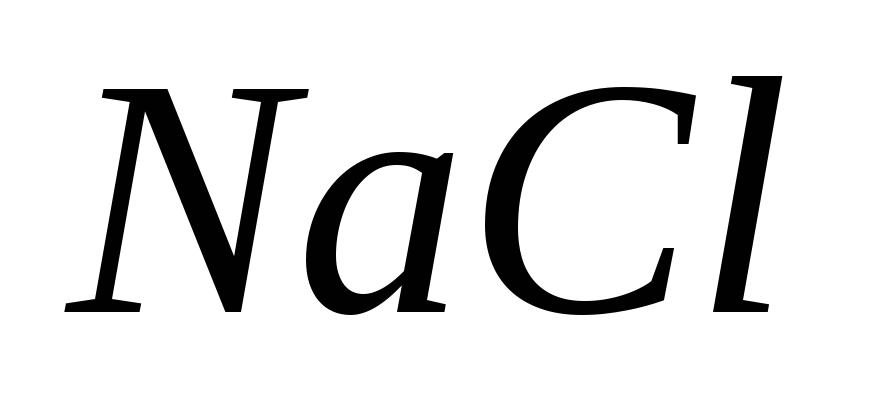 ,
,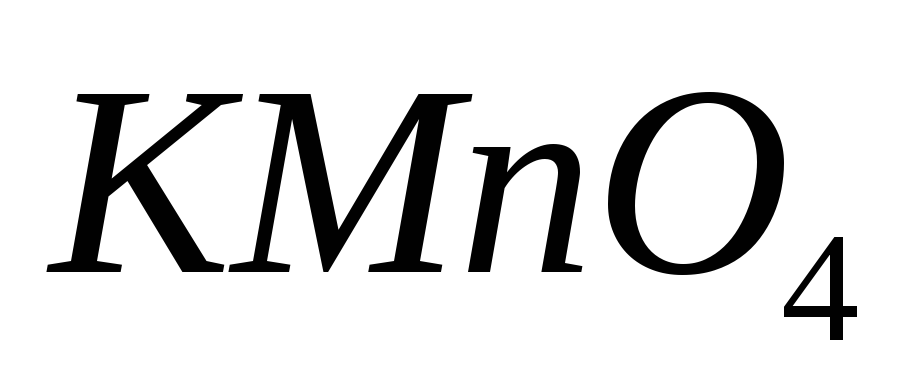 ,
,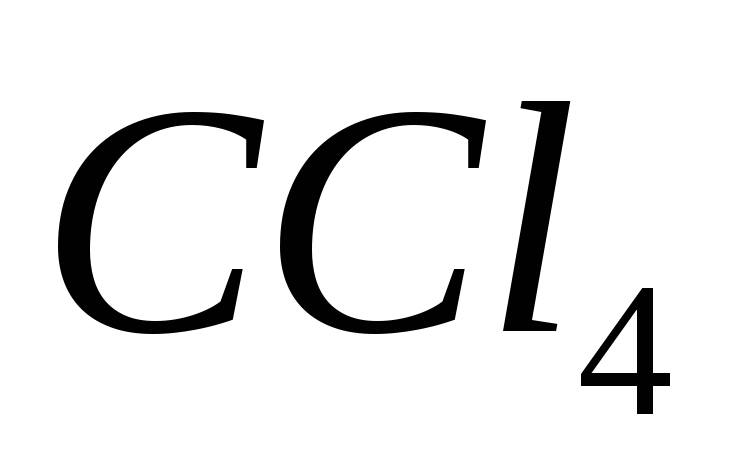 ?
?Предложите оптимальные условия (интервал b и c) для фотометрического определения титана с Н2О2(молярный коэффициент поглощения равен 720).
Вычислите молярный коэффициент поглощения соединения железа, если А = 0,75, b = 5 см, в 50 см3раствора содержится 0,005 г железа.
Рассчитайте оптическую плотность раствора, светопропускание которого равно 60%.
