
- •Сборник методических указаний к лабораторным работам
- •«Аналитическая химия и физико-химические методы анализа»
- •Содержание
- •Часть I. Химические методы анализа
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов (в присутствии вольфрама)
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Выполнение реакций обнаружения анионов
- •Обнаружение карбонатов.
- •Обнаружение нитратов
- •Обнаружение ортофосфатов
- •Обнаружение силикатов
- •Обнаружение сульфидов
- •Обнаружение сульфатов
- •Обнаружение хлоридов
- •Вопросы для самоподготовки
- •Гравиметрия (весовой анализ)
- •Цель и задачи работы
- •Программа работы Приборы и реактивы.
- •Определение сульфатов
- •Ход работы.
- •Определение железа
- •Ход работы.
- •Определение никеля
- •Ход работы.
- •Вопросы для самоподготовки
- •Протолитометрический анализ
- •Ход работы
- •Контрольная задача. Определение уксусной кислоты.
- •Вопросы для самоподготовки.
- •Перманганатометрия.
- •Приготовление первичного стандарта щавелевой кислоты
- •Ход работы:
- •Контрольная задача. Определение железа (II)
- •Ход работы:
- •Вопросы для самоподготовки.
- •Иодометрия
- •Стандартизация рабочего раствора тиосульфата натрия (вторичного стандарта).
- •Ход работы:
- •Контрольная задача: Определение меди (II).
- •Ход определения:
- •Вопросы для самоподготовки.
- •Комплексонометрия.
- •Цель и задачи работы.
- •Оборудование и реактивы:
- •Программа работы
- •Определение кальция
- •Ход работы:
- •Определение железа
- •Ход работы
- •Вопросы для самоподготовки
- •Часть II. Инструментальные методы анализа
- •Определение калия по методу градуировочного графика
- •Ход работы:
- •Приготовление стандартных растворов:
- •Подготовка прибора к работе:
- •Построение градуировочного графика
- •Контрольная задача. Определение содержания калия в анализируемом растворе
- •Фотометрический анализ
- •Выбор светофильтра
- •Построение градуировочного графика
- •Контрольная задача. Определение содержания меди (II) в анализируемом растворе
- •Определение железа (III) методом градуировочного графика
- •Фототурбидиметрия.
- •Ход работы:
- •Приготовление стандартных растворов и раствора сравнения:
- •Построение градуировочного графика:
- •Контрольная задача. Определение содержания в растворе.
- •Вопросы для самоконтроля
- •Рефрактометрия
- •Цель и задачи работы
- •Программа работы
- •Рефрактометрическое определение сахара в молоке.
- •Приборы и реактивы:
- •Ход работы:
- •Подготовка пробы к анализу:
- •Порядок работы на рефрактометре:
- •Контрольная задача Определение содержания сахара в анализируемом образце:
- •Определение содержания хлорида натрия в водном растворе. Приборы и реактивы.
- •Ход работы:
- •Приготовление стандартных растворов:
- •Построение градуировочного графика.
- •Контрольная задача. Определение содержания хлорида натрия в анализируемом растворе
- •Вопросы для самоподготовки
- •Потенциометрия
- •Цель и задачи работы
- •Программа работы
- •Определение хлородородной и уксусной кислот в растворе при их совместном присутствии методом потенциометрического титрования.
- •Приборы и реактивы
- •Ход работы
- •Установление титра рабочего раствора
- •Подготовка анализируемого образца к титрованию
- •Подготовка иономера к работе в режиме определения рН
- •Контрольная задача. Определение содержания хлороводородной и уксусной кислот в анализируемом образце
- •Вопросы для самоподготовки.
- •Кондуктометрия.
- •Цель и задачи работы.
- •Программа работы.
- •Определение слабой кислоты и соли слабого основания в их смеси.
- •Приборы и реактивы:
- •Ход работы:
- •12.2.1.1. Установление титра рабочего раствора :
- •12.2.1.2. Подготовка анализируемого образца к титрованию:
- •12.2.1.3. Контрольная задача. Определение содержания борной кислоты и солянокислого гидроксиламина в испытуемой смеси:
- •Определение ионовив их смеси.
- •Приборы и реактивы:
- •Подготовка анализируемого образца к титрованию:проводят по пункту 12.2.1.2.
- •Контрольная задача. Определение содержания солей никеля (II) и кальция в испытуемой смеси
- •Вопросы для самоконтроля.
- •13. Газохроматографический метод определения содержания токсичных микропримесей
- •13.1. Цель работы:
- •13.2. Объекты и средства исследования.
- •13.3. Программа работы
- •13.3.1. Приготовление градуировочных смесей
- •Условия хроматографирования с капиллярными колонками:
- •Литература:
Перманганатометрия.
Цель и задачи работы.
Закрепление знаний теории окислительно-восстановительных равновесий и титриметрического анализа с применением окислительно-восстановительных реакций. Получение навыков титрования и проведения расчетов результатов анализа и их обработка. Освоение способов прямого, заместительного титрования и титрования по остатку. Контрольная задача — определение восстановителей в растворах неизвестной концентрации.
Программа работы
Определение железа (II).
Оборудование и реактивы:
Бюретка вместимостью 25 см3;
Мерные колбы вместимостью 100, 250 и 500 см3 ;
Колбы для титрования вместимостью 250 см3 ;
Пипетки Мора на 5, 10, 15, 25 см3;
Аналитические весы с разновесами;
Набор ареометров;
Щавелевая кислота
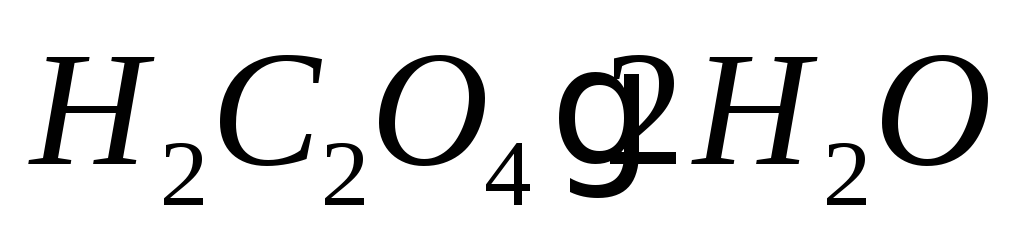 ,
х.ч. или ч.д.а.;
,
х.ч. или ч.д.а.;Перманганат калия
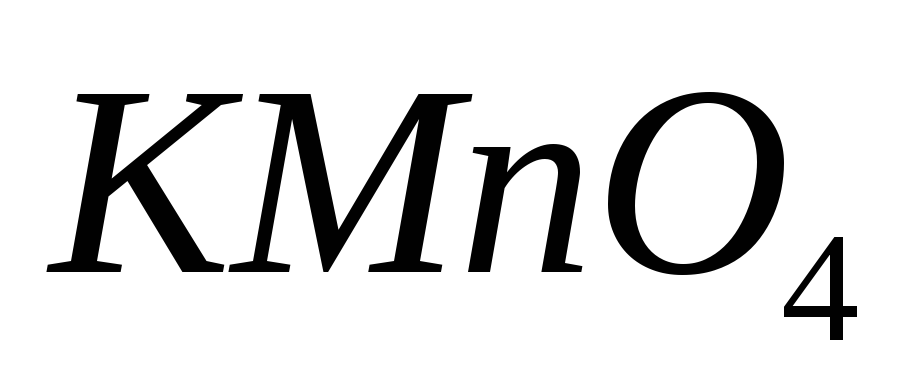 ,
х.ч. или ч.д.а.;
,
х.ч. или ч.д.а.;Серная кислота, раствор
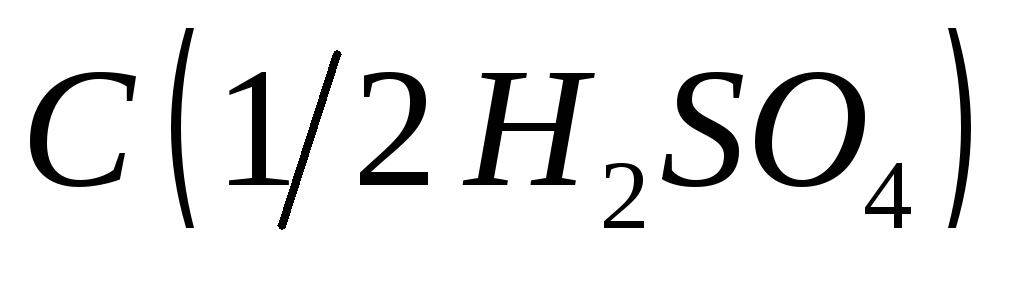 = 2 моль/дм3;
= 2 моль/дм3;Фосфорная кислота, раствор
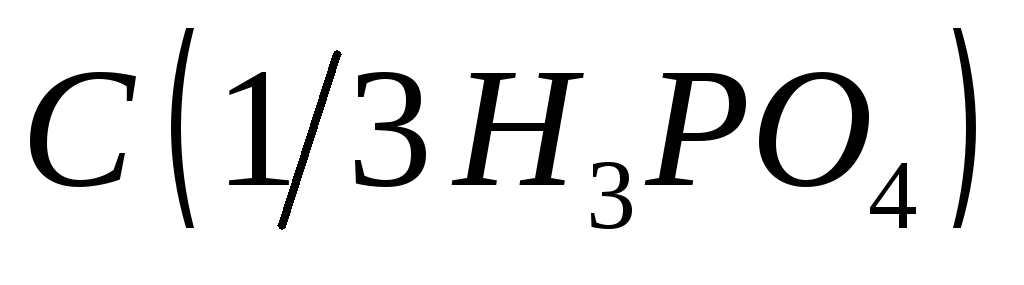 = 6 моль/дм3;
= 6 моль/дм3;Соль Мора, раствор
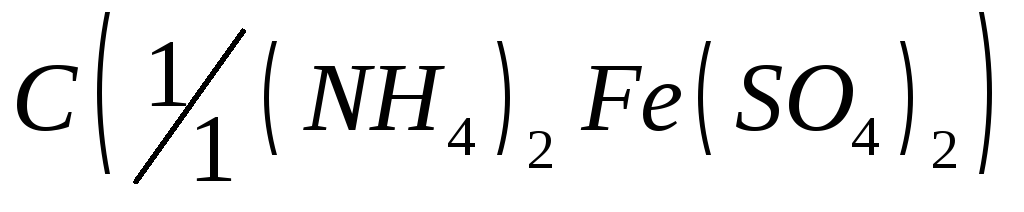 = 0,5 моль/дм3;
= 0,5 моль/дм3;Хлороводородная кислота, раствор
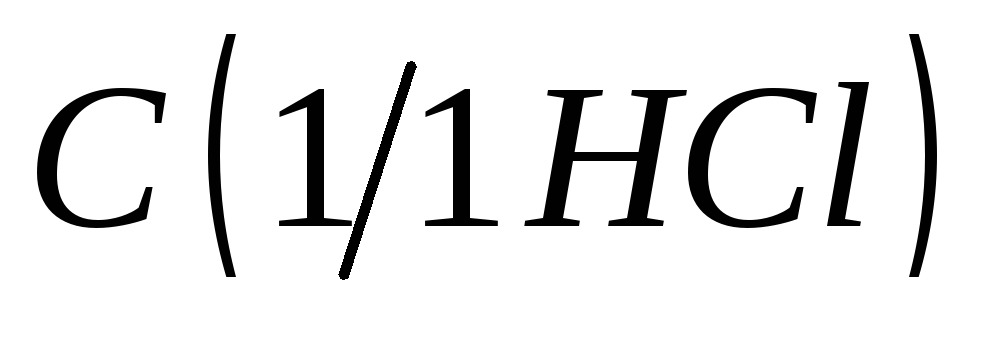 = 1
= 1
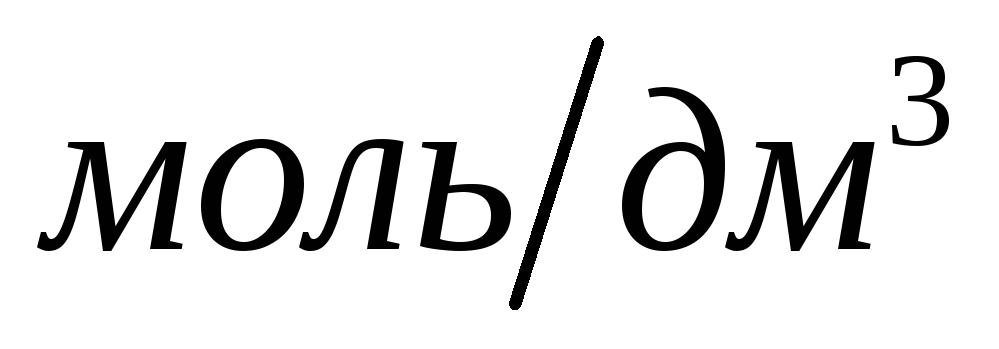 ;
;Оксалат аммония, раствор
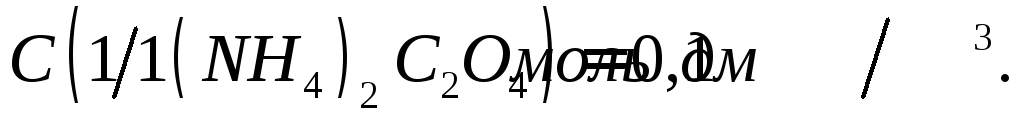 ;
;Индикатор метиловый оранжевый, раствор
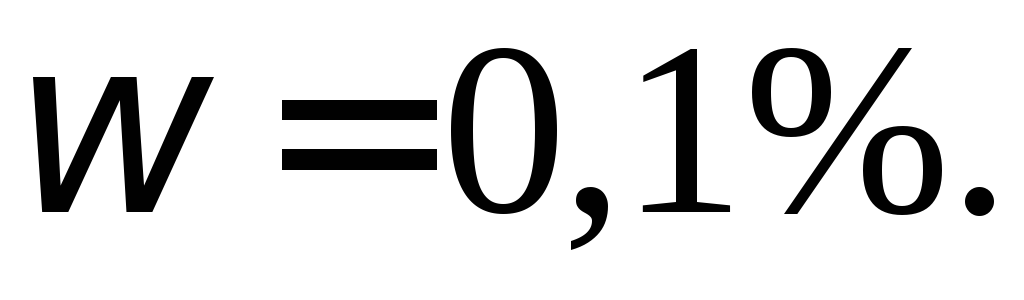 ;
;Нитрат серебра, водный раствор, = 1%;
Азотная кислота,
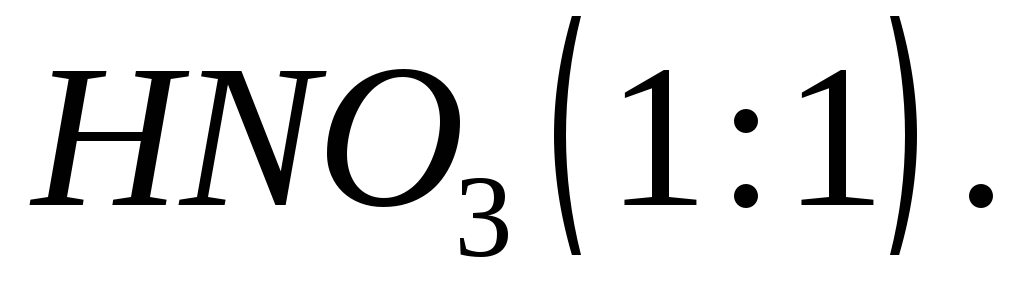 ;
;Хлорид кальция, раствор
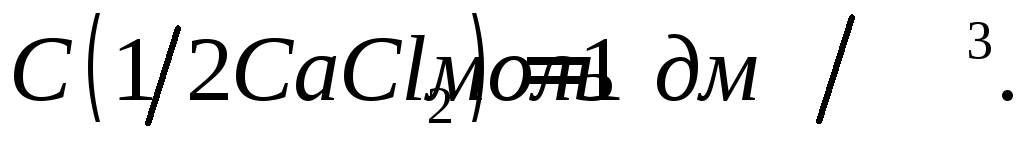
Приготовление первичного стандарта щавелевой кислоты
Выполняют по п.4.2.1.1.
из реактива
![]() квалификации х.ч. учитывая, что
квалификации х.ч. учитывая, что![]() .
Раствор следует готовить примерно такой
же концентрации, как раствор
.
Раствор следует готовить примерно такой
же концентрации, как раствор![]() .
.
Приготовление и стандартизация рабочего раствора перманганата калия (вторичного стандарта)
 =0,1 моль/дм3
=0,1 моль/дм3
Применяемый для приготовления растворов титранта твердый перманганат калия всегда в какой-то степени загрязнён диоксидом марганца, катализирующим процесс разложения перманганата в растворе. Удаление диоксида марганца фильтрованием заметно повышает устойчивость растворов перманганата. Фильтрование следует проводить спустя некоторое время после приготовления раствора, чтобы произошло полное окисление примесей в воде, для ускорения реакции окисления раствор можно прокипятить. Для фильтрования нельзя применять бумажный фильтр, так как целлюлоза реагирует с перманганатом, образуя диоксид марганца.
Разложение
раствора
![]() ускоряется на свету, при нагревании,
под действием кислот, оснований, ионов
ускоряется на свету, при нагревании,
под действием кислот, оснований, ионов
![]() и диоксида марганца:
и диоксида марганца:
![]()
![]()
Стандартные
растворы
![]() хранят в темном месте в темных склянках
со стеклянными пробками.
хранят в темном месте в темных склянках
со стеклянными пробками.
Для
установки характеристик раствора
перманганата обычно используют
свежеперекристаллизованную щавелевую
кислоту
![]() ,
оксалат натрия
,
оксалат натрия![]() или оксалат аммония
или оксалат аммония![]() .
Реакцию между перманганат- и оксалат-ионами
в кислой среде можно записать:
.
Реакцию между перманганат- и оксалат-ионами
в кислой среде можно записать:
![]()
Ход работы:
Рассчитывают навеску, учитывая, что
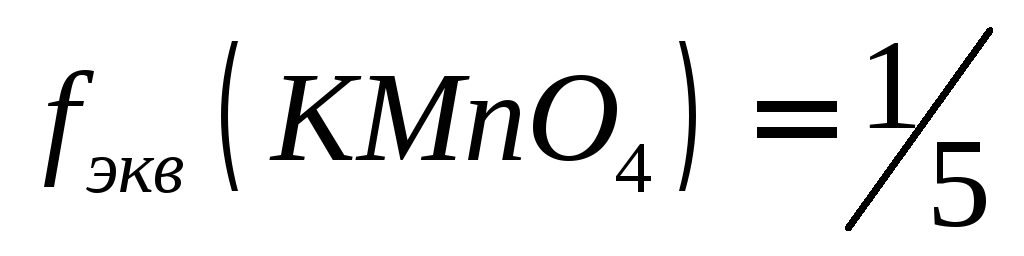 (кислая среда);
(кислая среда);На технических весах в стеклянном бюксе взвешивают рассчитанную навеску исходного перманганата.
Количественно переносят навеску дистиллированной водой в мерную колбу, растворяют при перемешивании и доводят раствор до метки дистиллированной водой.
Свежеприготовленный раствор
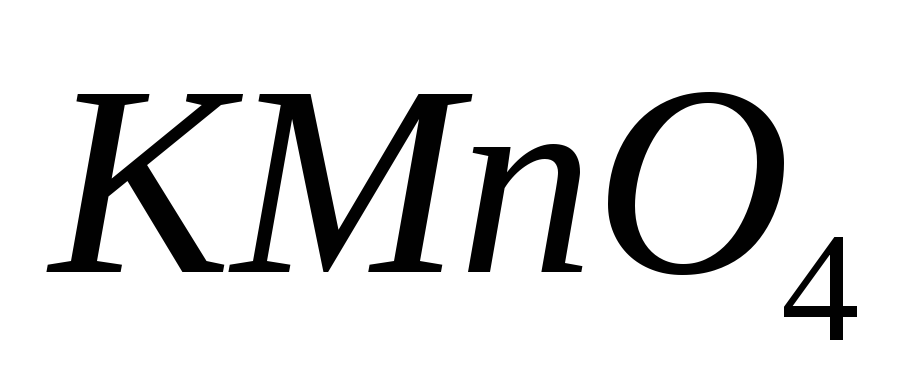 переносят в стакан, нагревают до кипения
и поддерживают эту температуру
приблизительно 1 ч. Затем раствор
охлаждают и фильтруют через стеклянный,
пористый фильтр. Можно перед фильтрованием
оставить раствор при комнатной
температуре на несколько дней.
переносят в стакан, нагревают до кипения
и поддерживают эту температуру
приблизительно 1 ч. Затем раствор
охлаждают и фильтруют через стеклянный,
пористый фильтр. Можно перед фильтрованием
оставить раствор при комнатной
температуре на несколько дней.Аликвотную часть раствора щавелевой кислоты 10 см3 переносят пипеткой в коническую колбу для титрования, добавляют 10 см3раствора
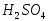 и нагревают на водяной бане примерно
до 75-800С. В начале титрования
следует приливать из бюретки раствор
и нагревают на водяной бане примерно
до 75-800С. В начале титрования
следует приливать из бюретки раствор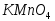 к горячему раствору оксалата по каплям.
Каждую следующую каплю прибавляют
после того, как исчезнет окраска от
предыдущей. Титрование заканчивают,
когда избыточная капля раствора
к горячему раствору оксалата по каплям.
Каждую следующую каплю прибавляют
после того, как исчезнет окраска от
предыдущей. Титрование заканчивают,
когда избыточная капля раствора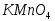 окрасит раствор в бледно-розовый цвет,
не исчезающий 1 мин.
окрасит раствор в бледно-розовый цвет,
не исчезающий 1 мин.Проводят 3-5 титрований. Результаты заносят в таблицу 4.1:
Результаты стандартизации раствора перманганата калия.
Таблица 4.1
|
№ п/п |
V(Н2С2О 4), см3 |
С(!/2Н2С2О4 ), моль/дм3 |
V(KMnO4), см3 |
С(1/5KMnO4), моль/дм3 |
Т(KMnO4), г/см3 |
|
|
|
|
|
|
|
Используя средний объем титранта,
затраченного на титрование, рассчитывают
характеристики раствора
![]() .
При расчете учитывают, что в точке
эквивалентности число молей эквивалента
титруемого вещества и титранта равны:
.
При расчете учитывают, что в точке
эквивалентности число молей эквивалента
титруемого вещества и титранта равны:![]()
