
- •Сборник методических указаний к лабораторным работам
- •«Аналитическая химия и физико-химические методы анализа»
- •Содержание
- •Часть I. Химические методы анализа
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов (в присутствии вольфрама)
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Выполнение реакций обнаружения анионов
- •Обнаружение карбонатов.
- •Обнаружение нитратов
- •Обнаружение ортофосфатов
- •Обнаружение силикатов
- •Обнаружение сульфидов
- •Обнаружение сульфатов
- •Обнаружение хлоридов
- •Вопросы для самоподготовки
- •Гравиметрия (весовой анализ)
- •Цель и задачи работы
- •Программа работы Приборы и реактивы.
- •Определение сульфатов
- •Ход работы.
- •Определение железа
- •Ход работы.
- •Определение никеля
- •Ход работы.
- •Вопросы для самоподготовки
- •Протолитометрический анализ
- •Ход работы
- •Контрольная задача. Определение уксусной кислоты.
- •Вопросы для самоподготовки.
- •Перманганатометрия.
- •Приготовление первичного стандарта щавелевой кислоты
- •Ход работы:
- •Контрольная задача. Определение железа (II)
- •Ход работы:
- •Вопросы для самоподготовки.
- •Иодометрия
- •Стандартизация рабочего раствора тиосульфата натрия (вторичного стандарта).
- •Ход работы:
- •Контрольная задача: Определение меди (II).
- •Ход определения:
- •Вопросы для самоподготовки.
- •Комплексонометрия.
- •Цель и задачи работы.
- •Оборудование и реактивы:
- •Программа работы
- •Определение кальция
- •Ход работы:
- •Определение железа
- •Ход работы
- •Вопросы для самоподготовки
- •Часть II. Инструментальные методы анализа
- •Определение калия по методу градуировочного графика
- •Ход работы:
- •Приготовление стандартных растворов:
- •Подготовка прибора к работе:
- •Построение градуировочного графика
- •Контрольная задача. Определение содержания калия в анализируемом растворе
- •Фотометрический анализ
- •Выбор светофильтра
- •Построение градуировочного графика
- •Контрольная задача. Определение содержания меди (II) в анализируемом растворе
- •Определение железа (III) методом градуировочного графика
- •Фототурбидиметрия.
- •Ход работы:
- •Приготовление стандартных растворов и раствора сравнения:
- •Построение градуировочного графика:
- •Контрольная задача. Определение содержания в растворе.
- •Вопросы для самоконтроля
- •Рефрактометрия
- •Цель и задачи работы
- •Программа работы
- •Рефрактометрическое определение сахара в молоке.
- •Приборы и реактивы:
- •Ход работы:
- •Подготовка пробы к анализу:
- •Порядок работы на рефрактометре:
- •Контрольная задача Определение содержания сахара в анализируемом образце:
- •Определение содержания хлорида натрия в водном растворе. Приборы и реактивы.
- •Ход работы:
- •Приготовление стандартных растворов:
- •Построение градуировочного графика.
- •Контрольная задача. Определение содержания хлорида натрия в анализируемом растворе
- •Вопросы для самоподготовки
- •Потенциометрия
- •Цель и задачи работы
- •Программа работы
- •Определение хлородородной и уксусной кислот в растворе при их совместном присутствии методом потенциометрического титрования.
- •Приборы и реактивы
- •Ход работы
- •Установление титра рабочего раствора
- •Подготовка анализируемого образца к титрованию
- •Подготовка иономера к работе в режиме определения рН
- •Контрольная задача. Определение содержания хлороводородной и уксусной кислот в анализируемом образце
- •Вопросы для самоподготовки.
- •Кондуктометрия.
- •Цель и задачи работы.
- •Программа работы.
- •Определение слабой кислоты и соли слабого основания в их смеси.
- •Приборы и реактивы:
- •Ход работы:
- •12.2.1.1. Установление титра рабочего раствора :
- •12.2.1.2. Подготовка анализируемого образца к титрованию:
- •12.2.1.3. Контрольная задача. Определение содержания борной кислоты и солянокислого гидроксиламина в испытуемой смеси:
- •Определение ионовив их смеси.
- •Приборы и реактивы:
- •Подготовка анализируемого образца к титрованию:проводят по пункту 12.2.1.2.
- •Контрольная задача. Определение содержания солей никеля (II) и кальция в испытуемой смеси
- •Вопросы для самоконтроля.
- •13. Газохроматографический метод определения содержания токсичных микропримесей
- •13.1. Цель работы:
- •13.2. Объекты и средства исследования.
- •13.3. Программа работы
- •13.3.1. Приготовление градуировочных смесей
- •Условия хроматографирования с капиллярными колонками:
- •Литература:
Протолитометрический анализ
Цель и задачи работы
Закрепление знаний
теории протолитических равновесий и
титриметрического анализа с применением
кислотно-основных реакций. Получение
навыков титрования с применением
![]() – индикоторов, проведения расчетов
результатов анализа и их обработка.
Контрольная задача – определение
протолитов и в растворах протолитов и
их смесей неизвестной концентрации.
– индикоторов, проведения расчетов
результатов анализа и их обработка.
Контрольная задача – определение
протолитов и в растворах протолитов и
их смесей неизвестной концентрации.
Программа работы
Определение уксусной кислоты
Оборудование и реактивы:
Бюретка вместимостью 25 см3;
Мерные колбы вместимостью 100, 250 и 500 см3 ;
Колбы для титрования вместимостью 250 см3 ;
Пипетки Мора на 5, 10, 15, 25 см3;
Аналитические весы с разновесами;
Набор ареометров;
Тетраборат натрия
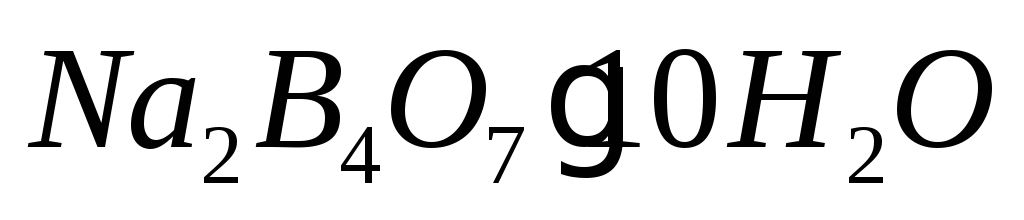 ,
х.ч. или ч.д.а.;
,
х.ч. или ч.д.а.;Щавелевая кислота
 ,
х.ч. или ч.д.а.;
,
х.ч. или ч.д.а.;Хлороводородная кислота концентрированная, х.ч. или ч.д.а.;
Гидроксид натрия кристаллический, х.ч. или ч.д.а.;
Уксусная кислота, раствор
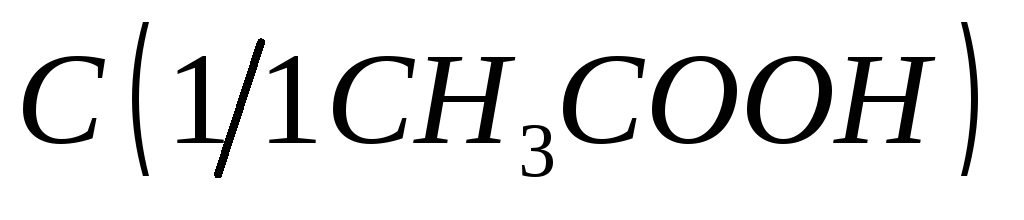 = 1 моль/дм3;
= 1 моль/дм3;Карбонат натрия, водный раствор,
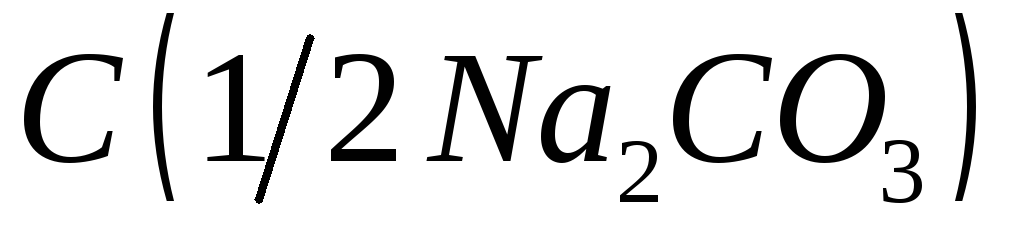 = 2 моль/дм3;
= 2 моль/дм3;Гидрокарбонат натрия, водный раствор,
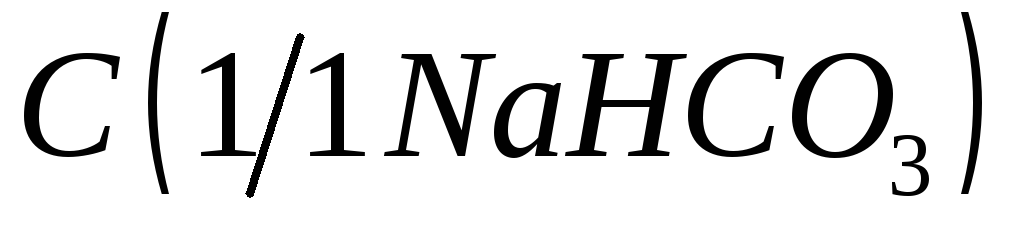 = 1 моль/дм3;
= 1 моль/дм3;Гидроксид натрия, водный раствор,
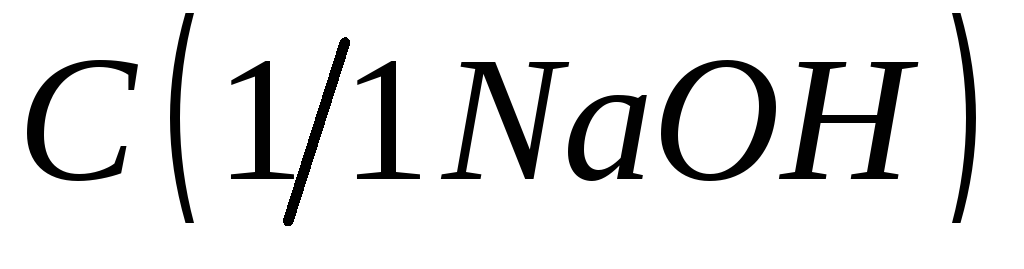 = 1 моль/дм3;
= 1 моль/дм3;Метиловый красный, водно-этанольный раствор, = 0,1%;
Метиловый оранжевый, водный раствор,= 0,1%;
Фенолфталеин, этанольный раствор, = 0,1%.
Ход работы
Приготовление первичного стандарта тетрабората натрия C(1/2 Na2B4O7) = 0,1 моль/дм3
Раствор готовят по точной навеске
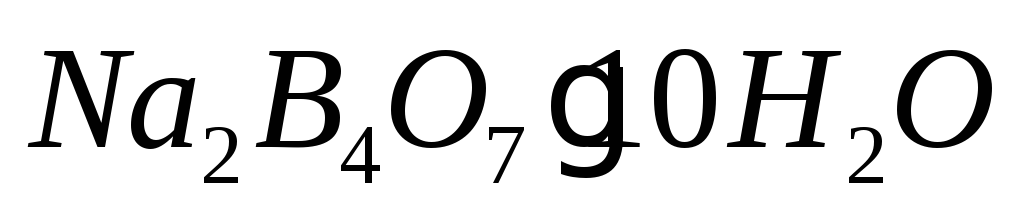 .
Массу навески необходимой для
приготовления заданного объема
.
Массу навески необходимой для
приготовления заданного объема раствора с заданной концентрацией
раствора с заданной концентрацией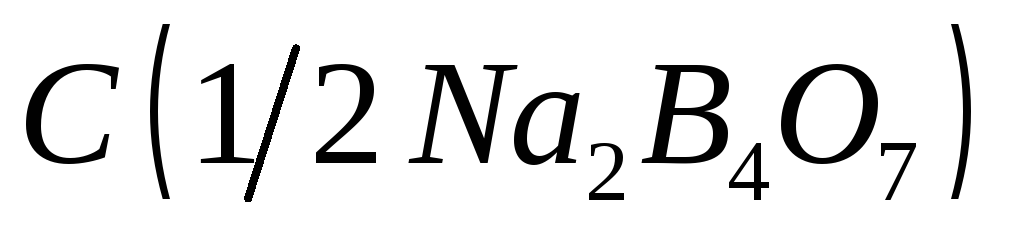 рассчитывают по формуле:
рассчитывают по формуле:
![]()
Навеску берут в бюксе или стаканчике для взвешивания на аналитических весах.
Навеску тетрабората натрия количественно переносят водой в мерную колбу заданного объема, приливают горячую дистиллированную воду примерно до половины и растворяют тетраборат натрия перемешиванием. Дают раствору остыть до комнатной температуры, доводят колбу до метки дистиллированной водой. закрывают пробкой и вновь перемешивают.
По точной массе навески и объему мерной колбы рассчитывают точную концентрацию и титр раствора тетрабората натрия:
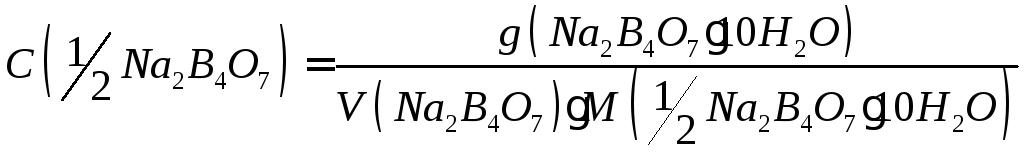
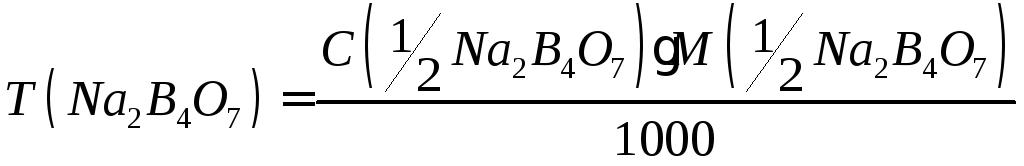
Рассчитывают ошибку титрования.
Приготовление стандартного раствора хлороводородной кислоты C(1/1 HCl) = 0,1 моль/дм3
С помощью ареометра определяют плотность концентрированной кислоты и по справочнику находят процентную концентрацию хлороводородной кислоты.
Рассчитывают объем концентрированной кислоты, необходимый для приготовления заданного объема раствора
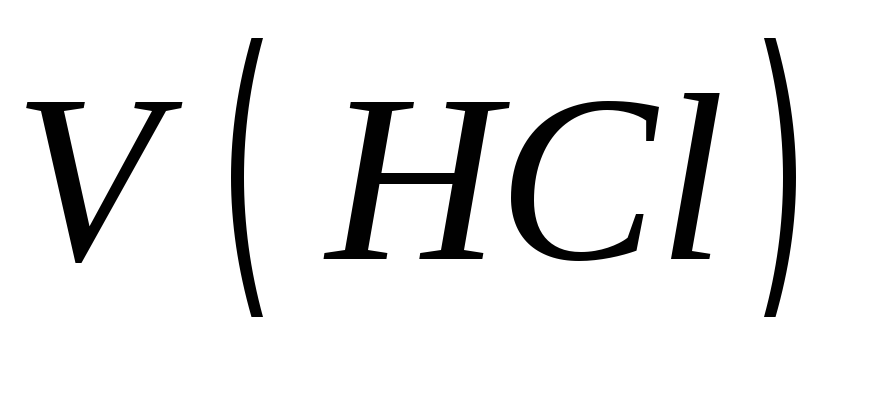 с заданной концентрацией
с заданной концентрацией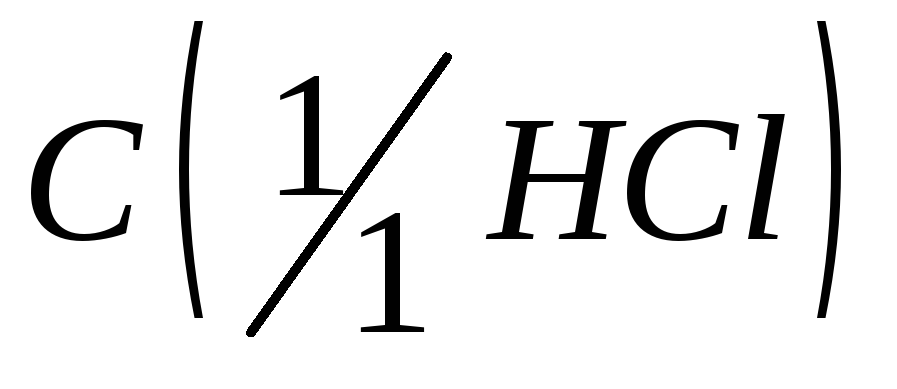 ,
по формуле:
,
по формуле:
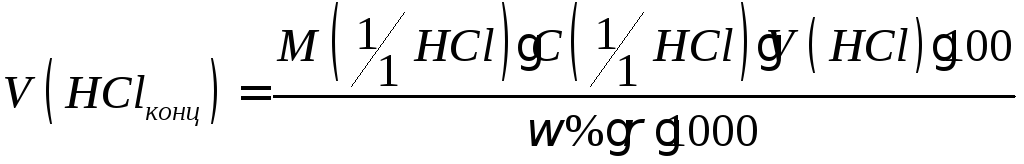
Рассчитанный объем концентрированной кислоты отмеряют мерным цилиндром и переносят (под тягой) в мерную колбу. Доводят до метки дистиллированной водой.
Стандартизацию полученного раствора хлороводородной кислоты проводят по раствору первичного стандарта тетрабората натрия (приготовленного по пункту 3.2.1.1). Для этого аликвотную часть раствора тетрабората натрия титруют приготовленным раствором хлороводородной кислоты в присутствии индикатора метилового красного (
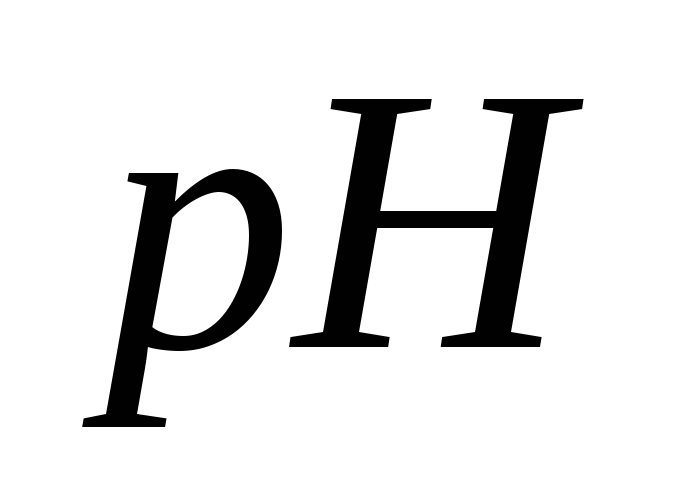 в точке эквивалентности для 0,1 М
раствора составляет 5,12;
в точке эквивалентности для 0,1 М
раствора составляет 5,12;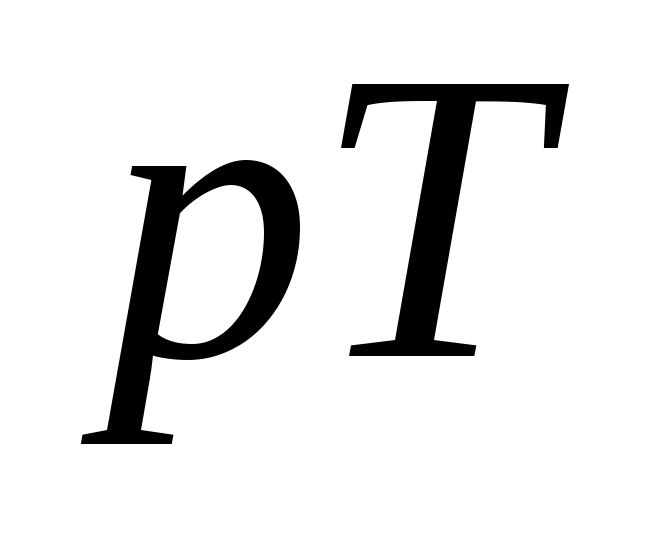 для метилового красного 5,5) до перехода
окраски раствора то желтого до
оранжево-желтого.
для метилового красного 5,5) до перехода
окраски раствора то желтого до
оранжево-желтого.
Проводят не менее 3 определений. Результаты заносят в таблицу 3.1:
Результаты стандартизации раствора хлороводородной кислоты.
Таблица 3.1.
|
№ п/п |
V(Na2B4O7), см3 |
C(1/2 Na2B4O7), моль/дм3 |
V(HCl), см3 |
С(1/1HCl), моль/дм3 |
Т(HCl), г/см3 |
|
|
|
|
|
|
|
Расчет характеристик стандартного раствора хлороводородной кислоты проводят по среднему значению объема раствора кислоты, пошедшего на титрования ( из 3-5 параллельных проб)
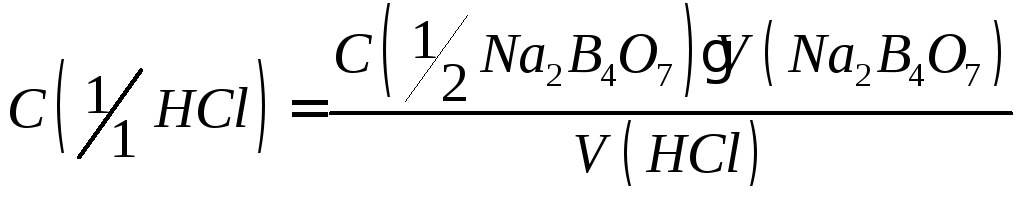
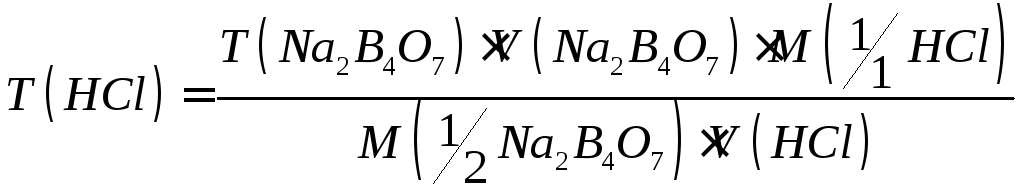
Рассчитывают ошибку титрования.
Приготовление стандартного раствора гидроксида натрия C(1/1NaOH) = 0,1 моль/дм3
Рассчитывают массу навески необходимой для приготовления заданного объема
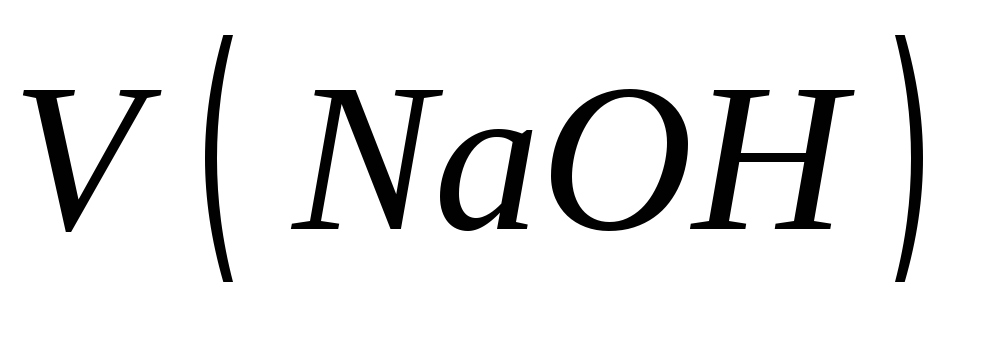 раствора с заданной концентрацией
раствора с заданной концентрацией рассчитывают по формуле:
рассчитывают по формуле:
![]()
Навеску берут в бюксе для взвешивания на аналитических весах.
Навеску гидроксида натрия количественно переносят водой в мерную колбу заданного объема, приливают дистиллированную воду примерно до половины и растворяют гидроксида натрия перемешиванием. Дают раствору остыть до комнатной температуры, доводят колбу до метки дистиллированной водой, закрывают пробкой и вновь перемешивают.
Стандартизацию полученного раствора гидроксида натрия проводят по раствору стандарта хлороводородной кислоты (приготовленного по пункту 3.2.1.2). Для этого аликвотную часть раствора хлороводородной кислоты титруют приготовленным гидроксида натрия в присутствии индикатора фенолфталеина(
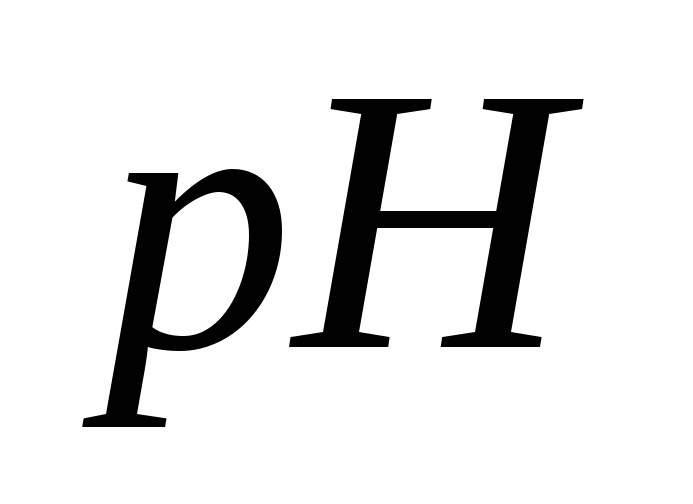 в точке эквивалентности составляет 7;
в точке эквивалентности составляет 7; для фенолфталеина 9,0) до окрашивания
раствора в бледно-розовый цвет.
для фенолфталеина 9,0) до окрашивания
раствора в бледно-розовый цвет.Расчет характеристик стандартного раствора гидроксида натрия проводят по среднему значению объема раствора гидроксида натрия, пошедшего на титрования ( из 3-5 параллельных проб). Результаты заносят в таблицу 3.2:
Результаты стандартизации раствора гидроксида натрия.
Таблица 3.2
|
№ п/п |
V(HCl), cм3 |
С(1/1HCl), моль/дм3 |
V(NaOH), см3 |
C(1/1NaOH), моль/дм3 |
T(NaOH), г/см3 |
|
|
|
|
|
|
|
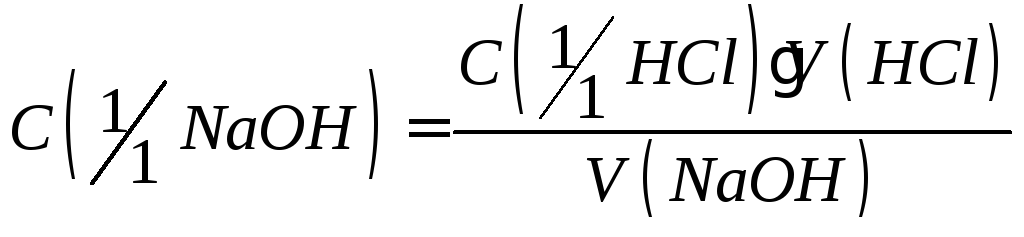
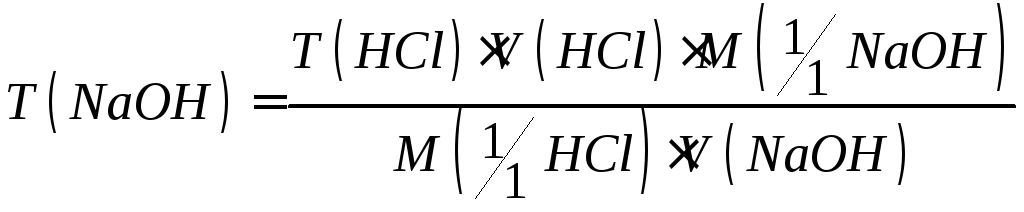
Стандартизацию раствора щелочи производят ежедневно.
Рассчитывают ошибку титрования.
