
- •Сборник методических указаний к лабораторным работам
- •«Аналитическая химия и физико-химические методы анализа»
- •Содержание
- •Часть I. Химические методы анализа
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов (в присутствии вольфрама)
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Выполнение реакций обнаружения анионов
- •Обнаружение карбонатов.
- •Обнаружение нитратов
- •Обнаружение ортофосфатов
- •Обнаружение силикатов
- •Обнаружение сульфидов
- •Обнаружение сульфатов
- •Обнаружение хлоридов
- •Вопросы для самоподготовки
- •Гравиметрия (весовой анализ)
- •Цель и задачи работы
- •Программа работы Приборы и реактивы.
- •Определение сульфатов
- •Ход работы.
- •Определение железа
- •Ход работы.
- •Определение никеля
- •Ход работы.
- •Вопросы для самоподготовки
- •Протолитометрический анализ
- •Ход работы
- •Контрольная задача. Определение уксусной кислоты.
- •Вопросы для самоподготовки.
- •Перманганатометрия.
- •Приготовление первичного стандарта щавелевой кислоты
- •Ход работы:
- •Контрольная задача. Определение железа (II)
- •Ход работы:
- •Вопросы для самоподготовки.
- •Иодометрия
- •Стандартизация рабочего раствора тиосульфата натрия (вторичного стандарта).
- •Ход работы:
- •Контрольная задача: Определение меди (II).
- •Ход определения:
- •Вопросы для самоподготовки.
- •Комплексонометрия.
- •Цель и задачи работы.
- •Оборудование и реактивы:
- •Программа работы
- •Определение кальция
- •Ход работы:
- •Определение железа
- •Ход работы
- •Вопросы для самоподготовки
- •Часть II. Инструментальные методы анализа
- •Определение калия по методу градуировочного графика
- •Ход работы:
- •Приготовление стандартных растворов:
- •Подготовка прибора к работе:
- •Построение градуировочного графика
- •Контрольная задача. Определение содержания калия в анализируемом растворе
- •Фотометрический анализ
- •Выбор светофильтра
- •Построение градуировочного графика
- •Контрольная задача. Определение содержания меди (II) в анализируемом растворе
- •Определение железа (III) методом градуировочного графика
- •Фототурбидиметрия.
- •Ход работы:
- •Приготовление стандартных растворов и раствора сравнения:
- •Построение градуировочного графика:
- •Контрольная задача. Определение содержания в растворе.
- •Вопросы для самоконтроля
- •Рефрактометрия
- •Цель и задачи работы
- •Программа работы
- •Рефрактометрическое определение сахара в молоке.
- •Приборы и реактивы:
- •Ход работы:
- •Подготовка пробы к анализу:
- •Порядок работы на рефрактометре:
- •Контрольная задача Определение содержания сахара в анализируемом образце:
- •Определение содержания хлорида натрия в водном растворе. Приборы и реактивы.
- •Ход работы:
- •Приготовление стандартных растворов:
- •Построение градуировочного графика.
- •Контрольная задача. Определение содержания хлорида натрия в анализируемом растворе
- •Вопросы для самоподготовки
- •Потенциометрия
- •Цель и задачи работы
- •Программа работы
- •Определение хлородородной и уксусной кислот в растворе при их совместном присутствии методом потенциометрического титрования.
- •Приборы и реактивы
- •Ход работы
- •Установление титра рабочего раствора
- •Подготовка анализируемого образца к титрованию
- •Подготовка иономера к работе в режиме определения рН
- •Контрольная задача. Определение содержания хлороводородной и уксусной кислот в анализируемом образце
- •Вопросы для самоподготовки.
- •Кондуктометрия.
- •Цель и задачи работы.
- •Программа работы.
- •Определение слабой кислоты и соли слабого основания в их смеси.
- •Приборы и реактивы:
- •Ход работы:
- •12.2.1.1. Установление титра рабочего раствора :
- •12.2.1.2. Подготовка анализируемого образца к титрованию:
- •12.2.1.3. Контрольная задача. Определение содержания борной кислоты и солянокислого гидроксиламина в испытуемой смеси:
- •Определение ионовив их смеси.
- •Приборы и реактивы:
- •Подготовка анализируемого образца к титрованию:проводят по пункту 12.2.1.2.
- •Контрольная задача. Определение содержания солей никеля (II) и кальция в испытуемой смеси
- •Вопросы для самоконтроля.
- •13. Газохроматографический метод определения содержания токсичных микропримесей
- •13.1. Цель работы:
- •13.2. Объекты и средства исследования.
- •13.3. Программа работы
- •13.3.1. Приготовление градуировочных смесей
- •Условия хроматографирования с капиллярными колонками:
- •Литература:
Контрольная задача. Определение уксусной кислоты.
Аликвотную часть раствора уксусной кислоты неизвестной концентрации титруют стандартным раствором гидроксида натрия в присутствии индикатора фенолфталеина (
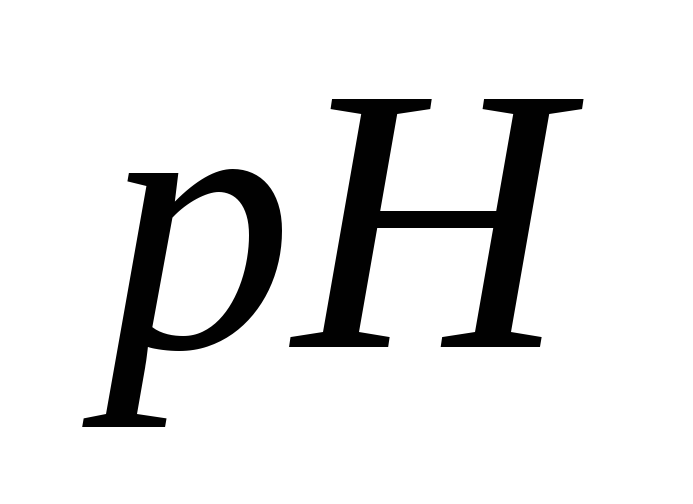 в точке эквивалентности для 0,1 раствора составляет 8,9;
в точке эквивалентности для 0,1 раствора составляет 8,9;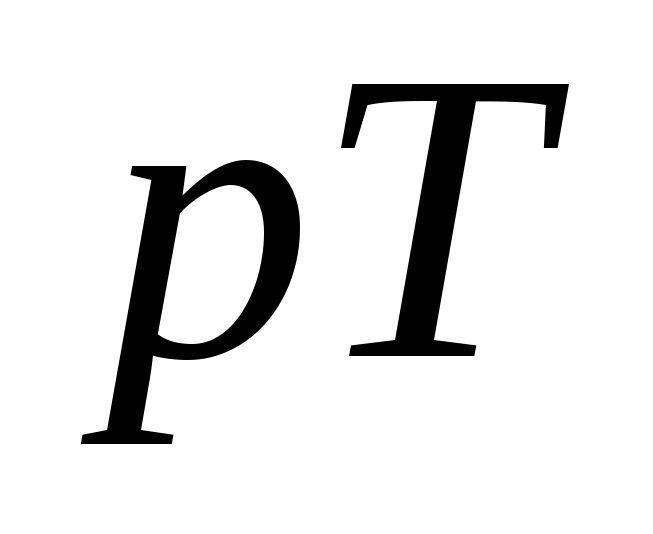 для фенолфталеина 9,0) до окрашивания
раствора в бледно-розовый цвет.
для фенолфталеина 9,0) до окрашивания
раствора в бледно-розовый цвет.Титрование повторяют 3-5 раз. Результаты заносят в таблицу 3.3:
Результаты титрования уксусной кислоты.
Таблица 3.3.
|
№ п/п |
V(NaOH) cм3 |
C(1/1NaOH), моль/дм3 |
V(CH3COOH),см3 |
C(1/1CH3COOH), моль/дм3 |
Т(CH3COOH), г/см3 |
|
|
|
|
|
|
|
Неизвестную концентрацию кислоты рассчитывают по среднему значению объема раствора гидроксида натрия, пошедшего на титрования ( из 3-5 параллельных проб):
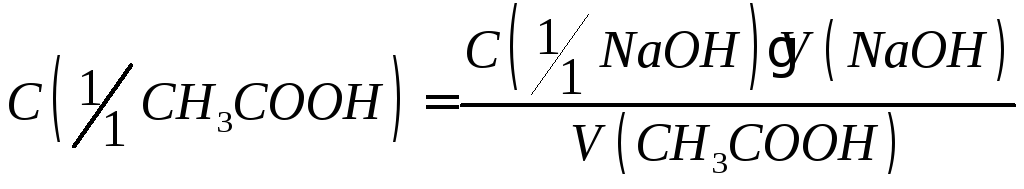
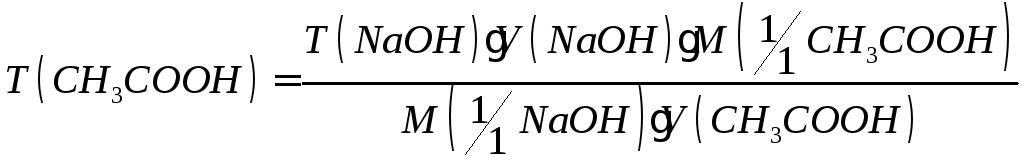
Рассчитывают ошибку титрования.
Вопросы для самоподготовки.
Какова роль кривых титрования?
В каких координатах строят кривые в разных методах титрования?
Обязательно ли совпадение точки эквивалентности и конечной точки титрования?
Назовите факторы, влияющие на вид кривой титрования (величина скачка, положение точки эквивалентности, наклон ветвей).
Можно ли оттитровать в водном растворе прямым способом борную кислоту. Соли аммония, ацетат-ион?
Сколько скачков на кривых титрования щавелевой, серной, этилендиаминтетрауксусной, угольной и фосфорной кислот гидроксидом натрия; карбоната натрия, фосфата натрия и гидрозина соляной кислоты?
Почему скачок титрования борной кислоты увеличивается в присутствии глицерина?
Укажите на кривых титрования области буферного действия, а также точку с максимальной буферной ёмкостью.
Как оттитровать угольную кислоту по второй ступени, фосфорную кислоту по третьей ступени?
Какие приёмы используют для титрования кислот и оснований с константами менее
 ?
?Какие приёмы используют для титрования смеси электролитов с близкими константами?
Рассчитайте эквивалентную массу карбоната натрия, бикарбоната натрия, тетрабората натрия, карбоната кальция, оксалата натрия, иодата калия, оксида ртути, щавелевой кислоты, янтарной кислоты, бензойной кислоты, бифталата калия, бииодата калия.
Назовите вторичные стандартные растворы, применяемые в методе кислотно-основного титрования.
Почему раствор щёлочи не должен содержать карбонат-ион? Перечислите несколько способов приготовления раствора щёлочи, не содержащего карбонат-ион.
Как меняется вид кривой (величина скачка, положение точки эквивалентности) при изменении: а) концентрации растворов; б) констант диссоциации кислот и оснований; в) температуры?
Каковы предельные значения концентрации кислот и оснований, а также константы диссоциации кислот и оснований, при которых наблюдается скачок титрования?
Можно ли прямым методом титровать борную кислоту, соли аммония, соли уксусной муравьиной, щавелевой кислот, угольную кислоту по второй ступени и фосфорную кислоту по третьей ступени?
При каком условии возможно реальное титрование смеси кислот (или многоосновных кислот по ступеням)? Можно ли оттитровать по ступеням щавелевую, серную кислоту?
Изложите сущность ионной, хромофорной и ионно-хромофорной теорий индикаторов.
