
- •Сборник методических указаний к лабораторным работам
- •«Аналитическая химия и физико-химические методы анализа»
- •Содержание
- •Часть I. Химические методы анализа
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов (в присутствии вольфрама)
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Обнаружение ионов
- •Выполнение реакций обнаружения анионов
- •Обнаружение карбонатов.
- •Обнаружение нитратов
- •Обнаружение ортофосфатов
- •Обнаружение силикатов
- •Обнаружение сульфидов
- •Обнаружение сульфатов
- •Обнаружение хлоридов
- •Вопросы для самоподготовки
- •Гравиметрия (весовой анализ)
- •Цель и задачи работы
- •Программа работы Приборы и реактивы.
- •Определение сульфатов
- •Ход работы.
- •Определение железа
- •Ход работы.
- •Определение никеля
- •Ход работы.
- •Вопросы для самоподготовки
- •Протолитометрический анализ
- •Ход работы
- •Контрольная задача. Определение уксусной кислоты.
- •Вопросы для самоподготовки.
- •Перманганатометрия.
- •Приготовление первичного стандарта щавелевой кислоты
- •Ход работы:
- •Контрольная задача. Определение железа (II)
- •Ход работы:
- •Вопросы для самоподготовки.
- •Иодометрия
- •Стандартизация рабочего раствора тиосульфата натрия (вторичного стандарта).
- •Ход работы:
- •Контрольная задача: Определение меди (II).
- •Ход определения:
- •Вопросы для самоподготовки.
- •Комплексонометрия.
- •Цель и задачи работы.
- •Оборудование и реактивы:
- •Программа работы
- •Определение кальция
- •Ход работы:
- •Определение железа
- •Ход работы
- •Вопросы для самоподготовки
- •Часть II. Инструментальные методы анализа
- •Определение калия по методу градуировочного графика
- •Ход работы:
- •Приготовление стандартных растворов:
- •Подготовка прибора к работе:
- •Построение градуировочного графика
- •Контрольная задача. Определение содержания калия в анализируемом растворе
- •Фотометрический анализ
- •Выбор светофильтра
- •Построение градуировочного графика
- •Контрольная задача. Определение содержания меди (II) в анализируемом растворе
- •Определение железа (III) методом градуировочного графика
- •Фототурбидиметрия.
- •Ход работы:
- •Приготовление стандартных растворов и раствора сравнения:
- •Построение градуировочного графика:
- •Контрольная задача. Определение содержания в растворе.
- •Вопросы для самоконтроля
- •Рефрактометрия
- •Цель и задачи работы
- •Программа работы
- •Рефрактометрическое определение сахара в молоке.
- •Приборы и реактивы:
- •Ход работы:
- •Подготовка пробы к анализу:
- •Порядок работы на рефрактометре:
- •Контрольная задача Определение содержания сахара в анализируемом образце:
- •Определение содержания хлорида натрия в водном растворе. Приборы и реактивы.
- •Ход работы:
- •Приготовление стандартных растворов:
- •Построение градуировочного графика.
- •Контрольная задача. Определение содержания хлорида натрия в анализируемом растворе
- •Вопросы для самоподготовки
- •Потенциометрия
- •Цель и задачи работы
- •Программа работы
- •Определение хлородородной и уксусной кислот в растворе при их совместном присутствии методом потенциометрического титрования.
- •Приборы и реактивы
- •Ход работы
- •Установление титра рабочего раствора
- •Подготовка анализируемого образца к титрованию
- •Подготовка иономера к работе в режиме определения рН
- •Контрольная задача. Определение содержания хлороводородной и уксусной кислот в анализируемом образце
- •Вопросы для самоподготовки.
- •Кондуктометрия.
- •Цель и задачи работы.
- •Программа работы.
- •Определение слабой кислоты и соли слабого основания в их смеси.
- •Приборы и реактивы:
- •Ход работы:
- •12.2.1.1. Установление титра рабочего раствора :
- •12.2.1.2. Подготовка анализируемого образца к титрованию:
- •12.2.1.3. Контрольная задача. Определение содержания борной кислоты и солянокислого гидроксиламина в испытуемой смеси:
- •Определение ионовив их смеси.
- •Приборы и реактивы:
- •Подготовка анализируемого образца к титрованию:проводят по пункту 12.2.1.2.
- •Контрольная задача. Определение содержания солей никеля (II) и кальция в испытуемой смеси
- •Вопросы для самоконтроля.
- •13. Газохроматографический метод определения содержания токсичных микропримесей
- •13.1. Цель работы:
- •13.2. Объекты и средства исследования.
- •13.3. Программа работы
- •13.3.1. Приготовление градуировочных смесей
- •Условия хроматографирования с капиллярными колонками:
- •Литература:
Часть I. Химические методы анализа
Капельный анализ неорганических веществ
Цель и задачи работы
Овладеть приемами выполнения качественных аналитических реакций капельным способом. Освоить методику дробного качественного анализа, обнаружения катионов и анионов в многокомпонентных средах с помощью специфических реакций. Произвести анализ объекта неизвестного состава.
Программа работы
Предварительная подготовка пробы
Анализ твердых объектов
Пробу измельчают в мельнице или растиранием в ступке. Берут навеску 0,1-0,5 г и растворяют в соответствующем, в зависимости от предполагаемого химического состава, растворителе (вода, растворы кислот и щелочей).
Анализ металлов и сплавов (безстружковый метод)
На очищенную поверхность образца помещают 2-3 капли азотной кислоты (1:1). После прекращения реакции, образовавшийся на поверхности металла раствор разбавляют дистиллированной водой (2-3 капли) и переносят с помощью капилляра или пипетки в микропробирку. Операцию повторяют 2-3 раза. Собранный раствор подвергают непосредственно анализу.
Анализ жидких сред
В зависимости от компонентного состава пробы, при необходимости, по специальным методикам проводят операции маскирования, осаждения и отделения органических соединений и отдельных ионов, мешающих анализу, или выделения открываемых ионов.
Выполнение реакций обнаружения катионов
Оборудование и реактивы.
Предметные стекла;
Микропробирки;
Пипетки;
Беззольные бумажные фильтры;
Универсальная индикаторная бумага;
Растворы индивидуальных катионов и анионов, 0,01 моль/дм3;
Обнаружение ионов
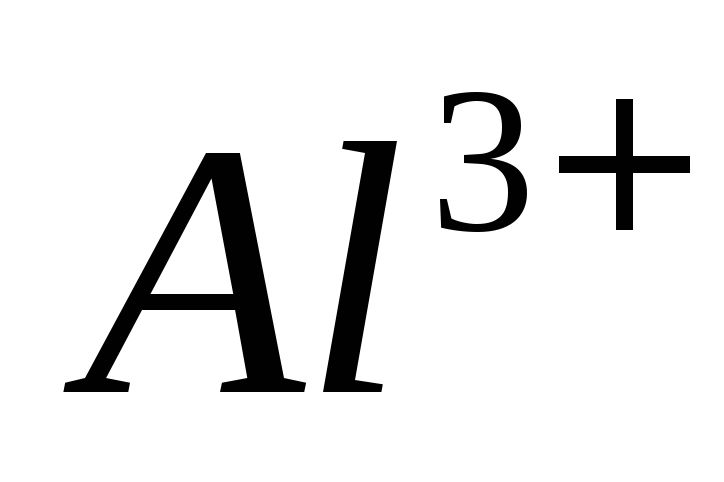
а) На ализариновую бумагу наносят каплю анализируемого раствора и выдерживают в парах аммиака до окрашивания пятна в фиолетовый цвет. При большом содержании алюминия красное окрашивание появляется сразу. Если содержание алюминия мало, то бумагу следует высушить в печи. Фиолетовая окраска ализарината алюминия исчезает, поскольку последний распадается на аммиак и желтый ализарин; при этом красный алюминиевый лак становится заметнее.
Предел обнаружения: 0,15 мкг.
Реагент: Ализариновая бумага. Беззольный фильтр погружают в насыщенный этанольный раствор ализарина, высушивают и хранят в закрытом сосуде.
Обнаружению алюминия мешают железо, уран, хром и марганец. Мешающее влияние этих элементов можно устранить осаждением гексацианоферратом (II) калия.
б)Анализируемый раствор подщелачивают до растворения первоначально выпавшего осадка. Каплю его переносят на фильтровальную бумагу и последовательно обрабатывают каплей раствора ализарина красного С и каплей уксусной кислоты. Образуется красно-фиолетовый алюминиевый лак.
Предел обнаружения: 0,67 мкг.
Реагент: Ализарин красный С (натриевая соль ализаринсульфокислоты), водный раствор = 0,1 % (масс).
Обнаружение ионов
а) На предметном стекле смешивают каплю анализируемого раствора с каплей серной кислоты и через 1 минуту добавляют каплю раствора перекиси водорода. В зависимости от содержания ванадия раствор приобретает от бледной коричнево-розовой до кроваво-красной окраски.
Предел обнаружения: 2,5 мкг.
Реагенты: серная кислота, водный раствор = 20% (масс), перекись водорода, водный раствор= 1% (масс).
Для устранения мешающего
влияния
![]() и
и![]() добавляют раствор
добавляют раствор![]() или
или![]() ,
связывающий эти катионы в комплексы
,
связывающий эти катионы в комплексы![]() и
и![]() соответственно.
соответственно.
б)На фильтровальную
бумагу наносят каплю анализируемого
раствора и реагента. В присутствии![]() проявляется чистое голубое окрашивание.
проявляется чистое голубое окрашивание.
Предел обнаружения: 0,05 мкг.
Реагент: Сульфосалициловая кислота, раствор в 80% (масс) фосфорной кислоте, = 2% (масс).
Обнаружению мешают
![]() .
.
в)В микропробирке
к анализируемому раствору добавляют
каплю реагента. В присутствии![]() раствор окрашивается в глубокий синий
цвет и флуоресцирует красным светом
при УФ облучении.
раствор окрашивается в глубокий синий
цвет и флуоресцирует красным светом
при УФ облучении.
Предел обнаружения: 1 мкг.
Реагент: Резорцин, раствор в 80% (масс) фосфорной кислоте, = 0,1% (масс).
В присутствии бихроматов раствор окрашивается в фиолетовый цвет, но не флуоресцирует.
