
- •САмостійна робота № 1
- •Загальні методичні вказівки Класифікація органічних сполук.
- •Типи органічних реакцій.
- •Алкани, циклоалкани в природі та техніці.
- •Дієнові вуглеводні, їх характеристика.
- •Багатоядерні ароматичні вуглеводні з ізольованими бензольними ядрами.
- •Нафта, її переробка та склад.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 2
- •Загальні методичні вказівки Похідні вуглеводнів. Ізомерія та номенклатура.
- •Фізичні та хімічні властивості похідних вуглеводнів.
- •Фторпохідні органічні сполуки. Добування та застосування.
- •Основні представники галогенопохідних, їх застосування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 3
- •Загальні методичні вказівки Феноли та нафтоли.Ізомерія і номенклатура.
- •Засоби добування та властивості фенолів та нафтолів.
- •Прості ефіри – номенклатура, ізомерія, властивості.
- •Основні представники. Епоксиди.
- •Етилен оксид в харчовій промисловості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 4
- •Загальні методичні вказівки Кетони – ізомерія, номенклатура.
- •Властивості та добування кетонів.
- •Окремі представники, їх характеристика.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 5
- •Загальні методичні вказівки Двоосновні карбонові кислоти – ізомерія та номенклатура.
- •Властивості, добування та застосування двоосновних карбонових кислот.
- •Мурашина та оцтова кислота, їх характеристика та добування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 6
- •Загальні методичні вказівки Похідні карбонових кислот,їх характеристика.
- •Галогенангідриди –номенклатура, засоби добування та властивості.
- •Ангідриди карбонових кислот –добування, властивості.
- •Окремі представники: оцтовийта фталевий ангідриди.
- •Пероксиди, їх характеристика.
- •Складні ефіри –властивості,добування.
- •Мила, їх властивості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 7
- •Загальні методичні вказівки Дубильні речовини.
- •Галова кислота, її властивості.
- •Альдегідо- та кетонокислоти. Добування та номенклатура.
- •Окремі представники кетонокислот. Пировиноградна кислота.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 8
- •Загальні методичні вказівки Засоби добування нітросполук.
- •Нітробензол.
- •Аліфатичні діазосполуки.
- •Аміди кислот.
- •Сечовина, її властивості.
- •Нітрили кислот.
- •Акрилонітрил в хімічній промисловості
- •Органічні сполуки сірки.Застосування та добування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 9
- •Загальні методичні вказівки Важливі представники п’ятичленнихгетероциклів з одним гетероатомом.
- •Важливі представники п’ятичленних гетероциклів з двома гетероатомами.
- •Важливі представники шестичленних гетероциклів з одним гетероатомом.
- •Складні гетероциклічні сполуки, їх характеристика.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 10
- •Загальні методичні вказівки Методи досліджень ліпідів.
- •Добування та переробка жирів та масел.
- •Поверхнево-активні речовини.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 11
- •Загальні методичні вказівки Стереохімія моносахаридів.
- •Найважливіші представники моносахаридів, їх застосування у харчовій промисловості.
- •Таутомерія моносахаридів в розчинах.
- •Високомолекулярні полісахариди.
- •Крохмаль, його будова, властивості та застосування у харчовій промисловості.
- •Целюлоза, її будова, властивості та застосування у промисловості.
- •Глікоген, як тваринний крохмаль.
- •Пектинові речовини, їх властивості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 12
- •Загальні методичні вказівки
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 13
- •Загальні методичні вказівки Аденозинтрифосфорна кислота
- •Біосинтез білків
- •Терпени, їх характеристика, класифікація та властивості.
- •Біциклічні терпени.
- •Стероїди, їх властивості та роль в житті людини.
- •Гормони, їх властивості та роль в житті людини.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 15
- •Загальні методичні вказівки
- •Завдання для виконання самостійної роботи
- •Рекомендована література
Прості ефіри – номенклатура, ізомерія, властивості.
Простими ефірами називають сполуки з загальною формулою R – О – R1; Аr – О – R; Аr – О – Аr, де R, R1, Аr – вуглеводневі радикали. Їх можна розглядати як продукти заміщення атому водню у молекулі оксисполук на радикал.
Для найменування ефірів можуть використовувати тривіальні назви (сірчаний ефір, фенетол), але у більшості випадків назва ефірів складається з назви радикалів, з додавання слова ефір: діметиловий ефір, діетиловий ефір, метилетиловий ефір. По ІЮПАК для найменування простих ефірів до назви вуглеводню додають назву алкокси (RО) абоарілокси групи (АrО). За основу назви вибирають радикал з більшим числом атомів вуглецю:
СН3 – О – СН3 СН3 – О – С2Н5 C6H5 – О – C6H5
діметиловий ефір, метилетиловий ефір, дифеніловий ефір,
Ізомерія ефірів пов’язана зі складом та будовою радикалів.
Способи добування.
Взаємодіяалкоголятів з галоген алкінами.
C2H5 – О – Na+C2H5I C2H5 – О – C2H5+NaІ
етилат натрію етил йодид діетиловий ефір
Взаємодія ацетилену зі спиртами. Вона використовується для добування простих алкілвінілових ефірів.
СН
≡ СН + НОС2Н5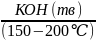 →
СН2
= СН – О – СН2
– СН3
→
СН2
= СН – О – СН2
– СН3
ацетилен етиловий спирт етил вініловий ефір
Фізичні властивості.Перші два представника простих ефірів: діметиловий та метилетиловий ефір – гази; починаючи з діетилового ефіру – рідини. Температура кипіння ефірів нижче температури кипіння відповідних спиртів, так як їх молекули не асоційовані за рахунок водневих зв’язків. Вони мають приємний (ефірним) запах, більшість із них погано розчинні у воді, але добре в багатьох органічних розчинниках.
Хімічні властивості. Прості ефіри – стійкі органічні сполуки. Вони не гідролізуються, в звичайних умовах не вступають в взаємодію з металевим натрієм, на них не діють луги та більшість кислот.
Взаємодія з йодоводнем. C2H5 – О – C2H5+ НІ → C2H5 – ОН +C2H5I
Приєднання сильних кислот. Ефіри розчиняються у кислотах з виділенням теплоти:C2H5 – О – C2H5+ НСІ →C2H5 – О – C2H5· НСІ. Отриману сполуку можна розглядати як сіль оксонію.
Утворення пероксидів. На світлі при збереженні прості ефіри окислюються з утворенням перекислих сполук:
R
– СН2
– О – R1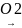 R
– СН – О – R1
R
– СН – О – R1
│
О – ОН
Отримані перекосі (головним чином у виді гідроперекосей) є дуже небезпечними при роботі з ефірами, так як вони можуть бути причиною вибуху.
Основні представники. Епоксиди.
Діетиловий ефір,етоксіетан, сірчаний ефірC2H5 – О – C2H5. Безбарвна рухома рідина з ефірним запахом, горюча. Широко використовується у якості органічного розчинника, володіє анастизуючою дією.
Ефіри фенолів: C6H5 – О – CH3 – анізол; C6H5 – ОC2H5 – фенетол – висококип’ячі рідини з приємним запахом, використовують у парфумерній промисловості.
Діоксан – простий циклічний ефір етиленгліколю. Використовується у якості органічного розчинника.
Епоксиди, або епокисями, називають прості ефіри циклічної будови з α-окисним кільцем:
 R
R1
R
R1


 С
С
С
С
Н Н
О
Відрізняються високою реакційною здібністю. Найбільш важливий представник епоксидів – окись етилену.
