
- •САмостійна робота № 1
- •Загальні методичні вказівки Класифікація органічних сполук.
- •Типи органічних реакцій.
- •Алкани, циклоалкани в природі та техніці.
- •Дієнові вуглеводні, їх характеристика.
- •Багатоядерні ароматичні вуглеводні з ізольованими бензольними ядрами.
- •Нафта, її переробка та склад.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 2
- •Загальні методичні вказівки Похідні вуглеводнів. Ізомерія та номенклатура.
- •Фізичні та хімічні властивості похідних вуглеводнів.
- •Фторпохідні органічні сполуки. Добування та застосування.
- •Основні представники галогенопохідних, їх застосування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 3
- •Загальні методичні вказівки Феноли та нафтоли.Ізомерія і номенклатура.
- •Засоби добування та властивості фенолів та нафтолів.
- •Прості ефіри – номенклатура, ізомерія, властивості.
- •Основні представники. Епоксиди.
- •Етилен оксид в харчовій промисловості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 4
- •Загальні методичні вказівки Кетони – ізомерія, номенклатура.
- •Властивості та добування кетонів.
- •Окремі представники, їх характеристика.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 5
- •Загальні методичні вказівки Двоосновні карбонові кислоти – ізомерія та номенклатура.
- •Властивості, добування та застосування двоосновних карбонових кислот.
- •Мурашина та оцтова кислота, їх характеристика та добування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 6
- •Загальні методичні вказівки Похідні карбонових кислот,їх характеристика.
- •Галогенангідриди –номенклатура, засоби добування та властивості.
- •Ангідриди карбонових кислот –добування, властивості.
- •Окремі представники: оцтовийта фталевий ангідриди.
- •Пероксиди, їх характеристика.
- •Складні ефіри –властивості,добування.
- •Мила, їх властивості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 7
- •Загальні методичні вказівки Дубильні речовини.
- •Галова кислота, її властивості.
- •Альдегідо- та кетонокислоти. Добування та номенклатура.
- •Окремі представники кетонокислот. Пировиноградна кислота.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 8
- •Загальні методичні вказівки Засоби добування нітросполук.
- •Нітробензол.
- •Аліфатичні діазосполуки.
- •Аміди кислот.
- •Сечовина, її властивості.
- •Нітрили кислот.
- •Акрилонітрил в хімічній промисловості
- •Органічні сполуки сірки.Застосування та добування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 9
- •Загальні методичні вказівки Важливі представники п’ятичленнихгетероциклів з одним гетероатомом.
- •Важливі представники п’ятичленних гетероциклів з двома гетероатомами.
- •Важливі представники шестичленних гетероциклів з одним гетероатомом.
- •Складні гетероциклічні сполуки, їх характеристика.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 10
- •Загальні методичні вказівки Методи досліджень ліпідів.
- •Добування та переробка жирів та масел.
- •Поверхнево-активні речовини.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 11
- •Загальні методичні вказівки Стереохімія моносахаридів.
- •Найважливіші представники моносахаридів, їх застосування у харчовій промисловості.
- •Таутомерія моносахаридів в розчинах.
- •Високомолекулярні полісахариди.
- •Крохмаль, його будова, властивості та застосування у харчовій промисловості.
- •Целюлоза, її будова, властивості та застосування у промисловості.
- •Глікоген, як тваринний крохмаль.
- •Пектинові речовини, їх властивості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 12
- •Загальні методичні вказівки
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 13
- •Загальні методичні вказівки Аденозинтрифосфорна кислота
- •Біосинтез білків
- •Терпени, їх характеристика, класифікація та властивості.
- •Біциклічні терпени.
- •Стероїди, їх властивості та роль в житті людини.
- •Гормони, їх властивості та роль в житті людини.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 15
- •Загальні методичні вказівки
- •Завдання для виконання самостійної роботи
- •Рекомендована література
Мурашина та оцтова кислота, їх характеристика та добування.
Мурашина кислота НСООН – безбарвна рідина з різким запахом, кипить при 1010С. Розчиняється у воді в будь-яких пропорціях. Викликає опіки на шкірі. Міститься у виділеннях залоз мурашок, а також у деяких рослинах (наприклад, у листі кропиви).
За хімічними властивостями мурашина кислота найбільш реакційно здатна з усіх карбонових кислот. Це пояснюється тим, що її карбоксильна група сполучена з воднем, а не з вуглеводневим радикалом. Завдяки наявності в молекулі альдегідної групи мурашина кислота має властивості альдегіду:
⁄ ⁄
О
⁄⁄ О
⁄
О
⁄⁄ О
Н – С і НО – С
 \\
\\
ОН Н
карбоксильна альдегідна
група група
тобто виявляє відновні властивості (дає реакцію «срібного дзеркала»):
НСООН + Аg2О → 2Аg↓ + СО2↑ + Н2О
При нагріванні розкладається на оксид вуглецю (ІІ) і воду:
НСООН → СО + Н2О
Раніше мурашину кислоту добували вимочуванням мурашок у воді з наступною перегонкою розчину. Тепер її добувають з оксиду вуглецю (ІІ) та їдкого натрію:
⁄⁄ О
СО + NaОН → H – С
\
ОNa.
З утворенням солі дією сірчаної кислоти витісняють, а потім відганяють мурашину кислоту:
НСООNa + H2SO4 → HCOOH + NaHSO4.
Через те, що мурашина кислота легко окислюється, її не можна добувати загальними методами.
Оцтова кислота СН3СООН при звичайній температурі – безбарвна рідина з різким характерним запахом. При температурі нижчій за +16,60С вона твердіє у вигляді кристалів, схожих на лід, через що дістала назву льодяної кислоти. Оцтова кислота у воді розчиняється у будь-яких пропорціях. 3-5%-ний водний розчин її відомий під назвою оцту, який вживають як приправу до їжі. 70-80%-на оцтова кислота називається оцтовою есенцією.
За хімічними властивостями оцтова кислота подібна до мінеральних кислот.
Метали, що стоять в ряду напруги до водню, заміщують водень карбоксильної групи, утворюючи солі:
2СН3СООН + Мg → (СН3СООН)2Мg + Н2↑
Оцтова кислота вступає в реакції нейтралізації з основами.
СН3СООН + NaОН → СН3СООNa + Н2О
Вона легко взаємодіє з солями, витісняючи більш слабкі і більш леткі кислоти.
2СН3СООН + СаСО3 → (СН3СООН)2Са + Н2О + СО2↑
Оцтова кислота легко взаємодіє з аміаком, утворюючи сіль – ацетат амонію:
СН3СООН + NН3 → СН3СООNН4
Взаємодією оцтової кислоти з основами, оксидами і солями користуються для добування її солей.
Сучасний синтетичний спосіб добування оцтової кислоти оснований на окисленні оцтового альдегіду, який у свою чергу добувають з ацетилену за реакцією М.Г. Кучерова (ацетилен добувають з досить доступної природної сировини - метану):
⁄⁄ О ⁄⁄ О
СН
≡ СН + Н2О
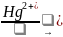 CН3
– С
CН3
– С
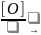 CН3
– С
CН3
– С
\ \
Н ОН
Великого значення набуває новий спосіб добування оцтової кислоти окисленням бутану:
¦ ⁄⁄ О
2СН3 – СН2 – СН2 – СН3 + 5О2 4СН3 – С + 2Н2О
¦ \
ОН
На відміну від добування оцтової кислоти з метану, яке є багатостадійним (метан → ацетилен → оцтовий альдегід → оцтова кислота), окислення бутану до оцтової кислоти скорочує цю стадійність, що дає великий економічний ефект при виробництві багатотоннажних речовин.
