
- •САмостійна робота № 1
- •Загальні методичні вказівки Класифікація органічних сполук.
- •Типи органічних реакцій.
- •Алкани, циклоалкани в природі та техніці.
- •Дієнові вуглеводні, їх характеристика.
- •Багатоядерні ароматичні вуглеводні з ізольованими бензольними ядрами.
- •Нафта, її переробка та склад.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 2
- •Загальні методичні вказівки Похідні вуглеводнів. Ізомерія та номенклатура.
- •Фізичні та хімічні властивості похідних вуглеводнів.
- •Фторпохідні органічні сполуки. Добування та застосування.
- •Основні представники галогенопохідних, їх застосування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 3
- •Загальні методичні вказівки Феноли та нафтоли.Ізомерія і номенклатура.
- •Засоби добування та властивості фенолів та нафтолів.
- •Прості ефіри – номенклатура, ізомерія, властивості.
- •Основні представники. Епоксиди.
- •Етилен оксид в харчовій промисловості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 4
- •Загальні методичні вказівки Кетони – ізомерія, номенклатура.
- •Властивості та добування кетонів.
- •Окремі представники, їх характеристика.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 5
- •Загальні методичні вказівки Двоосновні карбонові кислоти – ізомерія та номенклатура.
- •Властивості, добування та застосування двоосновних карбонових кислот.
- •Мурашина та оцтова кислота, їх характеристика та добування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 6
- •Загальні методичні вказівки Похідні карбонових кислот,їх характеристика.
- •Галогенангідриди –номенклатура, засоби добування та властивості.
- •Ангідриди карбонових кислот –добування, властивості.
- •Окремі представники: оцтовийта фталевий ангідриди.
- •Пероксиди, їх характеристика.
- •Складні ефіри –властивості,добування.
- •Мила, їх властивості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 7
- •Загальні методичні вказівки Дубильні речовини.
- •Галова кислота, її властивості.
- •Альдегідо- та кетонокислоти. Добування та номенклатура.
- •Окремі представники кетонокислот. Пировиноградна кислота.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 8
- •Загальні методичні вказівки Засоби добування нітросполук.
- •Нітробензол.
- •Аліфатичні діазосполуки.
- •Аміди кислот.
- •Сечовина, її властивості.
- •Нітрили кислот.
- •Акрилонітрил в хімічній промисловості
- •Органічні сполуки сірки.Застосування та добування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 9
- •Загальні методичні вказівки Важливі представники п’ятичленнихгетероциклів з одним гетероатомом.
- •Важливі представники п’ятичленних гетероциклів з двома гетероатомами.
- •Важливі представники шестичленних гетероциклів з одним гетероатомом.
- •Складні гетероциклічні сполуки, їх характеристика.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 10
- •Загальні методичні вказівки Методи досліджень ліпідів.
- •Добування та переробка жирів та масел.
- •Поверхнево-активні речовини.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 11
- •Загальні методичні вказівки Стереохімія моносахаридів.
- •Найважливіші представники моносахаридів, їх застосування у харчовій промисловості.
- •Таутомерія моносахаридів в розчинах.
- •Високомолекулярні полісахариди.
- •Крохмаль, його будова, властивості та застосування у харчовій промисловості.
- •Целюлоза, її будова, властивості та застосування у промисловості.
- •Глікоген, як тваринний крохмаль.
- •Пектинові речовини, їх властивості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 12
- •Загальні методичні вказівки
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 13
- •Загальні методичні вказівки Аденозинтрифосфорна кислота
- •Біосинтез білків
- •Терпени, їх характеристика, класифікація та властивості.
- •Біциклічні терпени.
- •Стероїди, їх властивості та роль в житті людини.
- •Гормони, їх властивості та роль в житті людини.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 15
- •Загальні методичні вказівки
- •Завдання для виконання самостійної роботи
- •Рекомендована література
САмостійна робота № 7
Тема: Дубильні речовини.
Повинні знати: властивості дубильних речовин, добування та номенклатуру альдегідо та кетонокислот, окремих предстпвників
Повинні вміти: писати структурні формули дубільних речовин, галової кислоти, альдегідо та кетонокислот
План.
Дубильні речовини.
Галова кислота, її властивості.
Альдегідо та кетонокислоти. Добування та номенклатура.
Окремі представники кетонокислот.Пировиноградна кислота.
Загальні методичні вказівки Дубильні речовини.
У процесі вичинки шкури тварин підлягають дублінню, завдяки чому збільшується міцність шкіри, зменшується набрякання під дією води, надається необхідна еластичність. Речовини, які викликають дубління, називають дубильними речовинами. Ця назва нагадує про те, що у свій час головним джерелом дубильних речовин була кора дуба. В теперішній час для дублювання використовують неорганічні речовини (солі трьохвалентного хрому, алюмінію та ін.), органічні речовини рослинного походження або добуті синтетично.
Однією найважливішою дубильною речовиною є танін, який добувають із наростів на дубових листках (чорнильних горіхів, - ця назва пішла з тих пір, коли чорнила готували змішуючи танін з солями двовалентного заліза; такий розчин почти безбарвний, при окисленні залаза на повітрі та взаємодії з ним таніну відбувається поступове проявлення чорного міцного кольору). Відомо декілька типів танінів. Багато яких з них є складними ефірами, побудованих з декількох молекул галової кислоти, - депсіди:
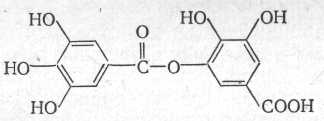
дидепсид (м-дигалова кислота)
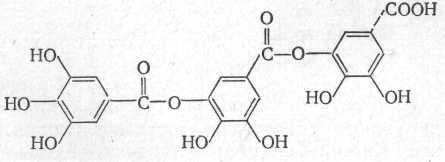
тридепсид
Інші таніни є ефіри галової кислоти з вуглеводами, частіше всього з глюкозою.
Синтетичні дубильні речовини по хімічній природі частіше всього є сульфопохідні багатоядерних фенолів, наприклад:

Галова кислота, її властивості.
Галава кислота, 3,4,5-триоксибензойна кислота
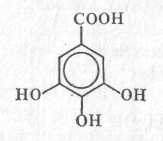
Кристалічна речовина, добре розчинна у гарячій воді. На повітрі окислюється та темніє. При нагріванні легко втрачає двоокись вуглецю та перетворюється у пірагалол. У природі галова кислота зустрічається як у вільному виді, так і пов’язаному стані, зазвичай у рослинах, які містять дубильні речовини (чорнильні горіхи, дубова кора, листя чаю). Вперше її добув Шеєле ще у кінці ХVІІ століття. Добувають гідролізом таніну. Використовують для добування пірагалолу, який утворюється при її нагріванні, синтезу барвників, у аналітичній хімії.
Альдегідо- та кетонокислоти. Добування та номенклатура.
Альдегідо- та кетонокислоти – це гетерофункціональні сполуки, у молекулах яких містяться одночасно оксо- (альдегідна або кетонна) та карбоксильна групи. Назва альдегідо- та кетокислот будується на основі відповідних карбонових кисмлот з вказанням положення карбонільної групи. Часто користуються тривіальними назвами кислот:
Н – С – СООН СН3 – С – СООН СН3 – С – СН2 – СООН
О О О
гліоксилова кислота піровиноградна кислота ацетооцтова кислота
(2-оксопропіонова) (3-оксомасляна)
СН3 – С – СН2 – СН2 –СООН
О
4-оксовалерьянова кислота
Для добування альдегідо- та кетокислот використовують реакції, за допомогою яких вводиться карбонільна група у карбоксильні сполуки, або, навпаки, карбоксил вводиться у сполуки, які вже містять альдегідну або кетонну групи.
Окислення гліколей:
НО
– СН2
– СН2
– ОН
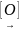 Н – С – СООН
Н – С – СООН
О
етиленгліколь гліоксилова кислота
Гідроліз дигалогензамісних кислот:

 ОН
ОН
СІ2СН
– СООН
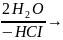 Н – С – СООН
Н – С – СООН
Н – С – СООН
Н – С – СООН
дихлороцтова кислота
ОН О
гліоксилова кислота
Окислення оксикислот:
СН3 – СН – СН2 – СН2 – СООН СН3 – С – СН2 – СН2 – СООН
ОН О
-оксивалерьянова кислота 4-оксовалерьянова кислота
