
- •САмостійна робота № 1
- •Загальні методичні вказівки Класифікація органічних сполук.
- •Типи органічних реакцій.
- •Алкани, циклоалкани в природі та техніці.
- •Дієнові вуглеводні, їх характеристика.
- •Багатоядерні ароматичні вуглеводні з ізольованими бензольними ядрами.
- •Нафта, її переробка та склад.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 2
- •Загальні методичні вказівки Похідні вуглеводнів. Ізомерія та номенклатура.
- •Фізичні та хімічні властивості похідних вуглеводнів.
- •Фторпохідні органічні сполуки. Добування та застосування.
- •Основні представники галогенопохідних, їх застосування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 3
- •Загальні методичні вказівки Феноли та нафтоли.Ізомерія і номенклатура.
- •Засоби добування та властивості фенолів та нафтолів.
- •Прості ефіри – номенклатура, ізомерія, властивості.
- •Основні представники. Епоксиди.
- •Етилен оксид в харчовій промисловості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 4
- •Загальні методичні вказівки Кетони – ізомерія, номенклатура.
- •Властивості та добування кетонів.
- •Окремі представники, їх характеристика.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 5
- •Загальні методичні вказівки Двоосновні карбонові кислоти – ізомерія та номенклатура.
- •Властивості, добування та застосування двоосновних карбонових кислот.
- •Мурашина та оцтова кислота, їх характеристика та добування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 6
- •Загальні методичні вказівки Похідні карбонових кислот,їх характеристика.
- •Галогенангідриди –номенклатура, засоби добування та властивості.
- •Ангідриди карбонових кислот –добування, властивості.
- •Окремі представники: оцтовийта фталевий ангідриди.
- •Пероксиди, їх характеристика.
- •Складні ефіри –властивості,добування.
- •Мила, їх властивості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 7
- •Загальні методичні вказівки Дубильні речовини.
- •Галова кислота, її властивості.
- •Альдегідо- та кетонокислоти. Добування та номенклатура.
- •Окремі представники кетонокислот. Пировиноградна кислота.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 8
- •Загальні методичні вказівки Засоби добування нітросполук.
- •Нітробензол.
- •Аліфатичні діазосполуки.
- •Аміди кислот.
- •Сечовина, її властивості.
- •Нітрили кислот.
- •Акрилонітрил в хімічній промисловості
- •Органічні сполуки сірки.Застосування та добування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 9
- •Загальні методичні вказівки Важливі представники п’ятичленнихгетероциклів з одним гетероатомом.
- •Важливі представники п’ятичленних гетероциклів з двома гетероатомами.
- •Важливі представники шестичленних гетероциклів з одним гетероатомом.
- •Складні гетероциклічні сполуки, їх характеристика.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 10
- •Загальні методичні вказівки Методи досліджень ліпідів.
- •Добування та переробка жирів та масел.
- •Поверхнево-активні речовини.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 11
- •Загальні методичні вказівки Стереохімія моносахаридів.
- •Найважливіші представники моносахаридів, їх застосування у харчовій промисловості.
- •Таутомерія моносахаридів в розчинах.
- •Високомолекулярні полісахариди.
- •Крохмаль, його будова, властивості та застосування у харчовій промисловості.
- •Целюлоза, її будова, властивості та застосування у промисловості.
- •Глікоген, як тваринний крохмаль.
- •Пектинові речовини, їх властивості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 12
- •Загальні методичні вказівки
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 13
- •Загальні методичні вказівки Аденозинтрифосфорна кислота
- •Біосинтез білків
- •Терпени, їх характеристика, класифікація та властивості.
- •Біциклічні терпени.
- •Стероїди, їх властивості та роль в житті людини.
- •Гормони, їх властивості та роль в житті людини.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 15
- •Загальні методичні вказівки
- •Завдання для виконання самостійної роботи
- •Рекомендована література
Галогенангідриди –номенклатура, засоби добування та властивості.
О
З агальна формула галогенангідридів карбонових кислот R – C ,
Х
де Х – фтор, хлор, бром, йод. Назва їх будується по принципу галогеналкілів: низивається ацил і атом галогену, наприклад Н – С – СІ – формілхлорид і т.п..
О
Галогенангідриди кислот утворюються при дії галогенідів фосфору (РСІ5, РСІ3), тіонілхлориду на кислоти або їх ангідриди:
О О
С Н3СН2
– С + РСІ5
СН3
–
СН2
– С + РОСІ3
+ НСІ
Н3СН2
– С + РСІ5
СН3
–
СН2
– С + РОСІ3
+ НСІ
ОН СІ
пропіонова кислота пропіонілхлорид
Галогенангідриди – рідини або тверді речовини з різким запахом, розкладаються водою («димлять» на повітрі):
О О
С Н3 – С + Н2О СН3 – С + НСІ
СІ ОН
ацетилхлорид оцтова кислота
Галогенангідриди – найбільш реакційноздібні похідні карбонових кислот. Для них характерна реакція нуклеофільного заміщення, пов’язана з обміном атому галогену на інші атоми і групи, і введення до молекули реагуючої з ним речовини ацилу (реакції ацилірування). Хлорангідриди ароматичного ряду менш активні, чим аліфатичного.
Реакції ацилірування:
г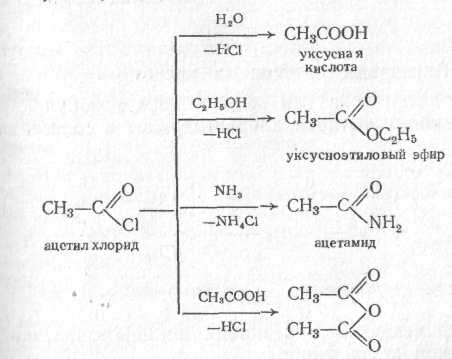 ідроліз
ідроліз
алкоголіз
амоноліз
ацидоліз
Відновлення хлорангідридів:
О
С
Н3
–
СН2
– С
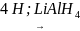 СН3
–
СН2
– СН2ОH
+ НСІ
СН3
–
СН2
– СН2ОH
+ НСІ
СІ
пропіонілхлорид
Ангідриди карбонових кислот –добування, властивості.
Добуваються при відділенні молекули води від двох молекул карбонової кислоти чи взаємодією хлорангідридів з солями цих кислот:
О
 О
СН3-С
О
СН3-С
СН3-С
+ СН3CООNa
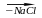 О
О
СІ СН3-С
ацетил хлорид ацетат натрія О
оцтовий ангідрид
Ангідриди нижчих кислот – рідини з різким запахом, нерозчинні у воді. Ангідриди вищих кислот – кристалічні речовини, без запаху. Температури кипіння ангідридів вищі, чим температури кипіння відповідних кислот.
По хімічним властивостям ангідриди нагадують хлорангідриди. Вони також є ациліруючими засобами, но реакції з ними проходять більш м’ягко, чим з хлорангідридами. Дією ангідридів на спирти отримуємо складні ефіри, дією на амміак – аміди.
Ангідриди кислот використовуються у реакціях ацилірованія, но вони менш активні, чим хлорангідриди:
 О
NH
СН3СОNH2
+ СН3СОNH4
(аммоноліз)
О
NH
СН3СОNH2
+ СН3СОNH4
(аммоноліз)
С Н3-С ацетамід
О О
С Н3-С
О СН ОН СН3С-ОСН3 + СН3СООН (алкоголіз)
оцтовий ангідрид метілацетат
