
- •САмостійна робота № 1
- •Загальні методичні вказівки Класифікація органічних сполук.
- •Типи органічних реакцій.
- •Алкани, циклоалкани в природі та техніці.
- •Дієнові вуглеводні, їх характеристика.
- •Багатоядерні ароматичні вуглеводні з ізольованими бензольними ядрами.
- •Нафта, її переробка та склад.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 2
- •Загальні методичні вказівки Похідні вуглеводнів. Ізомерія та номенклатура.
- •Фізичні та хімічні властивості похідних вуглеводнів.
- •Фторпохідні органічні сполуки. Добування та застосування.
- •Основні представники галогенопохідних, їх застосування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 3
- •Загальні методичні вказівки Феноли та нафтоли.Ізомерія і номенклатура.
- •Засоби добування та властивості фенолів та нафтолів.
- •Прості ефіри – номенклатура, ізомерія, властивості.
- •Основні представники. Епоксиди.
- •Етилен оксид в харчовій промисловості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 4
- •Загальні методичні вказівки Кетони – ізомерія, номенклатура.
- •Властивості та добування кетонів.
- •Окремі представники, їх характеристика.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 5
- •Загальні методичні вказівки Двоосновні карбонові кислоти – ізомерія та номенклатура.
- •Властивості, добування та застосування двоосновних карбонових кислот.
- •Мурашина та оцтова кислота, їх характеристика та добування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 6
- •Загальні методичні вказівки Похідні карбонових кислот,їх характеристика.
- •Галогенангідриди –номенклатура, засоби добування та властивості.
- •Ангідриди карбонових кислот –добування, властивості.
- •Окремі представники: оцтовийта фталевий ангідриди.
- •Пероксиди, їх характеристика.
- •Складні ефіри –властивості,добування.
- •Мила, їх властивості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 7
- •Загальні методичні вказівки Дубильні речовини.
- •Галова кислота, її властивості.
- •Альдегідо- та кетонокислоти. Добування та номенклатура.
- •Окремі представники кетонокислот. Пировиноградна кислота.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 8
- •Загальні методичні вказівки Засоби добування нітросполук.
- •Нітробензол.
- •Аліфатичні діазосполуки.
- •Аміди кислот.
- •Сечовина, її властивості.
- •Нітрили кислот.
- •Акрилонітрил в хімічній промисловості
- •Органічні сполуки сірки.Застосування та добування.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 9
- •Загальні методичні вказівки Важливі представники п’ятичленнихгетероциклів з одним гетероатомом.
- •Важливі представники п’ятичленних гетероциклів з двома гетероатомами.
- •Важливі представники шестичленних гетероциклів з одним гетероатомом.
- •Складні гетероциклічні сполуки, їх характеристика.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 10
- •Загальні методичні вказівки Методи досліджень ліпідів.
- •Добування та переробка жирів та масел.
- •Поверхнево-активні речовини.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 11
- •Загальні методичні вказівки Стереохімія моносахаридів.
- •Найважливіші представники моносахаридів, їх застосування у харчовій промисловості.
- •Таутомерія моносахаридів в розчинах.
- •Високомолекулярні полісахариди.
- •Крохмаль, його будова, властивості та застосування у харчовій промисловості.
- •Целюлоза, її будова, властивості та застосування у промисловості.
- •Глікоген, як тваринний крохмаль.
- •Пектинові речовини, їх властивості.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 12
- •Загальні методичні вказівки
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 13
- •Загальні методичні вказівки Аденозинтрифосфорна кислота
- •Біосинтез білків
- •Терпени, їх характеристика, класифікація та властивості.
- •Біциклічні терпени.
- •Стероїди, їх властивості та роль в житті людини.
- •Гормони, їх властивості та роль в житті людини.
- •Завдання для виконання самостійної роботи
- •САмостійна робота № 15
- •Загальні методичні вказівки
- •Завдання для виконання самостійної роботи
- •Рекомендована література
Окремі представники: оцтовийта фталевий ангідриди.
Оцтовий ангідрид – рідина, не змішується з водою і на холоді лише повільно з нею реагує. Добувають у промисловості у великих кількостях з кетену та оцтової кислоти:
О
СН3-С
С Н2 = С = О + СН3СООН О
кетен оцтова кислота СН3-С
О
Велика кількість оцтового ангідриду витрачається на виробництво штучного ацетатного волокна. Оцтовий ангідрид використовується як ацеліруючий засіб.
Фталевий ангідрид – це кристалічна речовина, кристалізується у виді голок, легко возгоняється. У промисловості фталевий ангідрид добувають окисленням нафталіну і використовують для різного синтезу.
При взаємодії з амміаком фталевий ангідрид утворює імід фталевої кислоти – фталімід. При конденсації фталевого ангідриду з бензолом у присутності хлористого алюмінію отримуємо антрахінон (промисловий спосіб) широко використовуємий у виробництві барвників.
Для фталевого ангідриду характерна реакція конденсації з фенолами за рахунок карбоксильного кисню. В результаті даної реакції утворюється фталеін – сполука, яка відноситься до похідних трифенилметану.
Пероксиди, їх характеристика.
При заміщенні атомів водню у молекулі пероксиду водню Н – О – О – Н на вуглеводневі радикали отримують гідропероксиди (заміщений один атом водню) та пероксиди (заміщено два атоми водню):
R – О – ОН R – О – О – R1
гідропероксиди пероксиди
Пероксидні сполуки добувають при аутоокисленні вуглеводнів, реакція відбувається по вільнорадикальному механізму. Гідропероксиди мають кислотні властивості, при взаємодії з розчинами лугів утворюють солі. Пероксиди та гідропероксиди відносяться до сильних окисників. Робота з ними вимагає обережності так як вони є вибухонебезпечні.
При взаємодії ангідридів або хлорангідридів кислот з пероксидами металів отримуються пероксиди ацилів:
О О О
2С6Н5
– С – СІ
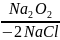 С6Н5
– С –О – О – С –С6Н5
С6Н5
– С –О – О – С –С6Н5
пероксид бензоілу
При взаємодії пероксид ацилів з алкоголятом натрію та послідовною дією мінеральних кислот добувають гідропероксиди ацилів або надкислоти (перкислоти):
О О О О
С6Н5
– С –О – О – С –С6Н5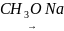 С6Н5
– С –ОONa
+ С6Н5
– С –ОСН3
С6Н5
– С –ОONa
+ С6Н5
– С –ОСН3
О
С6Н5 – С –ООН
надбензойна кислота
Пероксиди ацилів та надкислоти – сильні окисники. На холоді надкислоти повільно розкладаються, виділяя кисень, а при нагріванні вибухають, тому перегоняти їх неможна. Діючи як окисники, вони виділяють галоген з галогеноводнів, окислюють алкени до окисей. Зазвичай їх використовують у воді розчинів в хлороформі або чотирьоххлористому вуглеці.
