
- •7.0917.06 “Технологія зберігання, консервування і переробки плодів та овочів”
- •7.0917.07 “Технологія зберігання, консервування та переробки м’яса”
- •7.0917.11 “Технологія харчування”
- •Програма курсу вступ
- •Теоретичні уявлення в органічній хімії
- •Вуглеводні алкани
- •Алкадієни
- •Циклоалкани і циклоалкени
- •Галогенпохідні вуглеводнів
- •Похідні вуглеводнів, що містять гідроксил
- •Карбонільні сполуки (оксосполуки) альдегіди і кетони
- •Карбонові кислоти
- •Окси- і оксокислоти
- •Вуглеводи
- •Органічні сполуки, що містять азот
- •Амінокислоти
- •Гетероциклічні сполуки
- •Пестициди
- •Методичні рекомендації
- •Класифікація органічних сполук
- •Правила техніки безпеки у лабораторії органічної хімії та надання першої допомоги ( загальні правила )
- •Перша допомога при опіках та отруєннях
- •Гасіння місцевої пожежі та одягу що горить
- •Лабораторна робота №1 виділення та очищення органічних сполук, визначення фізичних констант, якісний аналіз
- •1. Перекристалізація
- •Перекристалізація з води
- •2. Сублімація (возгонка)
- •3. Екстракція (витяг)
- •4. Фракційна (дробна) перегонка
- •5. Визначення температури плавлення
- •6. Відкриття вуглецю і водню в органічній речовині
- •Лабораторна робота № 2 насичені та ненасичені вуглеводні
- •1. Одержання метану і дослідження його властивостей.
- •2. Одержання етилену і вивчення його властивостей
- •3. Одержання та властивості ацетилену
- •Завдання для самостійної роботи
- •Лабораторна робота №3 ароматичні вуглеводні
- •1. Одержання бензолу з бензойнокислого натрію
- •2. Відношення бензолу до брому
- •3. Взаємодія бензолу з водним розчином марганцевокислого калію
- •4. Властивості гомологів бензолу.
- •Завдання для самостійної роботи
- •Лабораторна робота № 4 галогенпохідні вуглеводнів
- •1. Одержання хлористого етилу
- •2. Утворення йодоформу з етилового спирту
- •3. Взаємодія хлороформу і чотирихлористого карбону з лугом Реактиви: хлороформ, чотирихлористий карбон, 10% розчин NaOh, нітратна кислота, AgNo3, kMnO4, аміак.
- •Завдання для самостійної роботи
- •Лабораторна робота №5 одно- й багатоатомні спирти. Феноли. Етери
- •1. Виявлення води у спирті
- •2. Розчинність спиртів у воді
- •3. Утворення алкоголяту і його гідроліз
- •4. Окиснення спиртів
- •5. Виявлення домішки метилового спирту в етиловому спирті
- •6. Відкриття сивушної олії
- •7. Якісна реакція на багатоатомні спирти
- •8. Розчинність, кислотний характер фенолів і нафтолів
- •9. Бромування фенолів
- •10. Кольорові реакції фенолів
- •Завдання для самостійної роботи
- •Лабораторна робота № 6 альдегіди і кетони
- •1.Одержання оцтового альдегіду при окисленні етилового спирту
- •2.Одержання ацетону з ацетату кальцію
- •Лабораторна робота №7 карбонові кислоти
- •1. Визначення реакції середовища деяких кислот
- •2. Доведення кислотних властивостей карбонових кислот
- •3. Дослідження окиснюваності деяких органічних кислот
- •4.Розклад мурашиної кислоти
- •5. Розклад щавлевої кислоти
- •6. Проба на ненасиченість олеїнової кислоти
- •7. Ізомеризація олеїнової кислоти в елаїдинову
- •8. Дія хлориду заліза (ііі) на оцтову кислоту (якісна реакція)
- •Завдання для самостійної роботи
- •Лабораторна робота №8 гідроксикислоти. Альдегідокислоти. Кетокислоти
- •1. Якісна реакція на a- оксикислоти з FeCl3
- •2.Розкладання молочної кислоти
- •3. Окислення молочної кислоти у піровиноградну
- •4. Утворення кислої і середньої солі винної кислоти
- •5. Доведення наявності оксигруп у винній кислоті
- •6. Розкладання лимонної кислоти
- •7. Взаємодія галової кислоти і таніну з FeCl3
- •Завдання для самостійної роботи
- •Лабораторна робота №9 естери. Жири та масла. Мила
- •1. Розчинність жирів у різноманітних розчинниках
- •2. Емульгування жирів
- •3. Одержання складних естерів
- •4. Акролеїнова проба на жири
- •5. Омилення жиру
- •6. Дослідження властивостей мила
- •В). Виділення вільних жирних кислот з мила.
- •7. Визначення йодного числа
- •Завдання для самостійної роботи
- •Лабораторна робота № 10 вуглеводи (моносахариди,дисахариди, полісахариди)
- •1. Загальна реакція на вуглеводи з - нафтолом
- •(Реакція Моліша)
- •2.Осмолення моносахаридів
- •3. Окислення моносахаридів реактивом Фелінга
- •4. Окислення моносахаридів аміачним розчином оксиду срібла (реакція срібного дзеркала)
- •9.Виявлення лактози у молоці
- •10. Кольорові реакції на сахарозу.
- •11.Карамелізація сахарози
- •12. Реакція крохмалю з йодом
- •13. Кислотний гідроліз крохмалю
- •14. Одержання рослинного пергаменту
- •15. Розчинення целюлози у мідно-аміачному розчині (реактиві Швейцера)
- •Завдання для самостійної роботи
- •Лабораторна робота №11 тема: аміни . Амінокислоти. Білки
- •1. Одержання аміну і дослідження деяких його властивостей
- •2.Реакції - амінокислот
- •3. Буферні властивості розчину білка
- •4. Осадження білків солями важких металів
- •5. Осадження білків мінеральними кислотами
- •6. Висолювання білків з розчинів
- •7. Осадження білків при нагріванні
- •8. Кольорові реакції білка.
- •Б) Ксантопротеінова реакція на білки й ароматичні амінокислоти
- •9. Відкриття аміногруп і сірки у білках
- •Завдання для самостійної роботи
- •Список рекомендованої літератури Основна
- •Додаткова
Завдання для самостійної роботи
Напишіть схеми реакцій послідовного одержання складного естеру з пропаналю та пропанону (через стадії добування кислот і спирту). Назвіть усі сполуки.
На основі ацетилену та етилового спирту отримайте етилацетат.
Напишіть схему утворення тригліцериду ліноленової кислоти. Поясніть процес висихання оліфи.
Напишіть схеми реакцій:
а) омилення трипальмітину;
б) каталітичного дегідрування олеїнодилінолену.
5. Наведіть рівняння реакцій, які лежать в основі виробництва плексиглазу, лавсану, гліфталевих смол.
Лабораторна робота № 10 вуглеводи (моносахариди,дисахариди, полісахариди)
1. Загальна реакція на вуглеводи з - нафтолом
(Реакція Моліша)
Реактиви: 15% спиртовий розчин нафтолу, концентрована сульфатна кислота, різні вуглеводи ( глюкоза, фруктоза, сахароза, крохмальний клейстер).
У пробірки налити по 0,5 мл води і внести дуже невеличку кількість вуглеводів: глюкози,фруктози, сахарози і крохмалю. Потім у кожну з пробірок додати 1-2 краплі спиртового розчину a–нафтолу і нахиливши пробірку, по стінках за допомогою піпетки обережно долити 1мл концентрованої сульфатної кислоти. Утвориться два шари: нижній -сульфатна кислота, верхній - водний шар. На межі двох шарів з'являється забарвлене кільце. Цю кольорову реакцію дають як моносахариди, так і полісахариди, причому кетози дають більш інтенсивне забарвлення чим альдози. При взаємодії концентрованої сульфатної кислоти вуглеводи розкладаються. Серед продуктів розкладання присутні фурфурол і його похідні. Вони конденсуються з нафтолом з утворенням забарвлених продуктів.
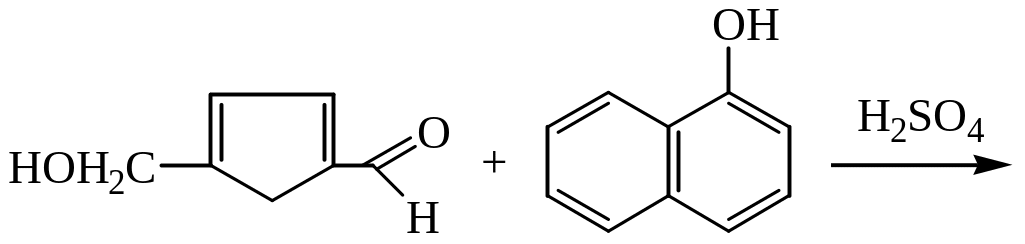
фурфурол α-нафтол
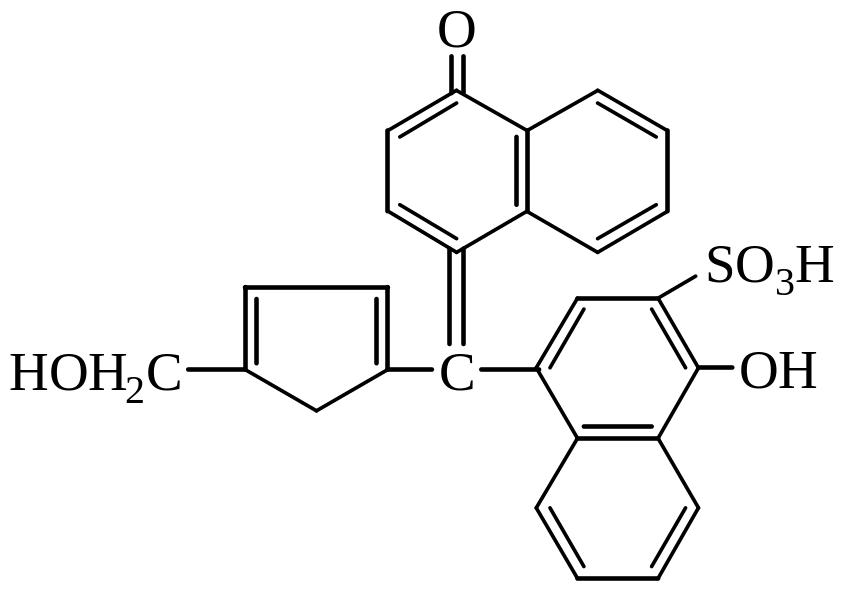
2.Осмолення моносахаридів
Реактиви: 10% розчин глюкози, 30-40% розчинNaOH, 10% розчин сульфатної кислоти.
У пробірці змішати 1,0 мл 10% розчину глюкози і 1,0 мл концентрованого розчину NaOH, внести в суміш кип'ятильні камінці і кип'ятити 2-3 хвилини. Рідина в пробірці набуває жовтого, а потім бурого кольору. Після охолодження її підкисліть 10% розчином сульфатної кислоти. Забарвлення блідне і з'являється запах паленого цукру.
При нагріванні з концентрованим розчином лугу моносахариди осмолюються і окиснюється. Утворюється складна суміш речовин. У ній містяться також продукти полімеризації і конденсації сполук, що утворяться при розпаді моноз, а також виявлені молочна, мурашина кислоти.
3. Окислення моносахаридів реактивом Фелінга
Реактиви: 1% розчин глюкози, 1% розчин фруктози, реактив Фелінга.
В одну пробірку помістити 1,0 мл розчину глюкози, у другу - стільки ж розчину фруктози. Потім у кожну пробірку додати рівний об'єм розчину Фелінга. Вміст пробірок перемішати і нагріти. Звернути увагу на появу жовто-червоного осадку CuO. Які вуглеводи визначаються цією реакцією?
4. Окислення моносахаридів аміачним розчином оксиду срібла (реакція срібного дзеркала)
Реактиви: аміачний розчин гідроксиду срібла, 1% розчин глюкози.
До 10 мл глюкози додати 1,0 мл аміачного розчину гідроксиду срібла. Нагріти. Спостерігати виділення або чорного осаду, або, якщо стінки пробірки були чисті, наліт срібла на стінках пробірки. (Під час нагрівання пробірку не можна струшувати, тому що срібло виділиться не на стінках пробірки, а у вигляді осаду).
При окисненні моносахаридів у лужному середовищі утвориться суміш продуктів в наслідок руйнації моносахарида. Але також утвориться в невеличкій кількості альдонова кислота (одноосновна). У даному випадку також утвориться глюконова кислота. Навести окислення глюкози до глюконової кислоти.
5.Реакція Селіванова на фруктозу
Реактиви: реактив Селіванова (розчин резорцину в розведеній соляній кислоті), 1% розчин фруктози, 5% розчин меду.
У пробірку внести декілька крапель реактиву Селіванова і додати 1,0 мл розчину фруктози. Нагріти до початку кипіння. Поступово рідина набуває червоне забарвлення, обумовлене утворенням оксиметилфурфуролу.
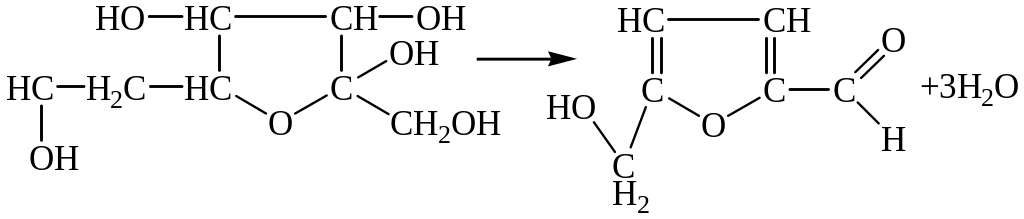
Такий же дослід проробити з розчином меду. Зробити висновок.
6. Доведення наявності гідроксогруп у моносахаридах і дисахаридах
Реактиви: 1% розчин глюкози і сахарози, 2н розчин NaOH, 0,2н розчин CuSO4 .
Одержати у двох пробірках блакитний осад гідроксиду міді, змішавши 0,5 мл сульфату міді з 1,0 мл гідроксиду натрію. До отриманого осаду долити надлишок розчину глюкози і сахарози. Вміст пробірок струснути. Чому відбувається розчинення осаду? Навести хімізм процесу.
7. Розпізнавання дисахаридів, що відновлюють ( редукують ) і не відновлюють ( не редукують)
Реактиви: 1% розчини сахарози , лактози і мальтози, реактив Фелінга.
У три пробірки наливають по 1,0 мл сахарози, мальтози і лактози. Потім у кожну пробірку додають у рівному об'ємі реактив Фелінга, нагрівають до початку кипіння. У якій із пробірок випадає червоно-жовтий осад міді (I)? Поясніть результати досліду. Поясніть хімізм взаємодії відповідного дисахариду з реактивом Фелінга.
8.Гідроліз сахарози
Реактиви: 1% розчин сахарози, 2н розчин HCl, розчин Фелінга, реактив Селіванова.
У пробірку налити 1 мл сахарози, декілька крапель розведеної соляної кислоти і прокип'ятити 4-5 хвилин. Частину отриманого розчину нейтралізувати розчином гідроксиду натрію до слаболужної реакції і додати розчин Фелінга. Нагріти. Чому виділяється червоно-жовтий осад оксиду міді (I)? До другої частини розчину долити реактив Селіванова, нагріти. Про що свідчить поява червоного забарвлення розчину? Навести рівняння гідролізу сахарози.
