
- •Термодинамика и теплопередача. Учебное пособие
- •Раздел I. Техническая термодинамика
- •Содержание
- •Раздел I
- •Тема 1. Газ, как рабочее тело термодинамических систем
- •Тема 2. Первый закон термодинамики
- •Тема 3. Термодинамические процессы
- •Тема 4. Второй закон термодинамики
- •Тема 5. Идеальные циклы тепловых двигателей
- •Основные условные обозначения
- •Основные сечения потока
- •Сокращения
- •Используемые индексы
- •Предисловие
- •Введение
- •Раздел I техническая термодинамика
- •Тема 1. Газ, как рабочее тело термодинамических систем
- •1.1. Структура основных понятий термодинамики авиационных гтд
- •1.2. Основные понятия и определения термодинамики
- •1.3. Реальный и идеальный газы. Параметры состояния рабочего тела
- •1.3.1. Давление
- •1.3.2. Температура
- •1.3.3. Удельный объём, плотность
- •1.4. Уравнение состояния идеального и реального газов
- •1.4.1. Уравнение состояния идеального газа
- •1.4.2. Уравнение состояния реального газа
- •1.5. Понятие о термодинамическом процессе. Равновесные (обратимые) и неравновесные (необратимые) процессы
- •1.5.1. Равновесные (обратимые) процессы
- •1.5.2. Графическое изображение термодинамического процесса
- •1.5.3. Неравновесные (необратимые) процессы
- •Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Проверьте, как Вы усвоили материал
- •Тема 2. Первый закон термодинамики
- •2.1. Внутренняя энергия рабочего тела. Изменение внутренней энергии
- •2.2. Работа газа, как форма передачи энергии в термодинамическом процессе
- •2.3. Теплота, как форма передачи энергии в термодинамическом процессе
- •2.4. Энтропия. Энтропийная “t-s” диаграмма
- •2.5. Зависимость количества работы и теплоты от характера термодинамического процесса
- •2.6. Теплоёмкость газа. Уравнение Майера. Показатель адиабаты
- •2.7. Энтальпия
- •2.8. Техническая работа (работа движущегося газа)
- •2.9. Содержание и уравнение первого закона термодинамики
- •2.10. Чистые вещества и смеси газов
- •Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Проверьте, как Вы усвоили материал
- •Тема 3. Термодинамические процессы
- •3.1. Последовательность и объём расчёта термодинамических процессов
- •3.2. Изохорный процесс: определение, осуществление и исследование
- •3.2.1. Исследование изохорного процесса
- •3.3. Изобарный процесс: определение, осуществление и исследование
- •3.3.1. Исследование изобарного процесса
- •3.4. Изотермический процесс: определение, осуществление, исследование
- •3.4.1. Исследование изотермического процесса
- •3.5. Адиабатный (изоэнтропический) процесс: определение, осуществление, исследование
- •3.5.1. Исследование адиабатного процесса
- •3.6. Сравнение адиабаты и изотермы
- •3.7. Обобщающее значение политропных процессов
- •3.8. Энтальпийная “I-s” диаграмма (“I-s” координаты)
- •Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Проверьте, как Вы усвоили материал
- •Тема 4. Второй закон термодинамики
- •4.1. Понятие о круговых процессах (циклах). Прямой цикл (цикл тепловой машины)
- •4.2. Полезная работа цикла. Термический кпд цикла
- •4.3. Цикл Карно и теорема Карно
- •4.4. Обратные циклы (циклы холодильных машин)
- •4.5. Второй закон термодинамики. Формулировки второго закона термодинамики
- •4.6. Второй закон термодинамики и энтропия
- •4.7. Статистическая интерпретация второго закона термодинамики
- •Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Информация к размышлению
- •Проверьте, как Вы усвоили материал
- •Тема 5. Идеальные циклы тепловых двигателей
- •5.1. Особенности термодинамического метода исследования циклов тепловых двигателей
- •5.2. Схема устройства и принцип работы авиационного газотурбинного двигателя (гтд)
- •5.3. Идеальный цикл гтд (цикл Брайтона – Стечкина)
- •5.4. Работа и термический кпд цикла гтд
- •5.6. Сравнение циклов Брайтона и Гемфри
- •5.7. Цикл с регенерацией тепла
- •5.8. Цикл со ступенчатым подводом тепла
- •5.9. Эксергетический метод термодинамического анализа
- •5.10. Идеальные циклы двигателей внутреннего сгорания (двс)
- •5.10.1. Идеальный цикл двс с подводом тепла
- •5.10.2. Идеальный цикл двс с подводом тепла при постоянном
- •5.10.3. Сравнение циклов Отто и Дизеля
- •5.10.4. Цикл двс со смешанным теплоподводом
- •Примеры решения задач
- •Решение
- •Решение
- •4. Эффективность цикла оцениваем по величине термического кпд цикла
- •Решение
- •Проверьте, как Вы усвоили материал
- •Заключение
- •Список использованной литературы
- •Приложение
- •Международная стандартная атмосфера (мса) гост 4401–81 (фрагмент)
- •Теплофизические величины
- •Соблюдайте гост 8.417 – 2002
2.5. Зависимость количества работы и теплоты от характера термодинамического процесса
Имея выражение для количества работы и теплоты через параметры состояния системы и их графическое представление в “p-υ” и “T-s” диаграммах, легко показать, что количества работы и теплоты зависят от характера процесса. Вне процесса понятия теплоты и работы не имеют смысла, так как обозначают не запас энергии, а лишь количества энергии, передаваемые в ходе процесса. Физически характер процесса зависит от соотношения между количествами работы и теплоты, которыми система обменивается с окружающей средой, изменяя свое состояние. Аналитически различие в характере процессов выражается различием между уравнениями разных процессов.
Из формул (2.15) и (2.19) видно, что для определения количества работы и теплоты (взятие интеграла) необходимо иметь характеристики процесса в виде уравнений p = f (υ) и T = f (s). Следовательно, количества работы и теплоты зависят от характера процесса.
Графически различие в характерах процессов выражается тем, что разные процессы изображаются различными кривыми в диаграммах состояния. А так как количество работы в “p-υ” диаграмме и количество теплоты в “T-s” диаграмме представляются в виде площадей под линиями процессов, то в этих диаграммах зависимость количеств работы и теплоты от характера процесса наиболее наглядна.
В самом деле, если система рассматривается в двух определенных состояниях, характеризующихся определенными значениями параметров и функций состояния, то на диаграммах (рис. 2.4., а и 2.5,а.) эти состояния изображаются точками 1 и 2. При этом на диаграмме нет никакой линии, связывающей точки 1 и 2, а, следовательно, и площади под ней – работы (и соответственно в “T-s” диаграмме – теплоты).
Если система, обмениваясь теплотой и работой с окружающей средой, переходит из состояния 1 в состояние 2, то это изменение выражается линией на диаграмме состояния, например линией 1–2 (см. рис. 2.4., б и 2.5,б.). В этом случае количества работы и теплоты выражаются в виде площадей соответственно на “p-υ” и “T-s” диаграммах, например, площадь а12б на рис. 2.4,б определяет работу в процессе 1–2, а площадь а12б на рис. 2.5,б – теплоту в том же процессе.
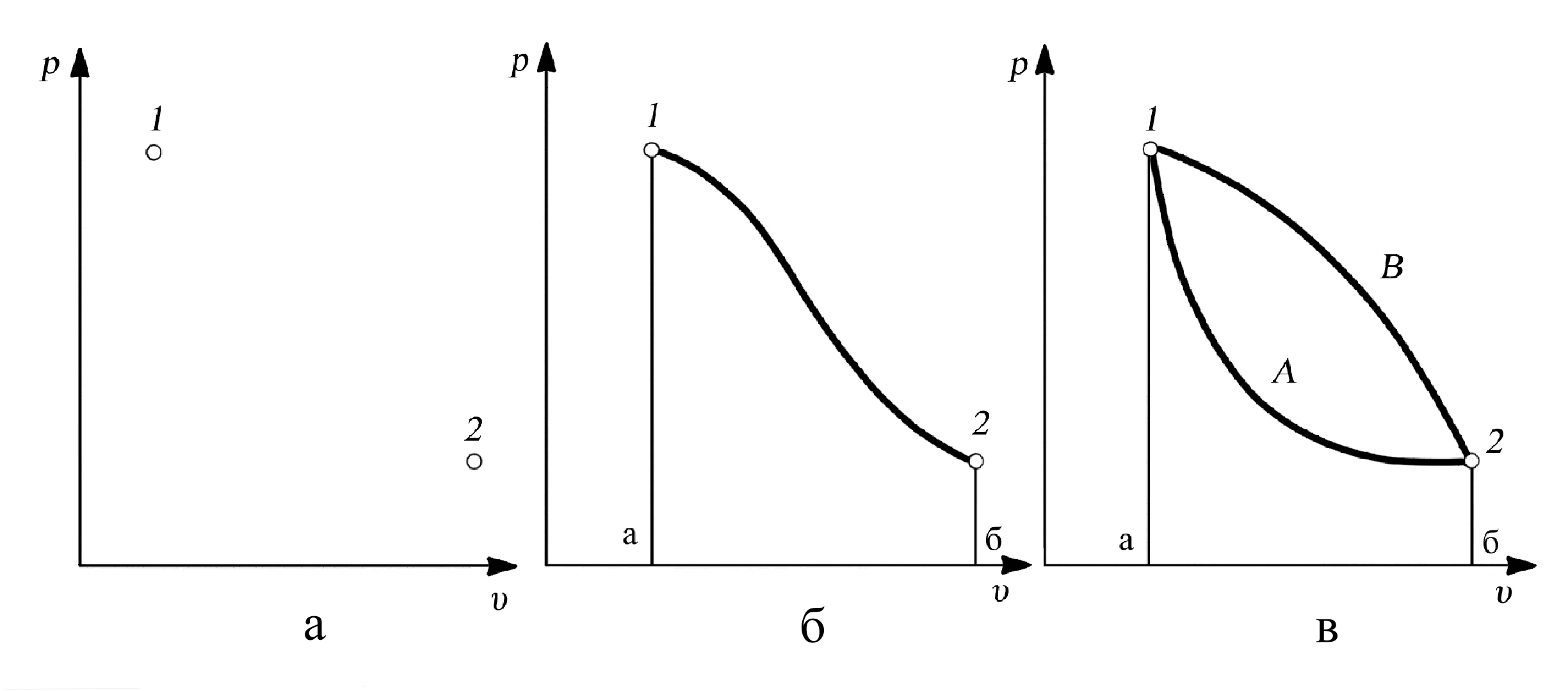
Рис. 2.4. Зависимость работы от характера процесса: а – знание начального и конечного состояний недостаточно для вычисления работы, б – при задании линии процесса работа выражается площадью под линией, в – при одинаковых начальных и конечных состояниях работа различна в различных процессах
Но характер изменения состояния системы между точками 1–2 может быть разным (линии 1А2 и 1В2 на рис. 2.4,в и 2.5,в), что, как уже отмечалось, зависит от соотношения между работой и теплотой при изменении состояния. Площади под линиями 1A2 и 1В2 оказываются различными, следовательно, различными будут и количества работы и теплоты в этих двух процессах. В примере, представленном на рис. 2.4,в,
L1A2
=
![]() <
L1B2
=
<
L1B2
=
![]()
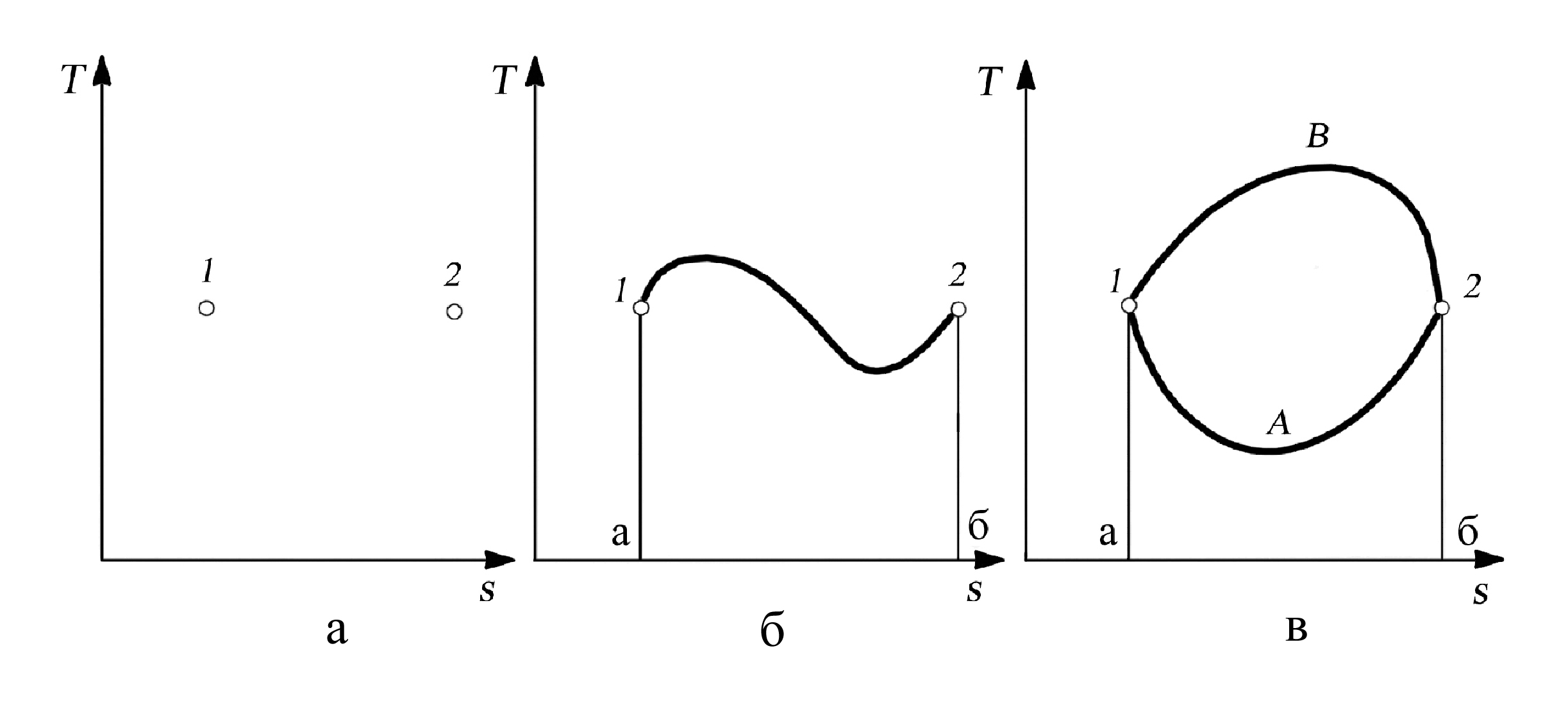
Рис. 2.5. Зависимость теплоты от характера процесса: а – знание начального и конечного состояний недостаточно для вычисления теплоты, б – при задании линии процесса теплота выражается площадью под линией, в – при одинаковых начальных и конечных состояниях теплота различна в различных процессах
В примере, представленном на рис. 2.5,в,
![]() q1A2
=
q1A2
=
![]() q1B2
=
q1B2
=
![]()
