
- •Термодинамика и теплопередача. Учебное пособие
- •Раздел I. Техническая термодинамика
- •Содержание
- •Раздел I
- •Тема 1. Газ, как рабочее тело термодинамических систем
- •Тема 2. Первый закон термодинамики
- •Тема 3. Термодинамические процессы
- •Тема 4. Второй закон термодинамики
- •Тема 5. Идеальные циклы тепловых двигателей
- •Основные условные обозначения
- •Основные сечения потока
- •Сокращения
- •Используемые индексы
- •Предисловие
- •Введение
- •Раздел I техническая термодинамика
- •Тема 1. Газ, как рабочее тело термодинамических систем
- •1.1. Структура основных понятий термодинамики авиационных гтд
- •1.2. Основные понятия и определения термодинамики
- •1.3. Реальный и идеальный газы. Параметры состояния рабочего тела
- •1.3.1. Давление
- •1.3.2. Температура
- •1.3.3. Удельный объём, плотность
- •1.4. Уравнение состояния идеального и реального газов
- •1.4.1. Уравнение состояния идеального газа
- •1.4.2. Уравнение состояния реального газа
- •1.5. Понятие о термодинамическом процессе. Равновесные (обратимые) и неравновесные (необратимые) процессы
- •1.5.1. Равновесные (обратимые) процессы
- •1.5.2. Графическое изображение термодинамического процесса
- •1.5.3. Неравновесные (необратимые) процессы
- •Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Проверьте, как Вы усвоили материал
- •Тема 2. Первый закон термодинамики
- •2.1. Внутренняя энергия рабочего тела. Изменение внутренней энергии
- •2.2. Работа газа, как форма передачи энергии в термодинамическом процессе
- •2.3. Теплота, как форма передачи энергии в термодинамическом процессе
- •2.4. Энтропия. Энтропийная “t-s” диаграмма
- •2.5. Зависимость количества работы и теплоты от характера термодинамического процесса
- •2.6. Теплоёмкость газа. Уравнение Майера. Показатель адиабаты
- •2.7. Энтальпия
- •2.8. Техническая работа (работа движущегося газа)
- •2.9. Содержание и уравнение первого закона термодинамики
- •2.10. Чистые вещества и смеси газов
- •Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Проверьте, как Вы усвоили материал
- •Тема 3. Термодинамические процессы
- •3.1. Последовательность и объём расчёта термодинамических процессов
- •3.2. Изохорный процесс: определение, осуществление и исследование
- •3.2.1. Исследование изохорного процесса
- •3.3. Изобарный процесс: определение, осуществление и исследование
- •3.3.1. Исследование изобарного процесса
- •3.4. Изотермический процесс: определение, осуществление, исследование
- •3.4.1. Исследование изотермического процесса
- •3.5. Адиабатный (изоэнтропический) процесс: определение, осуществление, исследование
- •3.5.1. Исследование адиабатного процесса
- •3.6. Сравнение адиабаты и изотермы
- •3.7. Обобщающее значение политропных процессов
- •3.8. Энтальпийная “I-s” диаграмма (“I-s” координаты)
- •Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Проверьте, как Вы усвоили материал
- •Тема 4. Второй закон термодинамики
- •4.1. Понятие о круговых процессах (циклах). Прямой цикл (цикл тепловой машины)
- •4.2. Полезная работа цикла. Термический кпд цикла
- •4.3. Цикл Карно и теорема Карно
- •4.4. Обратные циклы (циклы холодильных машин)
- •4.5. Второй закон термодинамики. Формулировки второго закона термодинамики
- •4.6. Второй закон термодинамики и энтропия
- •4.7. Статистическая интерпретация второго закона термодинамики
- •Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Информация к размышлению
- •Проверьте, как Вы усвоили материал
- •Тема 5. Идеальные циклы тепловых двигателей
- •5.1. Особенности термодинамического метода исследования циклов тепловых двигателей
- •5.2. Схема устройства и принцип работы авиационного газотурбинного двигателя (гтд)
- •5.3. Идеальный цикл гтд (цикл Брайтона – Стечкина)
- •5.4. Работа и термический кпд цикла гтд
- •5.6. Сравнение циклов Брайтона и Гемфри
- •5.7. Цикл с регенерацией тепла
- •5.8. Цикл со ступенчатым подводом тепла
- •5.9. Эксергетический метод термодинамического анализа
- •5.10. Идеальные циклы двигателей внутреннего сгорания (двс)
- •5.10.1. Идеальный цикл двс с подводом тепла
- •5.10.2. Идеальный цикл двс с подводом тепла при постоянном
- •5.10.3. Сравнение циклов Отто и Дизеля
- •5.10.4. Цикл двс со смешанным теплоподводом
- •Примеры решения задач
- •Решение
- •Решение
- •4. Эффективность цикла оцениваем по величине термического кпд цикла
- •Решение
- •Проверьте, как Вы усвоили материал
- •Заключение
- •Список использованной литературы
- •Приложение
- •Международная стандартная атмосфера (мса) гост 4401–81 (фрагмент)
- •Теплофизические величины
- •Соблюдайте гост 8.417 – 2002
2.2. Работа газа, как форма передачи энергии в термодинамическом процессе
При рассмотрении простейшей ТДС отмечалось, что процесс превращения теплоты в работу сопровождается обменом энергией между источниками теплоты, рабочим телом и источником работы. Существуют две формы передачи энергии между взаимодействующими телами – в форме теплоты и в форме работы.
Работа представляет собой часть внутренней энергии системы, передаваемой в термодинамическом процессе, т.е. она является формой обмена энергии. Она также является оценкой количественной величины передаваемой энергии. Из физики известно, что механическая работа производится только при наличии движения под действием механической силы. Без движения механической работы нет, следовательно, работа является формой передачи упорядоченного, организованного движения в одном направлении. В этом можно убедиться на примере совершения работы газом при его расширении. Частицы газа, находящиеся под поршнем в цилиндре, пребывают в непрерывном хаотическом, неупорядоченном движении.
Когда газ начинает перемещать поршень, т.е. совершать механическую работу, то на беспорядочное движение частиц газа накладывается организованное движение: все частицы наряду с хаотическим движением получают некоторое смещение в направлении движения поршня и совершают работу по перемещению поршня.
В термодинамике рассматривается только механическая работа. В количественном отношении механическая работа является мерой обмена механической формой движения, т.е. мерой энергии, передаваемой в механической форме.
Работа газа в технической термодинамике обозначается буквой L и измеряется в Джоулях, а удельная работа или работа 1 кг газа обозначаются буквой L и измеряется в Дж/кг.
Выведем формулу работы, совершаемую газом, для закрытой ТДС. Поместим 1 кг газа в цилиндр с подвижным поршнем и подведем к нему некоторое количество теплоты при условии, что давление газа в цилиндре постоянное и равно давлению внешних сил (рис. 2.1.) При подведении теплоты увеличится скорость хаотического движения молекул, что приведет к возрастанию давления и температуры газа. При этом сила, действующая на поршень изнутри цилиндра, станет больше силы внешней среды, в результате чего поршень переместится (вправо), т.е. газом будет совершена работа по перемещению поршня. Величина это работы L равна произведению силы Р = р·F на путь x:
т.е. L = p·F·x, но так как F·x = υ2 – υ1, имеем L = p·(υ2 – υ1) или L = p·Δ υ (2.13)
Т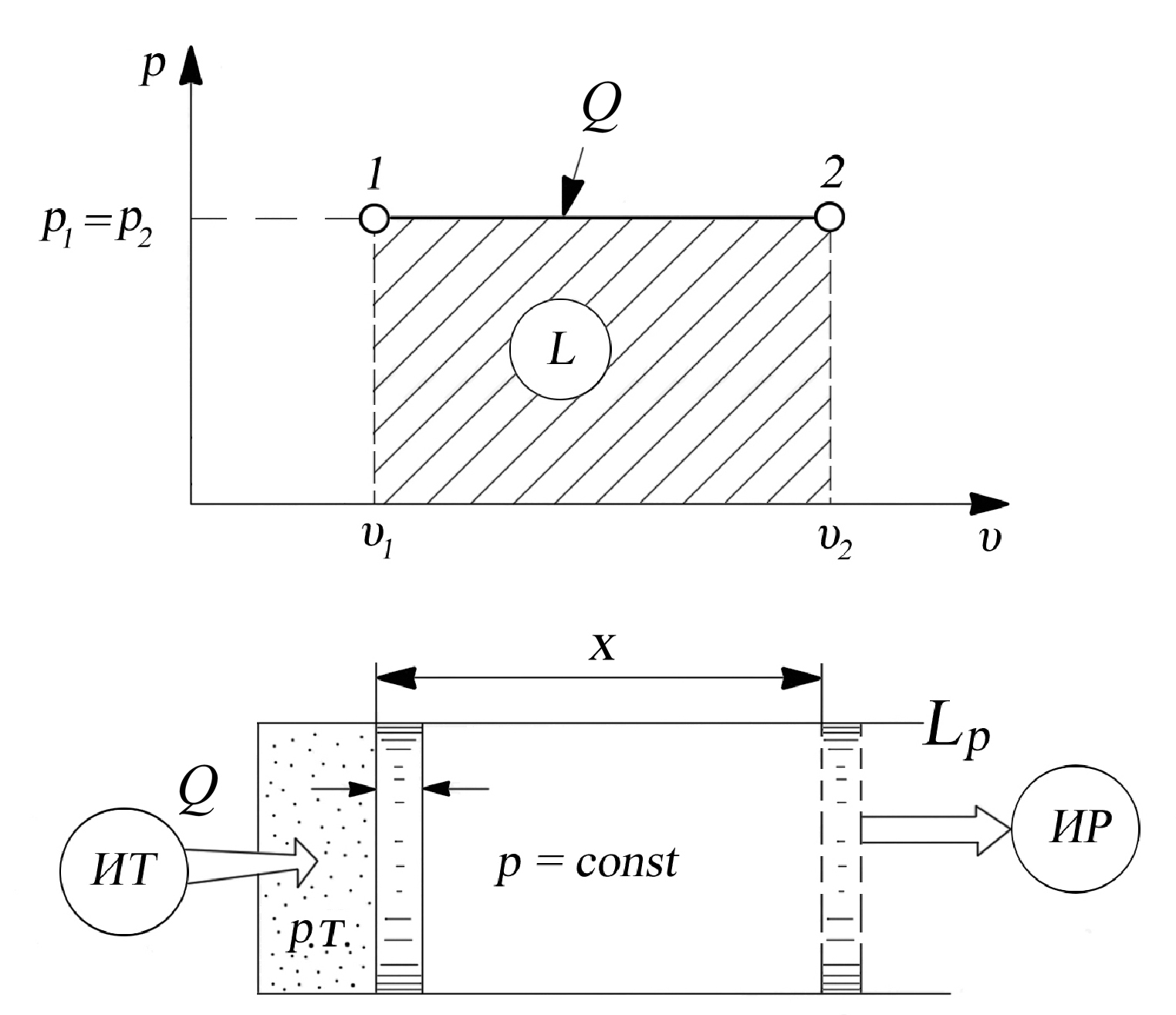 аким
образом, мы можем подсчитать работу,
зная параметры состояния рабочего тела.
Эта работа связана с изменением объёма,
поэтому она называется работой
расширения – сжатия
(деформации).
аким
образом, мы можем подсчитать работу,
зная параметры состояния рабочего тела.
Эта работа связана с изменением объёма,
поэтому она называется работой
расширения – сжатия
(деформации).
Рис. 2.1. К определению работы расширения–сжатия при p = const
Рассмотрим произвольный термодинамический процесс, в котором давление в течение всего процесса постоянно изменяется. Определим работу, совершаемую рабочим телом в произвольном термодинамическом процессе (рис. 2.2.).
Если подвести бесконечно малое количество теплоты dQ, произойдет бесконечно малое изменение объема dυ и будет получена элементарная работа dL, равная
dL = p·dυ (2.14)
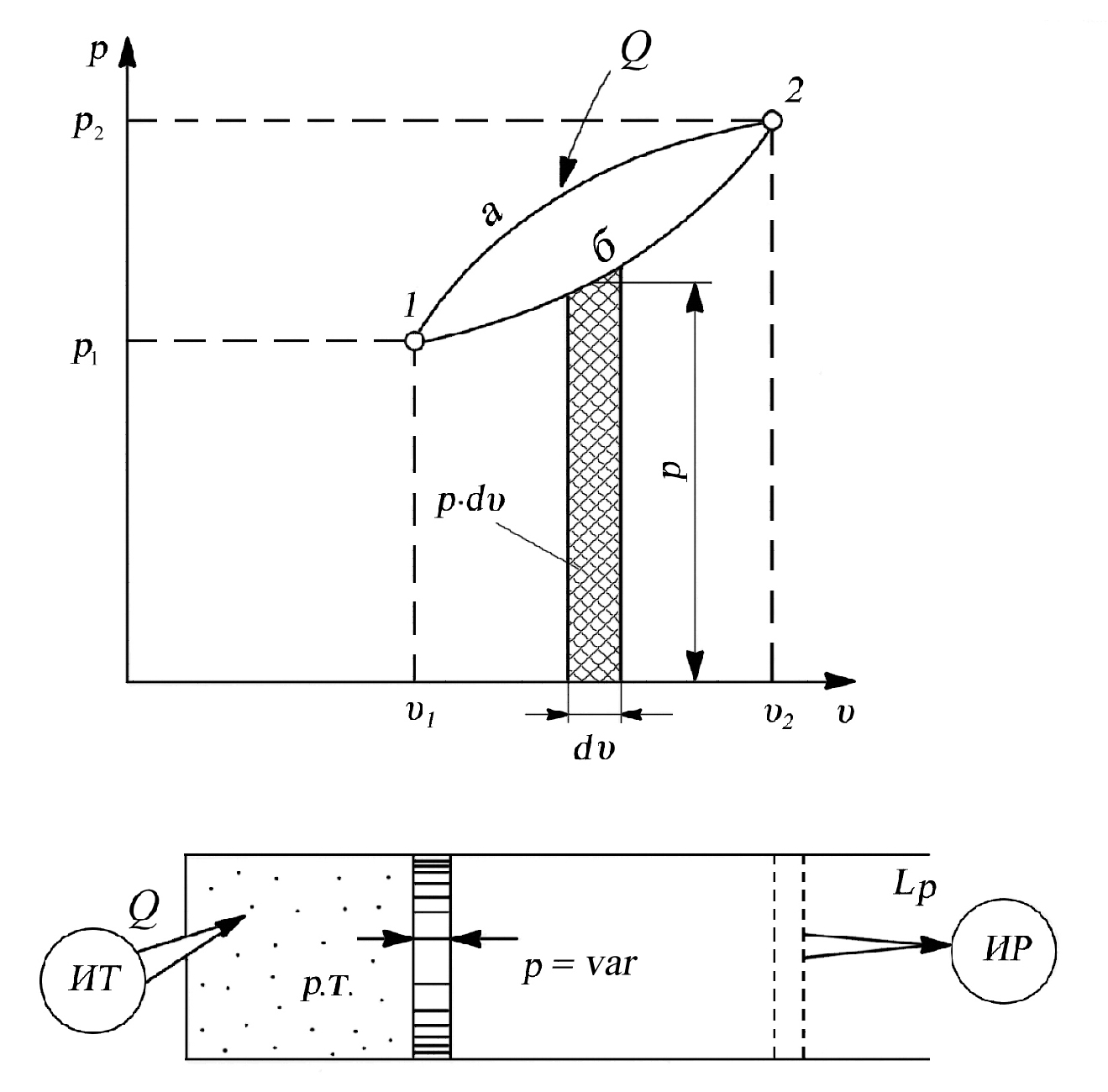
Рис. 2.2. К определению работы расширения при p = var
В общем случае давление в процессе не остается постоянным, поэтому работа в произвольном процессе 1–2 (рис. 2.2.) определяется по его формуле:
L1-2
=![]() =
= .
(2.15)
.
(2.15)
Для аналитического вычисления работы по уравнению (2.15) требуется знать закон изменения давления в данном процессе при изменении объёма, т.е. уравнение p = f (υ). Графическое изображение уравнения p = f (υ) называют рабочей диаграммой, так как она позволяет определить количество работы в рассматриваемом термодинамическом процессе.
Работа газа в любом
термодинамическом процессе в координатах
“р-υ“
изображается площадью, ограниченной
линией процесса и осью объёмов. Из
графического изображения работы (рис.
2.2.) видно, что ее величина зависит от
пути термодинамического процесса. Так,
в процессе, идущем по пути 1-а-2, работа
получается больше, чем в процессе, идущем
по пути 1-б-2 (рис. 2.2.). Действительно,
площадь υ11а2υ2
больше площади υ11б2υ2,
таким образом
![]() >
>
![]() .
.
Работа в уравнении (2.15) выражена через параметры p и υ, каждый из которых по-своему характеризует обмен механической энергией. Изменение объёма, т.е. механическое перемещение границ системы, является признаком передачи механической энергии. Величина давления в системе определяет возможность обмена механической работой: расширение (или сжатие) газа возможно только в том случае, когда давление в системе отличаются от давления в окружающей среде.
Таким образом, абсолютное давление характеризует с количественной стороны причину, вызывающую обмен механической энергией, т.е. обмен работой.
В термодинамике принято считать количество механической работы положительным, когда работа совершается термодинамической системой над окружающей средой. Применительно к газу, как рабочему телу, работа расширения газа принято считать положительной, а работа сжатия газа – отрицательной.
