
- •Практическое руководство по химии почв
- •Введение
- •Раздел I. Валовой анализ
- •1.1. Способы разложения почв
- •1.1.1. Разложение почв кислотами.
- •1.1.2. Разложение почв сплавлением.
- •1.1.3. Разложение почвы спеканием.
- •1.2. Определение гигроскопической влажности
- •1.3. Определение потери при прокаливании
- •1.4. Спекание почвы с содой
- •1.5. Анализ элементного состава почв
- •1.5.1. Определение кремния желатиновым методом
- •Пример расчета. Для спекания взято 1,0224 г прокаленной почвы. Прокаленный осадок SiO2 весит 0,8014 г. Содержание SiO2 равно:
- •1.5.2. Определение полуторных оксидов гравиметрическим методом
- •1.5.3. Определение железа фотометрическим методом
- •1.5.4. Определение алюминия фотометрическим методом
- •1.5.5.Вычисленное содержание алюминия по разности
- •1.5.6. Определение кальция и магния комплексонометрическим методом
- •1.5.6.1. Определение кальция
- •1.5.6.2. Определение суммы кальция и магния
- •1.5.7. Пероксидный метод определения титана
- •1.5.8. Определение фосфора фотометрическим методом
- •1.6. Способы выражения результатов валового анализа
- •1.7. Пересчеты данных валового анализа
- •1.8. Использование данных валового анализа
- •1.8.1. Использование элементного состава для суждения о генезисе почв.
- •1.8.2. Использование элементного состава для оценки потенциального плодородия почвы.
- •1.8.3. Использование данных элементного состава для расчета молекулярных отношений
- •1.8.4. Использование данных элементного состава для расчета запасов химических элементов
- •Пример расчета. Найти запас SiO2 в т/га если его содержание равно 80,63 %, плотность сложения почвы 1,18 г/см3, мощность слоя 9 см.
- •1.8.5. Использование данных элементного состава при изучении биологического круговорота веществ
- •1.8.6. Использование данных элементного состава для
- •1.8.6.1. Метод прямого сравнения
- •1.8.6.2. Методы стабильного компонента
- •1.8.6.2.1. Метод молекулярных отношений
- •1.8.6.2.2. Метод элювиально-аккумулятивных (еа) коэффициентов
- •1.8.6.2.3. Метод баланса веществ
- •1.8.7. Использование данных элементного состава для диагностики минералов илистой фракции.
- •Контрольные вопросы
- •Литература
- •Раздел II. Ионно-солевой комплекс почв
- •2.1. Метод водной вытяжки
- •2.1.1. Влияние солей на сельскохозяйственные культуры
- •2.1.2. Достоинства и недостатки водной вытяжки как метода изучения засоленных почв
- •2.1.3 Анализ водной вытяжки
- •2.1.3.1. Определение величины рН водной вытяжки
- •2.1.3.2. Определение величины сухого остатка
- •2.1.3.3. Определение величины прокаленного остатка
- •2.1.3.4. Определение щелочности от растворимых карбонатов
- •2.1.3.5. Определение общей щелочности
- •2.1.3.6. Определение хлорид-ионов
- •2.1.3.7. Определение сульфат-ионов
- •2.1.3.8. Определение ионов кальция и магния комплексонометрическим методом
- •2.1.3.8.1. Определение кальция
- •2.1.3.8.2. Определение суммы кальция и магния
- •2.1.3.9. Определение натрия и калия
- •2.1.3.9.1. Определение натрия и калия методом фотометрии пламени
- •2.1.3.9.2. Определение содержания натрия и калия по разности
- •Форма 4. Данные анализа водной вытяжки
- •2.1.4. Интерпретация данных водной вытяжки
- •2.1.4.1. Характеристика солевого режима почв по величине сухого остатка
- •2.1.4.2. Оценка химизма (типа) засоления почв.
- •2.1.4.2.1. Общие принципы оценки химизма засоления почв
- •2.1.4.2.2. Оценка степени засоления почв по содержанию токсичных ионов
- •2.1.4.2.3. Оценка степени засоления почв по «суммарному эффекту» токсичных ионов
- •2.1.5. Расчет промывной нормы
- •2.2. Катионообменная способность почв
- •2.2.1. Общие представления о катионообменной
- •2.2.2. Методы определения катионообменной способности почв
- •2.2.2.1. Оценка эффективной емкости катионного обмена
- •2.2.2.2. Определение стандартной емкости катионного обмена по Бобко-Аскинази в модификации цинао
- •2.2.2.3. Определение суммы обменных оснований методом Каппена-Гильковица
- •2.2.2.4. Определение гидролитической кислотности
- •2.2.2.5. Определение обменных катионов по методу Пфеффера в модификации в.А. Молодцова и и.В. Игнатовой
- •2.2.2.5.1. Определение кальция комплексонометрическим методом
- •2.2.2.5.2. Определение суммы кальция и магния комплексонометрическим методом
- •2.2.2.5.3. Определение натрия и калия методом фотометрии пламени
- •2.2.3. Использование результатов определения катионообменной способности почв
- •2.2.3.1. Вычисление степени насыщенности почв основаниями
- •2.2.3.2. Расчет дозы извести
- •2.2.3.3. Вычисление степени солонцеватости почв
- •2.2.3.4. Расчет дозы гипса
- •Контрольные вопросы
- •Литература
- •Раздел III. Органическое вещество почвы
- •3.1. Подготовка почвы для определения содержания и состава гумуса
- •3.2. Методы определения содержания общего гумуса почвы
- •3.2.1. Прямые методы определения содержания углерода органических соединений (гумуса) почвы.
- •3.2.2. Косвенные методы определения содержания углерода органических соединений (гумуса) почвы
- •3.2.2.1. Определение гумуса методом и.В.Тюрина в модификации в.Н.Симакова
- •3.2.2.2. Другие модификации метода и.В. Тюрина.
- •3.2.2.2.1. Спектрофотометрический метод определения содержания гумуса (д.С. Орлов, н.М. Гриндель)
- •3.2.2.2.2. Определение содержания органического углерода почвы методом и.В.Тюрина в модификации б.А.Никитина.
- •3.3. Методы определения общего содержания азота почвы.
- •3.3.1. Определение общего содержания азота методом Кьельдаля.
- •3.3.2. Определение общего содержания азота микрохромовым методом и.В. Тюрина.
- •3.4. Использование данных по содержанию общего гумуса и азота
- •3.4.1. Расчет отношения c:n
- •3.4.2. Вычисление запасов гумуса, углерода и азота.
- •3.5. Методы определение группового и фракционного состава гумуса.
- •3.5.1. Определение группового и фракционного состава гумуса по методу и.В. Тюрина в модификации в.В.Пономаревой и т.А.Плотниковой
- •3.5.2. Определение группового и фракционного состава гумуса по модифицированной схеме в.В.Пономаревой и т.А. Плотниковой (т.А. Плотникова, н.Е. Орлова, 1984).
- •Ход анализа
- •3.5.3. Ускоренный пирофосфатный метод определения состава гумуса по м.М. Кононовой и н.П. Бельчиковой
- •3.6. Методы изучения некоторых свойств гумусовых кислот при анализе фракционно-группового состава гумуса
- •3.6.1. Определение порога коагуляции гуминовых кислот.
- •3.6.2. Оптические свойства гумусовых веществ.
- •3.6.2.1. Электронные спектры поглощения гумусовых веществ
- •3.6.2.2. Определение коэффициента цветности q4/6
- •3.6.3. Гель-хроматография гумусовых веществ
- •3.7. Показатели гумусового состояния почв
- •Продолжение таблицы 31
- •3.8. Методы определения содержания и состава органического вещества в болотных торфяных почвах.
- •3.8.1. Определение потери при прокаливании и зольности торфа.
- •3.8.2. Одновременное определение общего содержания углерода и азота в торфяных почвах методом Анстета в модификации в.В. Пономаревой и т. А. Николаевой
- •Вычисление результатов анализа
- •Для анализа используют следующие реактивы:
- •3.8.3. Определение общего содержания азота в растительных материалах (торфах, лесных подстилках и пр.) методом к.Е. Гинзбурга и г.М. Щегловой
- •3.8.4. Определение содержания органического азота в вытяжках из торфов микрохромовым методом и.В. Тюрина
- •3.8.5. Определение состава органического вещества торфяно-болотных почв по методу в.В. Пономаревой и т.А. Николаевой.
- •Контрольные вопросы
- •Литература
- •Раздел I. Валовой анализ ……………………………………
- •Раздел II. Ионно-солевой комплекс почв ……………………
- •Раздел III. Органическое вещество почв
3.6.2. Оптические свойства гумусовых веществ.
Оригинальные исследования М.М. Кононовой и Н.П. Бельчиковой (1961) показали четкую зависимость между оптическими характеристиками гумусовых кислот, их свойствами и условиями образования.
Гумусовые вещества активно взаимодействуют с электромагнитными колебаниями, образуя спектры поглощения в широком диапазоне длин волн. Наиболее хорошо изучены спектры поглощения гумусовых кислот в интервале 220-750 нм – электронные спектры поглощения и в интервале 2-25 мкм – молекулярные спектры.
3.6.2.1. Электронные спектры поглощения гумусовых веществ
Электронные спектры характеризуют поглощение электромагнитных колебаний в ультрафиолетовом и видимом диапазонах. При изучении органического вещества почвы их используют: 1) для сравнительной характеристики гумусовых веществ и их фракций; 2) для изучения строения и свойств гуминовых кислот и фульвокислот; 3) для идентификации и количественного определения отдельных компонентов органической природы присутствующих в щелочных и спиртобензольных экстрактах из почв (хлорофилл, липиды, пигмент Рg) и других целей.
Обычно снимают электронные спектры поглощения растворов гуминовых кислот или фульвокислот полученных при растворении в 0,1 н. NaOH специально выделенных препаратов. Однако целесообразно проводить съемку спектров поглощения и тех растворов гуминовых кислот и фульвокислот, которые получаются при анализе группового и фракционного состава гумуса.
Для получения сравнимых и наглядных результатов М.М. Кононова рекомендует исследуемые растворы доводить до одинаковой концентрации по углероду – 0,136 г/л. Эта концентрация выбрана условно, можно использовать любую иную концентрацию растворов гумусовых веществ. Главное чтобы сравниваемые растворы были выровнены по содержанию в них углерода. Если были сняты спектры растворов с разной концентрацией углерода то найденные значения оптических плотностей приводят к стандартной концентрации по углероду по формуле:
![]()
где Dо – оптическая плотность раствора при концентрации углерода выбранной в качестве стандартной Dх – измеренная оптическая плотность раствора с концентрацией углерода Сх; Со – концентрация углерода в растворе выбранная в качестве стандартной, г/л; Сх – концентрация углерода в растворе при которой проводилось определение оптической плотности Dх, г/л.
Следует учесть, что растворы фульвокислот получаемые при анализе качественного состава гумуса имеют сильнокислую реакцию среды. В сильнокислой и кислой среде интенсивность окраски фульвокислот сильно уменьшается. Для получения сравнимых результатов реакцию среды доводят до рН = 12. В этой области окраска фульвокислот мало зависит от рН, а условия съемки спектров Гк и Фк оказываются одинаковыми.
Ход анализа. После приведения анализируемых растворов к стандартным условиям (концентрация углерода, реакция среды) измеряют величину оптической плотности при различных длинах волн. По полученным значениям оптических плотностей строят графики электронных спектров поглощения. На графике отображают изменение величины D раствора гумусовой кислоты (ось ординат) в зависимости от длины волны (λ) в нм (ось абсцисс). Наиболее точные результаты получают при использовании спектрофотометров с автоматической записью спектра.
Обычно электронные спектры поглощения гумусовых кислот в широком диапазоне длин волн от 240-260 до 750 нм не имеют четко выраженных полос или максимумов поглощения. В координатах D – λ спектры выглядят, как пологие кривые с постепенным уменьшением оптической плотности по мере увеличения длины волны (рис. 5).
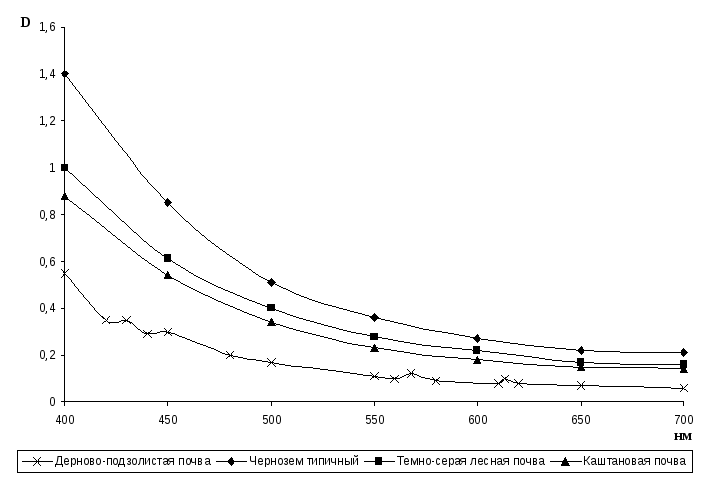
Рис. 5. Электронные спектры поглощения гуматов натрия
В связи с этим, при характеристике электронных спектров поглощения часто ограничиваются только видимой областью – от 400 до 750 нм, поскольку в ультрафиолетовой части спектра получают практически идентичную информацию. На спектрах гумусовых веществ некоторых типов почв (дерново-подзолистые, бурые лесные, луговые) часто обнаруживаются две пары максимумов при 420-425, 450-460 нм и 570-580, 615-620 нм, принадлежащие своеобразному зеленому пигменту, первоначально названному «зеленой гуминовой кислотой». В настоящее время он обозначается символом Рg. Содержание его в почвах иногда бывает столь значительно, что щелочная вытяжка имеет ясно выраженный зеленоватый оттенок. Обычно фракция Рg встречается в почвах, испытывающих повышенное увлажнение, хотя бы временное.
