
- •Практическое руководство по химии почв
- •Введение
- •Раздел I. Валовой анализ
- •1.1. Способы разложения почв
- •1.1.1. Разложение почв кислотами.
- •1.1.2. Разложение почв сплавлением.
- •1.1.3. Разложение почвы спеканием.
- •1.2. Определение гигроскопической влажности
- •1.3. Определение потери при прокаливании
- •1.4. Спекание почвы с содой
- •1.5. Анализ элементного состава почв
- •1.5.1. Определение кремния желатиновым методом
- •Пример расчета. Для спекания взято 1,0224 г прокаленной почвы. Прокаленный осадок SiO2 весит 0,8014 г. Содержание SiO2 равно:
- •1.5.2. Определение полуторных оксидов гравиметрическим методом
- •1.5.3. Определение железа фотометрическим методом
- •1.5.4. Определение алюминия фотометрическим методом
- •1.5.5.Вычисленное содержание алюминия по разности
- •1.5.6. Определение кальция и магния комплексонометрическим методом
- •1.5.6.1. Определение кальция
- •1.5.6.2. Определение суммы кальция и магния
- •1.5.7. Пероксидный метод определения титана
- •1.5.8. Определение фосфора фотометрическим методом
- •1.6. Способы выражения результатов валового анализа
- •1.7. Пересчеты данных валового анализа
- •1.8. Использование данных валового анализа
- •1.8.1. Использование элементного состава для суждения о генезисе почв.
- •1.8.2. Использование элементного состава для оценки потенциального плодородия почвы.
- •1.8.3. Использование данных элементного состава для расчета молекулярных отношений
- •1.8.4. Использование данных элементного состава для расчета запасов химических элементов
- •Пример расчета. Найти запас SiO2 в т/га если его содержание равно 80,63 %, плотность сложения почвы 1,18 г/см3, мощность слоя 9 см.
- •1.8.5. Использование данных элементного состава при изучении биологического круговорота веществ
- •1.8.6. Использование данных элементного состава для
- •1.8.6.1. Метод прямого сравнения
- •1.8.6.2. Методы стабильного компонента
- •1.8.6.2.1. Метод молекулярных отношений
- •1.8.6.2.2. Метод элювиально-аккумулятивных (еа) коэффициентов
- •1.8.6.2.3. Метод баланса веществ
- •1.8.7. Использование данных элементного состава для диагностики минералов илистой фракции.
- •Контрольные вопросы
- •Литература
- •Раздел II. Ионно-солевой комплекс почв
- •2.1. Метод водной вытяжки
- •2.1.1. Влияние солей на сельскохозяйственные культуры
- •2.1.2. Достоинства и недостатки водной вытяжки как метода изучения засоленных почв
- •2.1.3 Анализ водной вытяжки
- •2.1.3.1. Определение величины рН водной вытяжки
- •2.1.3.2. Определение величины сухого остатка
- •2.1.3.3. Определение величины прокаленного остатка
- •2.1.3.4. Определение щелочности от растворимых карбонатов
- •2.1.3.5. Определение общей щелочности
- •2.1.3.6. Определение хлорид-ионов
- •2.1.3.7. Определение сульфат-ионов
- •2.1.3.8. Определение ионов кальция и магния комплексонометрическим методом
- •2.1.3.8.1. Определение кальция
- •2.1.3.8.2. Определение суммы кальция и магния
- •2.1.3.9. Определение натрия и калия
- •2.1.3.9.1. Определение натрия и калия методом фотометрии пламени
- •2.1.3.9.2. Определение содержания натрия и калия по разности
- •Форма 4. Данные анализа водной вытяжки
- •2.1.4. Интерпретация данных водной вытяжки
- •2.1.4.1. Характеристика солевого режима почв по величине сухого остатка
- •2.1.4.2. Оценка химизма (типа) засоления почв.
- •2.1.4.2.1. Общие принципы оценки химизма засоления почв
- •2.1.4.2.2. Оценка степени засоления почв по содержанию токсичных ионов
- •2.1.4.2.3. Оценка степени засоления почв по «суммарному эффекту» токсичных ионов
- •2.1.5. Расчет промывной нормы
- •2.2. Катионообменная способность почв
- •2.2.1. Общие представления о катионообменной
- •2.2.2. Методы определения катионообменной способности почв
- •2.2.2.1. Оценка эффективной емкости катионного обмена
- •2.2.2.2. Определение стандартной емкости катионного обмена по Бобко-Аскинази в модификации цинао
- •2.2.2.3. Определение суммы обменных оснований методом Каппена-Гильковица
- •2.2.2.4. Определение гидролитической кислотности
- •2.2.2.5. Определение обменных катионов по методу Пфеффера в модификации в.А. Молодцова и и.В. Игнатовой
- •2.2.2.5.1. Определение кальция комплексонометрическим методом
- •2.2.2.5.2. Определение суммы кальция и магния комплексонометрическим методом
- •2.2.2.5.3. Определение натрия и калия методом фотометрии пламени
- •2.2.3. Использование результатов определения катионообменной способности почв
- •2.2.3.1. Вычисление степени насыщенности почв основаниями
- •2.2.3.2. Расчет дозы извести
- •2.2.3.3. Вычисление степени солонцеватости почв
- •2.2.3.4. Расчет дозы гипса
- •Контрольные вопросы
- •Литература
- •Раздел III. Органическое вещество почвы
- •3.1. Подготовка почвы для определения содержания и состава гумуса
- •3.2. Методы определения содержания общего гумуса почвы
- •3.2.1. Прямые методы определения содержания углерода органических соединений (гумуса) почвы.
- •3.2.2. Косвенные методы определения содержания углерода органических соединений (гумуса) почвы
- •3.2.2.1. Определение гумуса методом и.В.Тюрина в модификации в.Н.Симакова
- •3.2.2.2. Другие модификации метода и.В. Тюрина.
- •3.2.2.2.1. Спектрофотометрический метод определения содержания гумуса (д.С. Орлов, н.М. Гриндель)
- •3.2.2.2.2. Определение содержания органического углерода почвы методом и.В.Тюрина в модификации б.А.Никитина.
- •3.3. Методы определения общего содержания азота почвы.
- •3.3.1. Определение общего содержания азота методом Кьельдаля.
- •3.3.2. Определение общего содержания азота микрохромовым методом и.В. Тюрина.
- •3.4. Использование данных по содержанию общего гумуса и азота
- •3.4.1. Расчет отношения c:n
- •3.4.2. Вычисление запасов гумуса, углерода и азота.
- •3.5. Методы определение группового и фракционного состава гумуса.
- •3.5.1. Определение группового и фракционного состава гумуса по методу и.В. Тюрина в модификации в.В.Пономаревой и т.А.Плотниковой
- •3.5.2. Определение группового и фракционного состава гумуса по модифицированной схеме в.В.Пономаревой и т.А. Плотниковой (т.А. Плотникова, н.Е. Орлова, 1984).
- •Ход анализа
- •3.5.3. Ускоренный пирофосфатный метод определения состава гумуса по м.М. Кононовой и н.П. Бельчиковой
- •3.6. Методы изучения некоторых свойств гумусовых кислот при анализе фракционно-группового состава гумуса
- •3.6.1. Определение порога коагуляции гуминовых кислот.
- •3.6.2. Оптические свойства гумусовых веществ.
- •3.6.2.1. Электронные спектры поглощения гумусовых веществ
- •3.6.2.2. Определение коэффициента цветности q4/6
- •3.6.3. Гель-хроматография гумусовых веществ
- •3.7. Показатели гумусового состояния почв
- •Продолжение таблицы 31
- •3.8. Методы определения содержания и состава органического вещества в болотных торфяных почвах.
- •3.8.1. Определение потери при прокаливании и зольности торфа.
- •3.8.2. Одновременное определение общего содержания углерода и азота в торфяных почвах методом Анстета в модификации в.В. Пономаревой и т. А. Николаевой
- •Вычисление результатов анализа
- •Для анализа используют следующие реактивы:
- •3.8.3. Определение общего содержания азота в растительных материалах (торфах, лесных подстилках и пр.) методом к.Е. Гинзбурга и г.М. Щегловой
- •3.8.4. Определение содержания органического азота в вытяжках из торфов микрохромовым методом и.В. Тюрина
- •3.8.5. Определение состава органического вещества торфяно-болотных почв по методу в.В. Пономаревой и т.А. Николаевой.
- •Контрольные вопросы
- •Литература
- •Раздел I. Валовой анализ ……………………………………
- •Раздел II. Ионно-солевой комплекс почв ……………………
- •Раздел III. Органическое вещество почв
2.2.2.3. Определение суммы обменных оснований методом Каппена-Гильковица
Метод основан на вытеснении обменных оснований ионом водорода 0,1 н раствора НСl по схеме:
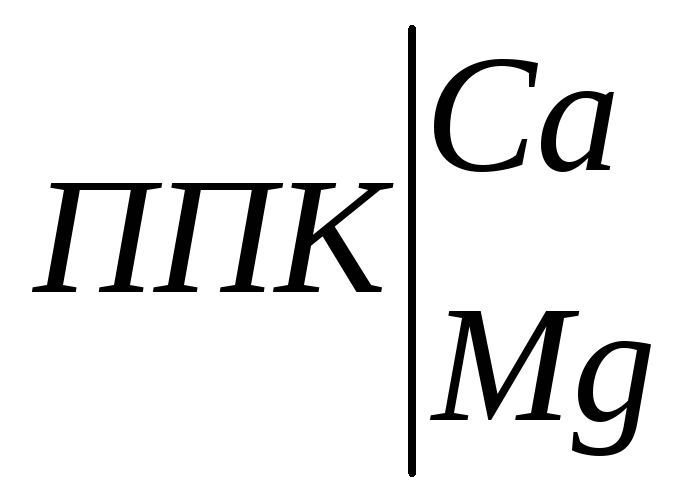 + 4НСl
+ 4НСl
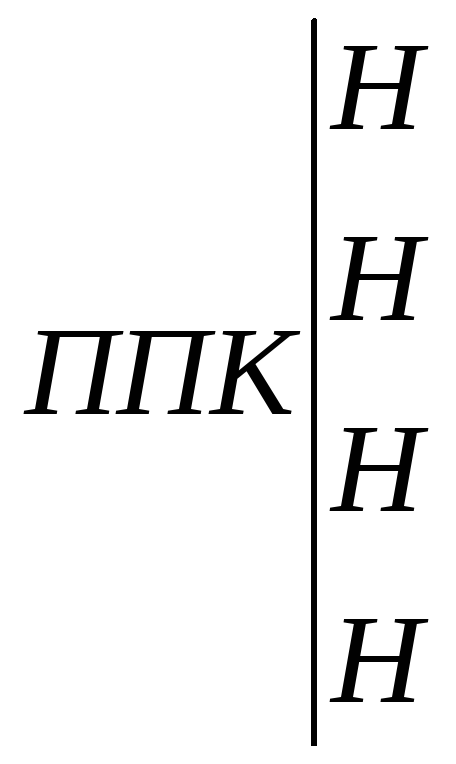 + СаСl2
+ MgCl2
+ СаСl2
+ MgCl2
Количество перешедших в раствор обменных оснований определяют по разности между содержанием Н+ в растворе до, и после взаимодействия кислоты с почвой. Однако следует учитывать, что часть кислоты расходуется на побочные реакции и при однократной обработке почвы кислотой вытесняются не все обменные основания. Поэтому для подзолистых и дерново-подзолистых почв обычно получаются завышенные результаты, а для черноземов – заниженные.
Ход анализа. 1. Взвешивают на технохимических весах 20 г воздушно-сухой почвы, просеянной через сито с отверстиями диаметром 1 мм. 2. Почву высыпают в колбу на 350-500 мл. 3. Из бюретки приливают 100 мл 0,1 н. раствора НС1, взбалтывают 1 ч на ротаторе и оставляют на сутки. 4. Вытяжку фильтруют через сухой беззольный фильтр. Если первые порции фильтрата окажутся мутными, то их снова выливают на тот же фильтр, а колбу ополаскивают дистиллированной водой. 5. Пипеткой отбирают 25-50 мл прозрачного фильтрата в коническую колбу на 150-200 мл, прибавляют 2-3 капли фенолфталеина, кипятят 1-2 мин, для удаления СО2 и титруют 0,1 н. раствором NаОН до слабо-розовой окраски не исчезающей в течение 1 мин.
Сумму обменных оснований вычисляют по формуле:
![]() ,
,
где S – сумма обменных оснований, мг-экв. на 100 г почвы; V1 – количество фильтрата HCl, взятого для титрования, мл; н1 – нормальность НСl; V2 – количество раствора NaOH, пошедшего на титрование взятого объема фильтрата, мл; н2 – нормальность NaOH; 100 – коэффициент пересчета на 100 г почвы; V0 – общий объем фильтрата, мл; m – навеска почвы, г; КН2О – коэффициент гигроскопичности.
Если сумма обменных оснований в почве ожидается больше 15 мг-экв., то соляной кислоты берут 200 мл или уменьшают навеску почвы до 10 г. Обычно руководствуются следующими придержками: для анализа дерново-подзолистых и светло-серых лесных почв берут 20 г почвы и 100 мл HCl, для анализа серых, темно-серых лесных почв и черноземов – 20 г почвы и 200 мл НС1.
Пример расчета. К навеске почвы равной 20,0 г прилито 100 мл 0,108 н. раствора НСl. После взаимодействия почвы с кислотой вытяжка отфильтрована. На титрование 50 мл фильтрата пошло 40 мл 0,106 н. NaOH. Коэффициент гигроскопичности равен 1,05.
![]() = 12,2 мг-экв/100 г
почвы.
= 12,2 мг-экв/100 г
почвы.
2.2.2.4. Определение гидролитической кислотности
Определение гидролитической кислотности основано на том, что при взаимодействии раствора СН3СОONa с почвой образуется уксусная кислота, которая оттитровывается щелочью. По количеству щелочи, пошедшей на титрование, и судят о величине гидролитической кислотности.
Ход анализа. 1. На технохимических весах отвешивают 20 г воздушно-сухой почвы, просеянной через сито с диаметром отверстий 1 мм, и высыпают в колбу на 200 мл.
2. К почве приливают 50 мл 1,0 н. раствора СН3СОONa и взбалтывают содержимое колбы в течение 1 ч. Часовое взбалтывание можно заменить пятиминутным взбалтыванием рукой с последующим отстаиванием суспензии в течение суток.
3. Суспензию отфильтровывают через сухой складчатый фильтр. Перед фильтрованием жидкость хорошо взбалтывают, чтобы перенести почву на фильтр. Если фильтрат окажется мутным, его следует снова профильтровать через тот же фильтр.
4. Отбирают пипеткой 25 мл прозрачного фильтрата и переносят в коническую колбу на 100 мл.
Прибавляют 1-2 капли фенолфталеина и титруют фильтрат 0,1 н. раствором NaОН до слабо-розовой окраски, не исчезающей в течение 1 мин.
Гидролитическую кислотность вычисляют по формуле:
г![]() деНГ
–
гидролитическая кислотность, мг-экв.
на 100 г почвы; V1
– количество раствора NaОН,
пошедшего на титрование взятого объема
фильтрата, мл; н. – нормальность NaOH;
100 – коэффициент пересчета на 100 г почвы;
V0
–общий объем фильтрата, мл; V2
– объем фильтрата, взятого для титрования,
мл; 1,75 – поправка на полноту вытеснения
ионов водорода; m
– навеска почвы, г.
деНГ
–
гидролитическая кислотность, мг-экв.
на 100 г почвы; V1
– количество раствора NaОН,
пошедшего на титрование взятого объема
фильтрата, мл; н. – нормальность NaOH;
100 – коэффициент пересчета на 100 г почвы;
V0
–общий объем фильтрата, мл; V2
– объем фильтрата, взятого для титрования,
мл; 1,75 – поправка на полноту вытеснения
ионов водорода; m
– навеска почвы, г.
Пример расчета. Для определения величины гидролитической кислотности к навеске воздушно-сухой почвы массой 20,0 г прилито 50 мл 1,0 н. раствора СН3СООNa. После того как суспензия была отфильтрована, взято 25 мл фильтрата, на титрование которого пошло 2,2 мл 0,104 н. раствора NaOH. Коэффициент гигроскопичности равен 1,05. Величина гидролитической кислотности равна:
![]()
