
- •Практическое руководство по химии почв
- •Введение
- •Раздел I. Валовой анализ
- •1.1. Способы разложения почв
- •1.1.1. Разложение почв кислотами.
- •1.1.2. Разложение почв сплавлением.
- •1.1.3. Разложение почвы спеканием.
- •1.2. Определение гигроскопической влажности
- •1.3. Определение потери при прокаливании
- •1.4. Спекание почвы с содой
- •1.5. Анализ элементного состава почв
- •1.5.1. Определение кремния желатиновым методом
- •Пример расчета. Для спекания взято 1,0224 г прокаленной почвы. Прокаленный осадок SiO2 весит 0,8014 г. Содержание SiO2 равно:
- •1.5.2. Определение полуторных оксидов гравиметрическим методом
- •1.5.3. Определение железа фотометрическим методом
- •1.5.4. Определение алюминия фотометрическим методом
- •1.5.5.Вычисленное содержание алюминия по разности
- •1.5.6. Определение кальция и магния комплексонометрическим методом
- •1.5.6.1. Определение кальция
- •1.5.6.2. Определение суммы кальция и магния
- •1.5.7. Пероксидный метод определения титана
- •1.5.8. Определение фосфора фотометрическим методом
- •1.6. Способы выражения результатов валового анализа
- •1.7. Пересчеты данных валового анализа
- •1.8. Использование данных валового анализа
- •1.8.1. Использование элементного состава для суждения о генезисе почв.
- •1.8.2. Использование элементного состава для оценки потенциального плодородия почвы.
- •1.8.3. Использование данных элементного состава для расчета молекулярных отношений
- •1.8.4. Использование данных элементного состава для расчета запасов химических элементов
- •Пример расчета. Найти запас SiO2 в т/га если его содержание равно 80,63 %, плотность сложения почвы 1,18 г/см3, мощность слоя 9 см.
- •1.8.5. Использование данных элементного состава при изучении биологического круговорота веществ
- •1.8.6. Использование данных элементного состава для
- •1.8.6.1. Метод прямого сравнения
- •1.8.6.2. Методы стабильного компонента
- •1.8.6.2.1. Метод молекулярных отношений
- •1.8.6.2.2. Метод элювиально-аккумулятивных (еа) коэффициентов
- •1.8.6.2.3. Метод баланса веществ
- •1.8.7. Использование данных элементного состава для диагностики минералов илистой фракции.
- •Контрольные вопросы
- •Литература
- •Раздел II. Ионно-солевой комплекс почв
- •2.1. Метод водной вытяжки
- •2.1.1. Влияние солей на сельскохозяйственные культуры
- •2.1.2. Достоинства и недостатки водной вытяжки как метода изучения засоленных почв
- •2.1.3 Анализ водной вытяжки
- •2.1.3.1. Определение величины рН водной вытяжки
- •2.1.3.2. Определение величины сухого остатка
- •2.1.3.3. Определение величины прокаленного остатка
- •2.1.3.4. Определение щелочности от растворимых карбонатов
- •2.1.3.5. Определение общей щелочности
- •2.1.3.6. Определение хлорид-ионов
- •2.1.3.7. Определение сульфат-ионов
- •2.1.3.8. Определение ионов кальция и магния комплексонометрическим методом
- •2.1.3.8.1. Определение кальция
- •2.1.3.8.2. Определение суммы кальция и магния
- •2.1.3.9. Определение натрия и калия
- •2.1.3.9.1. Определение натрия и калия методом фотометрии пламени
- •2.1.3.9.2. Определение содержания натрия и калия по разности
- •Форма 4. Данные анализа водной вытяжки
- •2.1.4. Интерпретация данных водной вытяжки
- •2.1.4.1. Характеристика солевого режима почв по величине сухого остатка
- •2.1.4.2. Оценка химизма (типа) засоления почв.
- •2.1.4.2.1. Общие принципы оценки химизма засоления почв
- •2.1.4.2.2. Оценка степени засоления почв по содержанию токсичных ионов
- •2.1.4.2.3. Оценка степени засоления почв по «суммарному эффекту» токсичных ионов
- •2.1.5. Расчет промывной нормы
- •2.2. Катионообменная способность почв
- •2.2.1. Общие представления о катионообменной
- •2.2.2. Методы определения катионообменной способности почв
- •2.2.2.1. Оценка эффективной емкости катионного обмена
- •2.2.2.2. Определение стандартной емкости катионного обмена по Бобко-Аскинази в модификации цинао
- •2.2.2.3. Определение суммы обменных оснований методом Каппена-Гильковица
- •2.2.2.4. Определение гидролитической кислотности
- •2.2.2.5. Определение обменных катионов по методу Пфеффера в модификации в.А. Молодцова и и.В. Игнатовой
- •2.2.2.5.1. Определение кальция комплексонометрическим методом
- •2.2.2.5.2. Определение суммы кальция и магния комплексонометрическим методом
- •2.2.2.5.3. Определение натрия и калия методом фотометрии пламени
- •2.2.3. Использование результатов определения катионообменной способности почв
- •2.2.3.1. Вычисление степени насыщенности почв основаниями
- •2.2.3.2. Расчет дозы извести
- •2.2.3.3. Вычисление степени солонцеватости почв
- •2.2.3.4. Расчет дозы гипса
- •Контрольные вопросы
- •Литература
- •Раздел III. Органическое вещество почвы
- •3.1. Подготовка почвы для определения содержания и состава гумуса
- •3.2. Методы определения содержания общего гумуса почвы
- •3.2.1. Прямые методы определения содержания углерода органических соединений (гумуса) почвы.
- •3.2.2. Косвенные методы определения содержания углерода органических соединений (гумуса) почвы
- •3.2.2.1. Определение гумуса методом и.В.Тюрина в модификации в.Н.Симакова
- •3.2.2.2. Другие модификации метода и.В. Тюрина.
- •3.2.2.2.1. Спектрофотометрический метод определения содержания гумуса (д.С. Орлов, н.М. Гриндель)
- •3.2.2.2.2. Определение содержания органического углерода почвы методом и.В.Тюрина в модификации б.А.Никитина.
- •3.3. Методы определения общего содержания азота почвы.
- •3.3.1. Определение общего содержания азота методом Кьельдаля.
- •3.3.2. Определение общего содержания азота микрохромовым методом и.В. Тюрина.
- •3.4. Использование данных по содержанию общего гумуса и азота
- •3.4.1. Расчет отношения c:n
- •3.4.2. Вычисление запасов гумуса, углерода и азота.
- •3.5. Методы определение группового и фракционного состава гумуса.
- •3.5.1. Определение группового и фракционного состава гумуса по методу и.В. Тюрина в модификации в.В.Пономаревой и т.А.Плотниковой
- •3.5.2. Определение группового и фракционного состава гумуса по модифицированной схеме в.В.Пономаревой и т.А. Плотниковой (т.А. Плотникова, н.Е. Орлова, 1984).
- •Ход анализа
- •3.5.3. Ускоренный пирофосфатный метод определения состава гумуса по м.М. Кононовой и н.П. Бельчиковой
- •3.6. Методы изучения некоторых свойств гумусовых кислот при анализе фракционно-группового состава гумуса
- •3.6.1. Определение порога коагуляции гуминовых кислот.
- •3.6.2. Оптические свойства гумусовых веществ.
- •3.6.2.1. Электронные спектры поглощения гумусовых веществ
- •3.6.2.2. Определение коэффициента цветности q4/6
- •3.6.3. Гель-хроматография гумусовых веществ
- •3.7. Показатели гумусового состояния почв
- •Продолжение таблицы 31
- •3.8. Методы определения содержания и состава органического вещества в болотных торфяных почвах.
- •3.8.1. Определение потери при прокаливании и зольности торфа.
- •3.8.2. Одновременное определение общего содержания углерода и азота в торфяных почвах методом Анстета в модификации в.В. Пономаревой и т. А. Николаевой
- •Вычисление результатов анализа
- •Для анализа используют следующие реактивы:
- •3.8.3. Определение общего содержания азота в растительных материалах (торфах, лесных подстилках и пр.) методом к.Е. Гинзбурга и г.М. Щегловой
- •3.8.4. Определение содержания органического азота в вытяжках из торфов микрохромовым методом и.В. Тюрина
- •3.8.5. Определение состава органического вещества торфяно-болотных почв по методу в.В. Пономаревой и т.А. Николаевой.
- •Контрольные вопросы
- •Литература
- •Раздел I. Валовой анализ ……………………………………
- •Раздел II. Ионно-солевой комплекс почв ……………………
- •Раздел III. Органическое вещество почв
2.2.3. Использование результатов определения катионообменной способности почв
Данные, полученные при изучении катионообменной способности почвы, используют для дальнейших расчетов. С их помощью находят степень насыщенности почвы основаниями и степень солонцеватости почвы, рассчитывают дозы извести и гипса, необходимых для оптимизации реакции среды и состава обменных катионов.
2.2.3.1. Вычисление степени насыщенности почв основаниями
Степенью насыщенности почв основаниями называется отношение суммы обменных оснований к емкости поглощения выраженное в процентах.
В состав обменных катионов кислых почв наряду с поглощенными основаниями (главным образом Са и Мg) входят поглощенные ионы водорода и алюминия. Степень насыщенности показывает, какая часть от всех поглощенных катионов почвы приходится на поглощенные основания. Степень насыщенности основаниями вычисляют по формуле:
![]() ,
,
где V – степень насыщенности почвы основаниями, %; S – сумма обменных оснований, мг-экв.; H – гидролитическая кислотность, мг-экв.; S+H – емкость поглощения кислых почв; 100 – коэффициент пересчета в проценты.
По степени насыщенности основаниями почвы подразделяются на:
сильноненасыщенные – V < 30%
ненасыщенные – V = 30-50%
слабонасыщенные – V = 50-80%
насыщенные – V > 80%.
Степень насыщенности основаниями используют для определения потребности почв в известковании. При степени насыщенности основаниями > 75% почвы не нуждаются в известковании при насыщенности основаниями < 50% потребность в известковании обычно высокая.
Пример расчета. Анализировался пахотный горизонт дерново-подзолистой почвы. Сумма обменных оснований равна 5,0 мг-экв/ 100 г почвы, гидролитическая кислотность – 5,8 мг-экв/ 100 г почвы. Степень насыщенности почвы основаниями равна:
![]()
Почва ненасыщенна основаниями и нуждается в известковании.
2.2.3.2. Расчет дозы извести
Во многих регионах земного шара широко распространены почвы с кислой реакцией среды (подзолистые, дерново-подзолистые, серые лесные и др.). Кислая реакция среды обусловлена как ионами водорода почвенного раствора, так и обменными ионами водорода и алюминия. В кислых почвах создаются неблагоприятные условия для роста и развития большинства сельскохозяйственных культур, что ведет к снижению их урожайности. Негативное влияние повышенной кислотности на растения обусловлено различными причинами.
Кислые почвы характеризуются недостатком Са2+ и отчасти Mg2+, элементов, необходимых для нормального развития растений. В тоже время содержание Al3+, Mn2+, Н+ часто достигает токсичных для сельскохозяйственных культур концентраций. Кислая реакция среды угнетающе действует на аммонификацию, нитрификацию и фиксацию азота из воздуха, ухудшая азотный режим почвы, поскольку оптимум рН для развития микрофлоры, определяющей эти процессы, находится в пределах 6,5-8,0. В кислых почвах складывается неблагоприятный фосфатный режим, что обусловлено связыванием фосфора соединениями железа и алюминия, в результате чего он переходит в труднодоступное для растений состояние. При подкислении почв существенно возрастает растворимость и подвижность бора, меди, цинка, кобальта и других микроэлементов. Избыточное количество их подвижных форм оказывает токсичное действие на растения. В тоже время высокая кислотность снижает доступность растениям такого важного микроэлемента как молибден. В кислой среде ухудшаются условия гумусообразования, что ведет к преимущественному накоплению фульвокислот и низкомолекулярных органических соединений, менее ценных с агрономической точки зрения, чем гуминовые кислоты. Низкое содержание и неблагоприятный состав гумуса, наряду с дефицитом кальция, обусловливают неудовлетворительные физические свойства кислых почв. Они часто переуплотнены, плохо оструктурены, склонны к коркообразованию, что неблагоприятно отражается на их водно-воздушном режиме.
Эффективное использование сильнокислых и кислых почв возможно только после проведения химической мелиорации. Широко распространенным приемом повышения их плодородия служит известкование, устраняющее избыточную кислотность и способствующее насыщению ППК кальцием. При внесении в почву извести (СаСО3) она реагирует с углекислотой почвенного раствора и переходит в гидрокарбонат кальция, который взаимодействует с почвой:
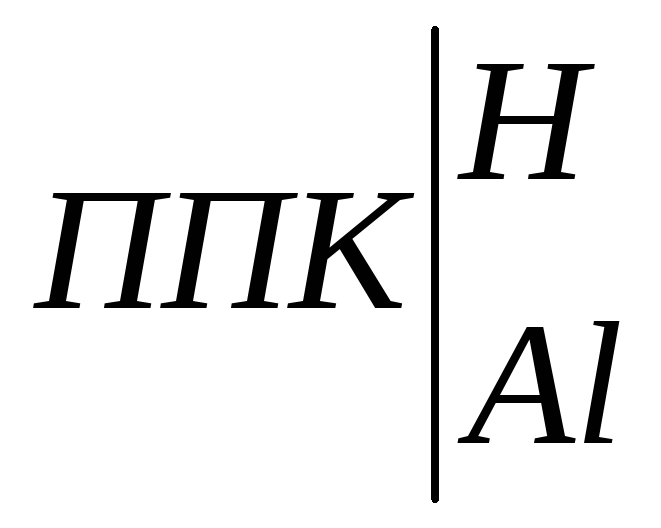 +
2Сa(HCO3)2
+
2Сa(HCO3)2
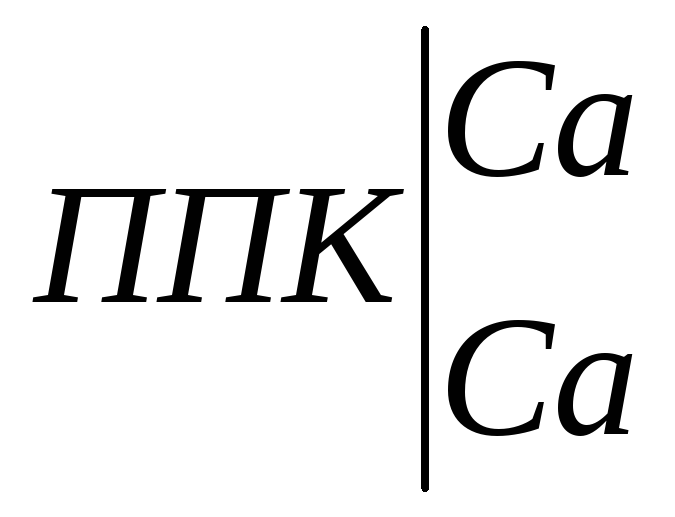 + H2O
+ 4CO2
+ Al(OH)3
+ H2O
+ 4CO2
+ Al(OH)3
Дозу извести, т/га, необходимую для оптимизации реакции среды, рассчитывают по величине гидролитической кислотности, которая рассматривается как суммарная кислотность почвы, состоящая из актуальной и потенциальной кислотности. Также необходимо знать мощность пахотного слоя и его плотность. Поскольку известь перемешивается со всем пахотным слоем необходимо найти его массу на площади 1 га по формуле:
M = dv ∙ h ∙ 100,
где M – масса пахотного слоя на площади 1 га, т/га; dv – плотность почвы, г/см3; h – мощность пахотного слоя, см; 100 – коэффициент пересчета.
После этого находят количество ионов водорода, содержащихся в пахотном слое, и с учетом уравнения химической реакции нейтрализации рассчитывают дозу извести, т/га.
Пример расчета. Мощность пахотного слоя равна 25 см, его плотность – 1,30 г/см3, гидролитическая кислотность – 5,2 мг-экв/100 г почвы. Масса пахотного слоя М = 1,30 ∙ 20 ∙ 100 = 2600 т. Поскольку в 100 г почвы содержится 5,2 мг-экв водорода, что соответствует 5,2 мг, то в 1 кг почвы будет содержаться 52 мг или 0,052 г водорода. Тогда во всем пахотном слое на площади 1 га содержание водорода составит: 0,052 ∙ 2 600 000 = 135 200 г, или 135,2 кг. На нейтрализацию 1 кг водорода требуется 50 кг извести, что вытекает из уравнения химической реакции:
2Н+ + СаСО3 = Са2+ + Н2О + СО2.
Следовательно, доза извести составит 135,2 ∙ 50 = 6760 кг, или 6,8 т/га.
Если известковые материалы содержат инертные примеси и имеют повышенную влажность, то дозу извести, т/га, находят по формуле:
![]() ,
,
где Д – доза извести, т/га; НГ – гидролитическая кислотность, мг-экв/100 г почвы; dV – плотность почвы, г/см3; h – мощность слоя, см; W – влажность мелиоранта, %; DB – содержание действующего вещества в мелиоранте, %.
